

所属成套资源:2026届高中化学一轮总复习 课时跟踪检测练习(含答案)
第18讲 硫及其化合物 课时跟踪检测练习(含答案)2026届高中化学一轮总复习
展开 这是一份第18讲 硫及其化合物 课时跟踪检测练习(含答案)2026届高中化学一轮总复习,共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
1.下列有关硫及其化合物的说法错误的是( )
A.SO2、SO3都属于酸性氧化物
B.硫在空气中燃烧的产物是SO3
C.浓硫酸具有吸水性,可用于干燥氢气
D.常温下,浓硫酸可以用铁罐储存和运输,因为铁在常温下与浓硫酸钝化
2.进行浓硫酸与蔗糖反应的实验时,无需标注的实验图标是( )
3.下列物质性质与用途具有对应关系的是( )
A.浓硫酸具有难挥发性,可用于制备HCl气体
B.SO2具有氧化性,工业上可用氨水吸收除去
C.Na2S具有还原性,可用于除去工业废水中的Hg2+
D.BaSO4难溶于水且不被X射线透过,可用作钡餐
4.(2024·大同模拟)下列现象或用途与浓硫酸的脱水性有关的是( )
A.浓硫酸可作氯气的干燥剂
B.浓硫酸滴加到胆矾上,蓝色晶体变成白色粉末
C.浓硫酸滴加到蔗糖中,蔗糖变黑
D.浓硫酸在加热条件下可与铜等不活泼金属反应
5.(2022·广东高考5题)若将铜丝插入热浓硫酸中进行如图(a~d 均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
A.Cu与浓硫酸反应,只体现H2SO4的酸性
B.a处变红,说明SO2是酸性氧化物
C.b或c处褪色,均说明SO2具有漂白性
D.试管底部出现白色固体,说明反应中无H2O生成
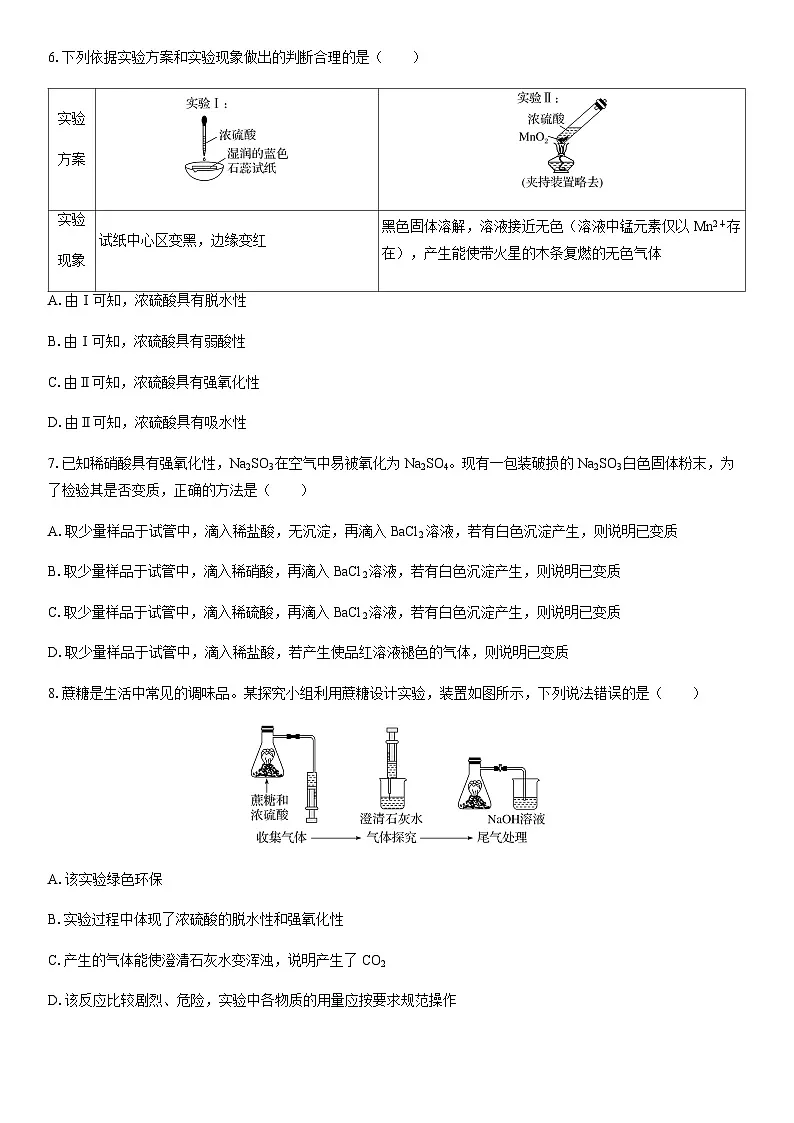
6.下列依据实验方案和实验现象做出的判断合理的是( )
A.由Ⅰ可知,浓硫酸具有脱水性
B.由Ⅰ可知,浓硫酸具有弱酸性
C.由Ⅱ可知,浓硫酸具有强氧化性
D.由Ⅱ可知,浓硫酸具有吸水性
7.已知稀硝酸具有强氧化性,Na2SO3在空气中易被氧化为Na2SO4。现有一包装破损的Na2SO3白色固体粉末,为了检验其是否变质,正确的方法是( )
A.取少量样品于试管中,滴入稀盐酸,无沉淀,再滴入BaCl2溶液,若有白色沉淀产生,则说明已变质
B.取少量样品于试管中,滴入稀硝酸,再滴入BaCl2溶液,若有白色沉淀产生,则说明已变质
C.取少量样品于试管中,滴入稀硫酸,再滴入BaCl2溶液,若有白色沉淀产生,则说明已变质
D.取少量样品于试管中,滴入稀盐酸,若产生使品红溶液褪色的气体,则说明已变质
8.蔗糖是生活中常见的调味品。某探究小组利用蔗糖设计实验,装置如图所示,下列说法错误的是( )
A.该实验绿色环保
B.实验过程中体现了浓硫酸的脱水性和强氧化性
C.产生的气体能使澄清石灰水变浑浊,说明产生了CO2
D.该反应比较剧烈、危险,实验中各物质的用量应按要求规范操作
9.如图是实验室进行二氧化硫制备与性质探究实验的组合装置,部分固定装置未画出。下列有关说法正确的是( )
A.关闭K1,打开K2,试剂X是酸性KMnO4或H2O2溶液,均可证明SO2有还原性
B.关闭K2,打开K1,滴加H2SO4溶液,装置B中每消耗1.5 ml Na2O2,转移电子数为1.5NA
C.为防止环境污染,装置C和E中的试剂均取用NaOH溶液
D.实验过程中体现了H2SO4的酸性、难挥发性、强氧化性
二、非选择题(本题包括2小题)
10.(2024·衡水模拟)Ⅰ.某同学设计实验探究Cu与98%浓硫酸的反应,装置如图所示,回答下列问题:
(1)试管①中发生反应的化学方程式为 。
(2)试管②用来检验生成的SO2,下列试剂中利用SO2的还原性进行检验的是 (填字母)。
A.酸性KMnO4溶液B.品红溶液
C.溴水D.Na2S溶液
(3)试管③中盛放 ,用来吸收SO2,防止污染空气。
Ⅱ.如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题:
(4)足量Y与1 ml金属铜充分反应,转移电子的物质的量为 ml。
(5)将Z通入X的水溶液中,发生反应的化学方程式为 。
(6)碳和M的浓溶液的反应中,氧化剂与还原剂物质的量之比为 。
11.某化学兴趣小组设计如下实验方案制备SO2并进行相关实验探究。
(1)装置A中反应的化学方程式为 。
(2)设计装置C的目的是验证SO2的 性,装置C中发生反应的离子方程式是 。
(3)选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱。
装置连接顺序为A、F、 、 、 、I,其中装置F的作用是 ,
通过 (填现象)即可证明亚硫酸的酸性强于次氯酸。
(4)装置D中NaOH全部转化为NaHSO3的标志是 。请设计简单实验测定室温下HSO3-的电离平衡常数Ka与水解平衡常数Kh的相对大小: 。
第18讲 硫及其化合物
1.B SO2、SO3都属于酸性氧化物,A正确;硫在空气中燃烧的产物是SO2,B错误;浓硫酸具有吸水性,可用于干燥氢气,C正确;常温下,铁在浓硫酸中钝化,浓硫酸可以用铁罐储存和运输,D正确。
2.D 浓硫酸具有强腐蚀性,实验时需要护目镜,A不符合题意;浓硫酸与蔗糖反应,生成有毒的SO2气体,反应时需要排风,B不符合题意;浓硫酸具有强腐蚀性,做完实验需要洗手,C不符合题意;此反应不需要用电,D符合题意。
3.A 具有难挥发性的浓硫酸可用于制备HCl气体,A正确;SO2是酸性氧化物,工业上可用氨水吸收除去,B错误;Na2S可用于除去工业废水中的Hg2+,是生成难溶性的硫化汞,与还原性无关,C错误;硫酸钡可用作钡餐是因为硫酸钡难溶于水,不能与胃液中的盐酸反应,且不被X射线透过,D错误。
4.C 浓硫酸作Cl2的干燥剂,体现的是其吸水性,A错误;浓硫酸加到胆矾上,蓝色晶体变成白色粉末,浓硫酸体现了吸水性,B错误;浓硫酸使蔗糖变黑,体现了浓硫酸的脱水性,C正确;在加热条件下,浓硫酸和铜等不活泼金属反应,体现了其强氧化性和酸性,D错误。
5.B Cu与浓硫酸反应生成Cu2+,体现了硫酸的氧化性,A项错误;能使紫色石蕊试液变红说明有酸性物质生成,可以说明SO2是酸性氧化物,B项正确;c处褪色,体现了SO2的还原性,C项错误;反应后混合液中硫酸浓度很高,浓硫酸吸水,导致生成的CuSO4不能形成蓝矾,D项错误。
6.A 浓硫酸滴到湿润的蓝色石蕊试纸上,试纸中心区变黑,边缘变红,说明浓硫酸具有脱水性,A正确;实验Ⅰ中试纸边缘变红,说明浓硫酸具有酸性,无法证明具有弱酸性,B错误;由实验Ⅱ可知,MnO2被还原为Mn2+,根据氧化还原反应规律推知,-2价O元素被氧化生成O2,产生能使带火星的木条复燃的无色气体,该反应中MnO2既是氧化剂又是还原剂,浓硫酸表现了酸性,C、D错误。
7.A 先滴入稀盐酸,若无沉淀,则排除了Ag+干扰,同时也把Na2SO3反应掉,再滴入BaCl2溶液,若有白色沉淀产生,则沉淀一定是BaSO4,从而证明样品已经变质,A正确;稀硝酸具有强氧化性,即使样品没有变质也会被硝酸氧化成Na2SO4,B错误;若先滴入稀硫酸会引入SO42-,再滴入BaCl2溶液,一定会产生BaSO4沉淀,C错误;滴入稀盐酸,产生使品红溶液褪色的气体,说明一定含有Na2SO3,但无法说明是否已经变质,D错误。
8.C 产生的气体能使澄清石灰水变浑浊,气体可能是二氧化硫,也可能是二氧化碳或二者的混合物,C错误。
9.C 关闭K1,打开K2,试剂X是H2O2溶液,反应无明显现象,不能证明SO2有还原性,A错误;关闭K2,打开K1,滴加H2SO4溶液,B中发生反应:Na2O2+SO2 Na2SO4,1个SO2分子发生反应,转移2个电子,则装置B中每消耗1.5 ml Na2O2,转移电子数为3NA,B错误;SO2与NaOH溶液反应,为防止环境污染,装置C和E中的试剂均取用NaOH溶液,C正确;该实验开始是硫酸和亚硫酸钠反应生成硫酸钠、二氧化硫气体和水,该反应是非氧化还原反应,没有体现H2SO4的强氧化性,D错误。
10.Ⅰ.(1)Cu+2H2SO4(浓) △ CuSO4+SO2↑+2H2O
(2)AC (3)NaOH溶液
Ⅱ.(4)1 (5)SO2+2H2S 3S↓+2H2O (6)2∶1
解析:Ⅰ.铜与浓硫酸共热生成CuSO4、SO2和H2O,试管②中可盛放酸性高锰酸钾溶液或溴水检验SO2,SO2会污染环境,试管③中应盛放NaOH溶液吸收SO2。Ⅱ.X为氢化物,硫元素化合价为-2价,X为H2S;Y为S单质;Z为氧化物,硫元素化合价为+4价,Z为SO2;M为酸,硫元素化合价为+6价,M为H2SO4;N为盐,硫元素化合价为-2价,N为含硫离子或硫氢根离子的盐。(1)试管①中反应的化学方程式为Cu+2H2SO4(浓) △ CuSO4+SO2↑+2H2O。(2)酸性KMnO4溶液与SO2反应,体现了SO2的还原性,A正确;SO2能使品红溶液褪色,体现了SO2的漂白性,B错误;溴水与SO2反应,体现了SO2的还原性,C正确;Na2S与SO2反应,体现SO2的氧化性,D错误。(3)试管③中盛放NaOH溶液,用于吸收SO2。(4)Y为S单质,加热条件下,硫与铜反应的方程式为2Cu+S △ Cu2S,铜元素化合价由0价升高到+1价,则1 ml金属铜充分反应,转移电子的物质的量为1 ml。(5)Z为SO2,X为H2S,SO2和H2S反应的化学方程式为SO2+2H2S 3S↓+2H2O。(6)M为H2SO4,碳与浓硫酸在加热条件下反应的化学方程式为C+2H2SO4(浓) △ CO2↑+2SO2↑+2H2O,其中碳是还原剂,硫酸是氧化剂,则氧化剂与还原剂物质的量之比为2∶1。
11.(1)CaSO3+2HCl CaCl2+SO2↑+H2O (2)还原 Br2+SO2+2H2O 4H++2Br-+SO42- (3)E H G 除去HCl气体 G中品红溶液不褪色,I中出现白色沉淀
(4)溶液由红色变为无色 常温下,用pH试纸(或pH计)测定NaHSO3溶液的pH,若pH<7,则Ka>Kh;若pH>7,则Ka<Kh
解析:(1)A中CaSO3和HCl发生复分解反应。(2)C中溴水与SO2发生氧化还原反应:Br2+SO2+2H2O 4H++2Br-+SO42-,SO2体现还原性。(3)亚硫酸和次氯酸盐发生氧化还原反应而不是复分解反应,要证明亚硫酸的酸性强于次氯酸,可以证明亚硫酸的酸性强于碳酸、碳酸的酸性强于次氯酸。A为SO2的发生装置,F能除去SO2中的HCl,通过E,发生反应:SO2+NaHCO3 CO2+NaHSO3,证明亚硫酸的酸性强于碳酸,通过H,除去CO2中的SO2,通过G,检验SO2已除尽,通过I,证明碳酸的酸性强于次氯酸。(4)装置D中NaOH全部转化为NaHSO3后,SO2开始漂白品红,则溶液由红色变为无色。HSO3-水解使溶液呈碱性,HSO3-电离使溶液呈酸性,通过测定溶液的pH,可以比较HSO3-的水解常数和电离常数的相对大小。
A.护目镜
B.排风
C.洗手
D.用电
实验
方案
实验
现象
试纸中心区变黑,边缘变红
黑色固体溶解,溶液接近无色(溶液中锰元素仅以Mn2+存在),产生能使带火星的木条复燃的无色气体
相关试卷
这是一份第18讲 硫及其化合物 课时跟踪检测练习(含答案)2026届高中化学一轮总复习,共7页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份2024届高考化学一轮复习 课时跟踪检测(十六) 硫及其化合物(含答案),共14页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份第16讲 氯及其化合物 课时跟踪检测练习(含答案)2026届高中化学一轮总复习,共9页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




