











所属成套资源:鲁科版高中化学高二上册(选必二)知识点串讲课件+分层训练+易错点精练+综合拔高练+专题训练+单元测试
选择性必修2共价键与分子的空间结构课堂教学课件ppt
展开 这是一份选择性必修2共价键与分子的空间结构课堂教学课件ppt,文件包含22共价键与分子的空间结构知识点串讲课件-鲁科版高中化学高二上册选必二pptx、221分子空间结构的理论分析分层训练含答案解析-鲁科版高中化学高二上册选必二docx、222分子的空间结构与分子性质分层训练含答案解析-鲁科版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
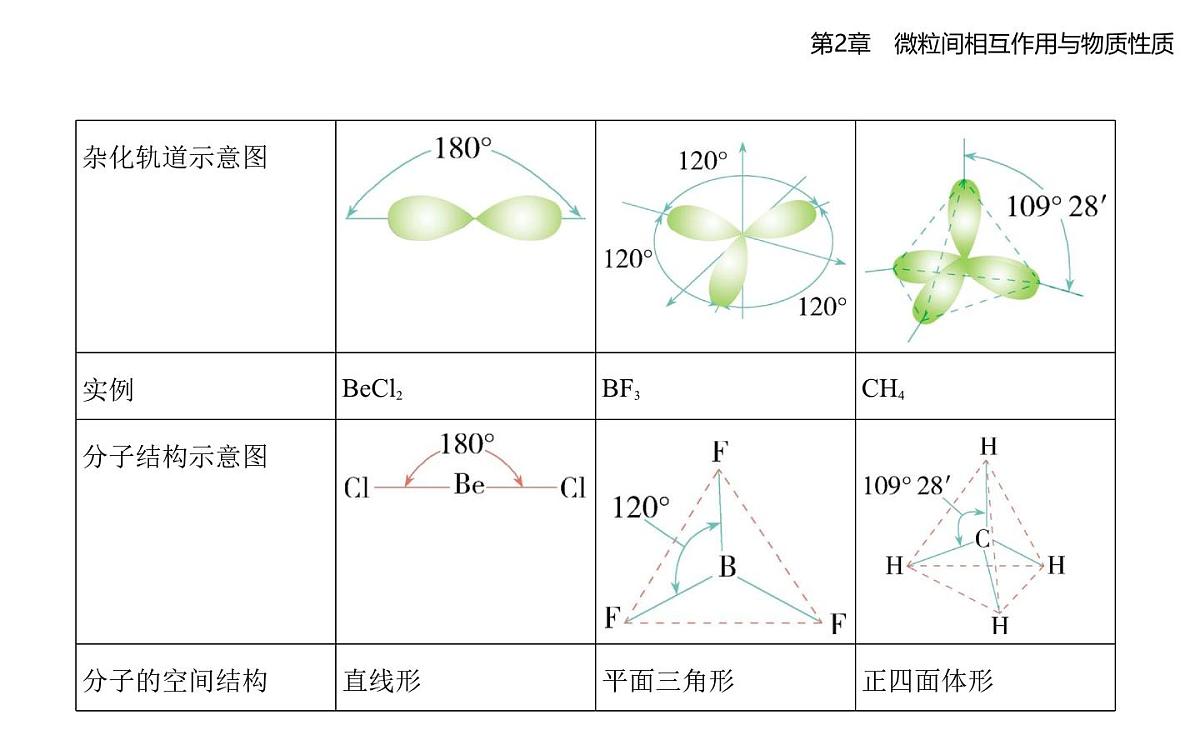
(2)杂化轨道理论要点①原子在成键时,同一原子中能量相近的原子轨道可重新组合成杂化轨道。②杂化前后原子轨道数目不变(参加杂化的轨道数目等于形成的杂化轨道数目),且杂化轨道的能量相同。③杂化改变了原子轨道的形状、方向,杂化使原子的成键能力增强。
归纳总结 对杂化过程的理解
(3)杂化轨道的类型与分子空间结构的关系 当杂化轨道全部用于形成σ键时,分子的空间结构与杂化轨道的空间结构相同,见下表:
(4)苯分子的空间结构① ②苯分子中的大π键:每个碳原子各有一个与碳环平面垂直的未参与杂化的2p轨道,这六个轨道相互平行且各有一个未成对电子,以“肩并肩”的方式相互重叠,从而形成属于六个碳原子的大π键。
(5)氨分子的空间结构 2.价电子对互斥理论(1)基本观点:分子中的中心原子的价电子对——成键电子对(bp)和孤电子对(lp)由于相互排斥作用,处于不同的空间取向且尽可能趋向于彼此远离。两个原子间的成键电子不论是单键
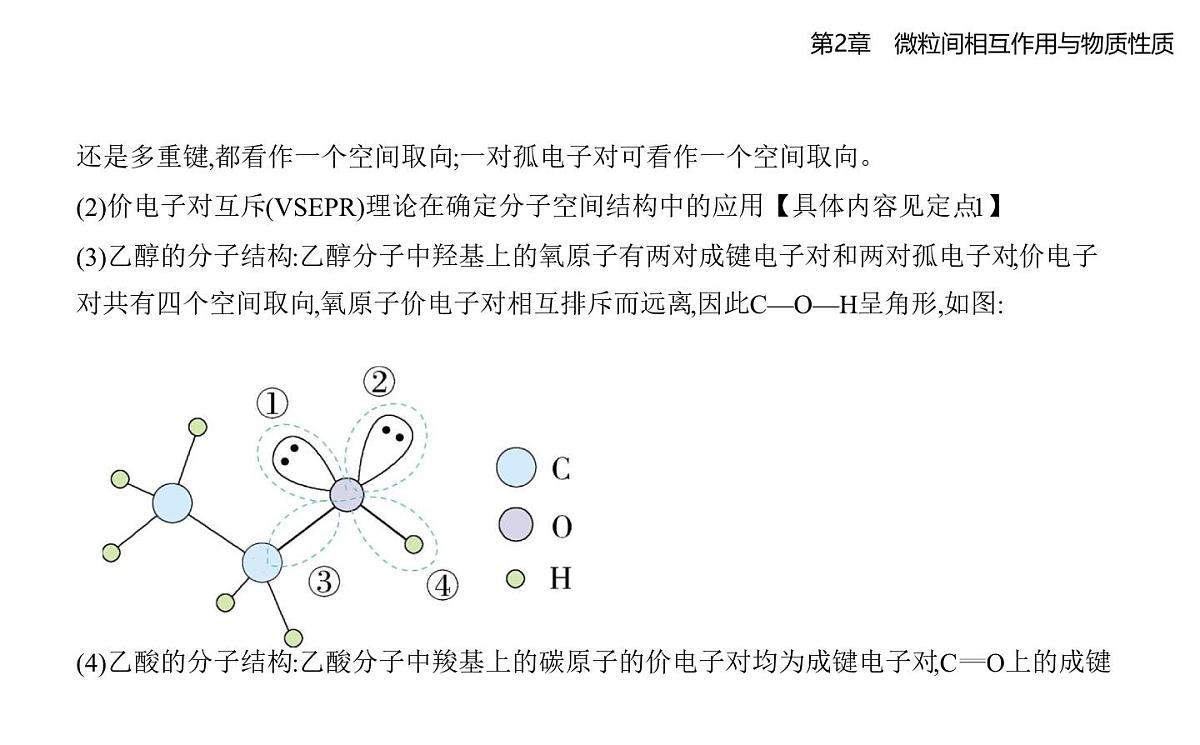
还是多重键,都看作一个空间取向;一对孤电子对可看作一个空间取向。(2)价电子对互斥(VSEPR)理论在确定分子空间结构中的应用【具体内容见定点1】(3)乙醇的分子结构:乙醇分子中羟基上的氧原子有两对成键电子对和两对孤电子对,价电子对共有四个空间取向,氧原子价电子对相互排斥而远离,因此C—O—H呈角形,如图: (4)乙酸的分子结构:乙酸分子中羧基上的碳原子的价电子对均为成键电子对,C O上的成键
电子对只有一个空间取向,因此碳原子的价电子对共有三个空间取向,相互排斥而远离,因此 部分呈三角形。
3.等电子原理(1)基本内容 化学通式相同且价电子总数相等的分子或离子具有相同的空间结构和相同的化学键类型等结构特征。(2)应用①判断一些简单分子或原子团的空间结构。a.S 、P 等离子具有AX4通式,价电子总数为32,中心原子采取sp3杂化,整个离子呈四面体形空间结构。b.S 、Cl 等离子具有AX3通式,价电子总数为26,中心原子采取sp3杂化,由于存在孤电子对,离子呈三角锥形空间结构。②利用等电子体在性质上的相似性制造新材料。
1.分子中的原子排布与对称性(1)对称分子①概念:依据对称轴的旋转或借助对称面的反映能够复原的分子。②与分子性质的关系:分子的许多性质如极性、旋光性等都与分子的对称性有关。(2)手性分子①手性:具有旋光性的分子本身和它们在镜中的像,就如同人的左手和右手,相似但不能重叠,因而称这类分子表现出手性。②不对称碳原子(也称手性碳原子):对于仅通过单键连接其他原子的碳原子,当其所连接的四个原子或基团均不相同时,这个碳原子称为不对称碳原子。③应用:手性分子缩合制蛋白质和核酸;药物的不对称合成。
2.分子中的电荷分布与极性(1)极性分子、非极性分子的概念①极性分子:分子内存在正、负两极的分子。②非极性分子:分子内不存在正、负两极的分子。(2)判断分子极性的方法【具体内容见定点3】(3)分子的极性对分子性质(沸点、溶解性)的影响①在相对分子质量相同的情况下,极性分子构成的物质比非极性分子构成的物质具有更高的沸点。②“相似相溶”原理:极性分子易溶于极性溶剂(如水),非极性分子易溶于非极性溶剂(如四氯化碳)。
知识辨析1.2s轨道与3p轨道能形成sp2杂化轨道,这种说法正确吗?2.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键,这种说法正确吗?3.Cl 、Cl 、Cl 中,中心原子Cl都是以sp3杂化轨道与O原子成键的,它们的空间结构都是正四面体形,这种说法正确吗?4.CH4、NH3、H2O中心原子的杂化类型都为sp3,键角依次减小,这种说法正确吗?5.含有非极性键的分子一定为非极性分子,这种说法正确吗?6.硝酸根离子中所有原子都在同一平面上,这种说法正确吗?7.H2O是极性分子,CO2可溶于H2O,因此CO2是极性分子,这种说法正确吗?
一语破的1.不正确。只有能量相近的原子轨道才能形成杂化轨道,2s轨道与3p轨道不在同一电子层,能量相差较大。2.不正确。如SO3的中心原子是采用sp2杂化轨道成键的。3.不正确。由VSEPR理论可知,Cl 、Cl 、Cl 中,中心原子Cl都是以sp3杂化轨道与O原子成键的,但它们的空间结构分别是V形、三角锥形、正四面体形。4.正确。CH4、NH3、H2O中心原子都采取sp3杂化,中心原子的孤电子对数依次为0、1、2,孤电子对数越多排斥作用越大,键角越小。5.不正确。H2O2是含有非极性键的极性分子。6.正确。N 中中心原子是氮原子,孤电子对数是0,价电子对数为3,空间结构为平面三角形,所有原子都在同一平面上。
7.不正确。CO2是非极性分子,CO2溶于H2O时,部分与H2O反应生成H2CO3。
1.中心原子价电子对数的确定方法(以ABx型分子为例) (1) (a-xb)中各字母的含义
①a表示中心原子的价电子数。对于主族元素:a=中心原子的主族序数。对于阳离子:a=中心原子的主族序数-离子的电荷数。对于阴离子:a=中心原子的主族序数+|离子的电荷数|。②b表示与中心原子结合的原子的未成对电子数。③x表示与中心原子结合的原子数。(2)举例分析SO2分子中S原子孤电子对数= (6-2×2)=1,SO2分子的价电子对数为2+1=3;S 中S原子的孤电子对数= (6+2-3×2)=1,S 的价电子对数为3+1=4;N 中N原子的孤电子对数= (5-1-4×1)=0,N 的价电子对数为4+0=4。
特别提醒 ①当孤电子对数为0.5时,按1对待。②多重键只计算σ键电子对,不计π键电子对。即,共价单键、双键、三键计算时,都只计入一个σ电子对。③该理论不适用于推测中心原子为过渡金属的粒子的空间结构。2.根据VSEPR理论判断分子或离子的空间结构(1)方法
(2)常见分子或离子的空间结构
3.键角大小比较(1)比较键角时,先看中心原子杂化类型,一般键角按sp、sp2、sp3顺序依次减小。(2)中心原子杂化类型相同时,孤电子对数越多,键角越小。(3)中心原子杂化类型、孤电子对数都相同时,中心原子的电负性越大,键角越大。
典例 氨基乙酸钠(H2NCH2COONa)用于有机产品的合成、工业洗涤剂中间体以及生化研究。下列说法正确的是 ( )A.碳、氮原子的杂化类型完全相同B.氨基乙酸钠中N原子的价电子对数为4C.1 ml氨基乙酸根离子中所含σ键为10 mlD.氮原子和与其成键的另外三个原子在同一平面内
思路点拨 首先写出氨基乙酸根离子的结构式,其结构式为 ,然后根据结构式、价电子对互斥理论判断。
解析 氨基乙酸钠分子中氮原子是sp3杂化,而碳原子是sp3、sp2杂化,A错误;氨基乙酸钠中存在2个N—H键、1个C—N键,N原子上含有1对孤电子对,则N原子的价电子对数为4,B正确;1 个氨基乙酸根离子中有一个碳氧双键,有8个σ键,C错误;由于氮原子为sp3杂化,故氮原子和与其成键的另外三个原子形成的是三角锥形结构,不可能共平面,D错误。
1.根据杂化轨道的空间结构判断
2.根据杂化轨道之间的夹角判断
3.根据杂化轨道数判断杂化轨道数=中心原子上的孤电子对数+中心原子结合的原子数,故由杂化轨道数可判断杂化轨道类型。
4.根据共价键类型判断 由杂化轨道理论可知,原子之间成键时,未参与杂化的p轨道可形成π键,杂化轨道用于形成σ键或容纳未参与成键的孤电子对。对于能够明确结构式的分子,其中心原子的杂化轨道数=中心原子形成的σ键数+中心原子上的孤电子对数。例如:①SiF4分子中,基态硅原子有4个价电子,与4个氟原子形成4个σ键,中心原子上无孤电子对,杂化轨道数为4,则SiF4分子中硅原子采取sp3杂化。②基态碳原子有4个价电子,在HCHO分子中,1个碳原子与2个氢原子形成2个σ键,与1个氧原子形成 键, 键中有1个σ键、1个π键,碳原子上无孤电子对,杂化轨道数为3,则HCHO分子中碳原子采取sp2杂化。
典例 下表中各粒子对应的空间结构及解释均正确的是 ( )
思路点拨 价电子对数 杂化轨道数 杂化轨道类型。
解析 氨基负离子中N原子价电子对数=2+ =4,且含有两对孤电子对,根据价电子对互斥理论知,该离子的空间结构为V形,N原子采用sp3杂化,故A错误。SO2中S原子价电子对数=2+ =3,且含有一对孤电子对,根据价电子对互斥理论知,该分子的空间结构为V形,S原子采用sp2杂化,水分子中O原子采用sp3杂化,故B错误。C2H2中C原子价电子对数都是2且不含孤电子对,该分子的空间结构为直线形,C原子采用sp杂化,且C原子的价电子均参与成键,故C正确。碳酸根离子中C原子价电子对数=3+ =3,且不含孤电子对,该离子的空间结构为平面三角形,C原子采用sp2杂化,故D错误。
1.只含有非极性键的双原子分子是非极性分子,如O2、H2等。2.含有极性键的双原子分子都是极性分子,如HCl、HF、HBr等。
3.含有极性键的多原子分子,空间结构对称的是非极性分子,如CO2、BF3等;空间结构不对称的是极性分子,如NH3、CH3Cl等。4.判断ABn型分子极性的经验规律:(1)若中心原子A的化合价的绝对值等于该元素所在的主族序数,则为非极性分子;若不等,则为极性分子。(2)若中心原子有孤电子对,则为极性分子;若无孤电子对,则为非极性分子。如CS2、BF3、SO3、CH4为非极性分子;H2S、SO2、NH3、PCl3为极性分子。
典例 下列物质:①BeCl2、②C2H4、③P4、④BF3、⑤NF3、⑥H2O2,其中含有极性键的非极性分子是 ( )A.①③④ B.②③⑥C.①②④ D.③④⑤
相关课件
这是一份选择性必修2共价键与分子的空间结构课堂教学课件ppt,文件包含22共价键与分子的空间结构知识点串讲课件-鲁科版高中化学高二上册选必二pptx、221分子空间结构的理论分析分层训练含答案解析-鲁科版高中化学高二上册选必二docx、222分子的空间结构与分子性质分层训练含答案解析-鲁科版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
这是一份鲁科版 (2019)选择性必修2共价键模型教课课件ppt,文件包含21共价键模型知识点串讲课件-鲁科版高中化学高二上册选必二pptx、211共价键分层训练含答案解析-鲁科版高中化学高二上册选必二docx、212键参数分层训练含答案解析-鲁科版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
这是一份高中化学鲁科版 (2019)选择性必修2共价键与分子的空间结构教学课件ppt,共50页。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)
.png)



