



所属成套资源:2026届高三化学二轮专题试题解析考点复习专题(Word版附解析)
2026届高三化学二轮专题试题解析复习第7章专题试题解析03化学平衡常数及相关计算(Word版附解析)
展开 这是一份2026届高三化学二轮专题试题解析复习第7章专题试题解析03化学平衡常数及相关计算(Word版附解析),文件包含第7章专题03化学平衡常数及相关计算原卷版docx、第7章专题03化学平衡常数及相关计算Word版含解析docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。
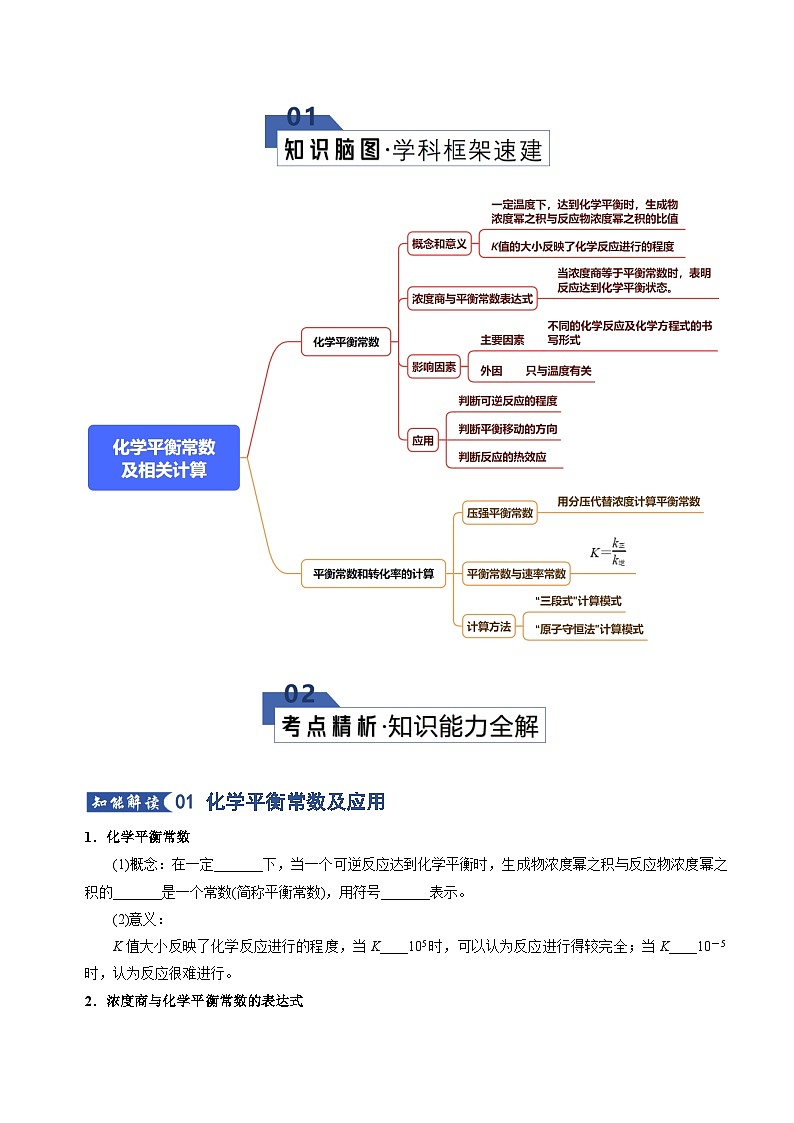
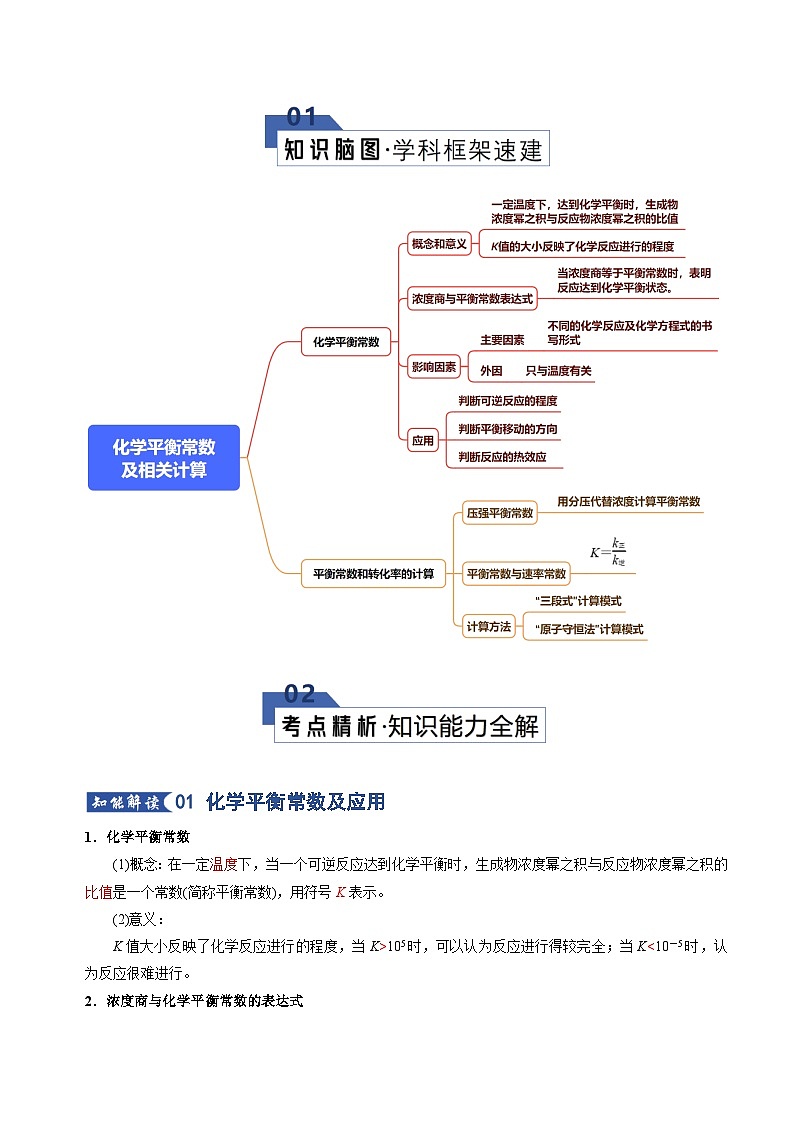
01 化学平衡常数及应用
1.化学平衡常数
(1)概念:在一定_______下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的_______是一个常数(简称平衡常数),用符号_______表示。
(2)意义:
K值大小反映了化学反应进行的程度,当K____105时,可以认为反应进行得较完全;当K____10-5时,认为反应很难进行。
2.浓度商与化学平衡常数的表达式
(1)浓度商:对于一般的可逆反应:mA(g)+nB(g)pC(g)+qD(g),在任意时刻的eq \f(cpC·cqD,cmA·cnB)称为浓度商,常用Q表示,即Q=______________。
(2)化学平衡常数表达式:当在一定温度下达到化学平衡时,K=______________。
(3)Q与K的关系:当反应中有关物质的浓度商等于平衡常数时,表明反应达到限度,即达到化学平衡状态。
3.化学平衡常数的影响因素
(1)内因:不同的化学反应及化学方程式的书写形式是决定化学平衡常数的主要因素。
(2)外因:在化学方程式一定的情况下,K只受_______影响。
4.平衡常数的应用
(1)判断可逆反应进行的程度
(2)判断反应是否达到平衡或进行的方向
对于化学反应aA(g)+bB(g)cC(g)+dD(g)的任意状态,浓度商Q=eq \f(ccC·cdD,caA·cbB)。
Q<K,反应向_______方向进行;
Q=K,反应处于_______状态;
Q>K,反应向_______方向进行。
(3)判断可逆反应的反应热
①升高温度eq \b\lc\{\rc\ (\a\vs4\al\c1(K增大,正反应为_______反应, K减小,正反应为_______反应))
②降低温度eq \b\lc\{\rc\ (\a\vs4\al\c1(K增大,正反应为_______反应, K减小,正反应为_______反应))
5.平衡转化率
(1)概念:某一反应的平衡转化率α等于该物质在反应中的___________(如物质的量、物质的量浓度等)与该物质___________的比值。
α = eq \f(该反应物的起始总量-该反应物的平衡量,该反应物的起始总量)×100%
(2)意义:反应的平衡转化率表示在一定_______和一定_________下反应进行的限度。
【跟踪训练】
1.书写下列化学反应的平衡常数表达式。
(1)Cl2+H2OHCl+HClO
(2)C(s)+H2O(g)CO(g)+H2(g)
(3)CH3COOH+C2H5OHCH3COOC2H5+H2O
(4)COeq \\al(2-,3)+H2OHCOeq \\al(-,3)+OH-
(5)CaCO3(s)CaO(s)+CO2(g)
2.在一定温度下,已知以下三个反应的平衡常数:
反应①:CO(g)+CuO(s)CO2(g)+Cu(s) K1
反应②:H2(g)+CuO(s)Cu(s)+H2O(g) K2
反应③:CO(g)+H2O(g)CO2(g)+H2(g) K3
K3与K1、K2的关系是K3=_____________________________。
3.甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关化学反应以及在不同温度下的化学反应平衡常数如表所示:
(1)根据表中信息推导出K1、K2与K3之间的关系,则K3=_________(用K1、K2表示)。
(2)反应③的ΔH______(填“>”或“”“=”或“0。某温度下,反应物的起始浓度分别为c(M)=1 ml·L-1,c(N)=2.4 ml·L-1。
(1)若达到平衡后,M的转化率为60%,列出“三段式”,计算此时N的平衡浓度是多少?平衡常数K是多少?
(2)若反应温度不变,反应物的起始浓度分别为c(M)=4 ml·L-1,c(N)=a ml·L-1;达到平衡后,c(P)=2 ml·L-1,则M的转化率为__________,N的起始浓度为____________。
2.内酯在化工、医药、农林等领域有广泛的应用。内酯可以通过有机羧酸异构化制得。某羧酸A在0.2 ml·L-1盐酸中转化为内酯B的反应可表示为A(aq)B(aq),忽略反应前后溶液体积变化。一定温度下,当A的起始浓度为a ml·L-1时,A的转化率随时间的变化如下表所示:
(1)反应进行到100 min时,B的浓度为________ ml·L-1。
(2)v正(t=50 min)________(填“>”“0,下列有关说法正确的是( )
A.平衡常数表达式为K=eq \f(cCO·cH2,cC·cH2O)
B.恒温条件下压缩容器的体积,平衡不移动,平衡常数K不发生变化
C.升高体系温度,平衡常数K减小
D.恒温恒压条件下,通入氦气,平衡正向移动,平衡常数K不发生变化
2.O3是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O3可溶于水,在水中易分解,产生的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生的反应如下:
反应① O3O2+[O] ΔH>0 平衡常数为K1;
反应② [O]+O32O2 ΔH0。
(1)此反应的平衡常数表达式为K=________。
(2)温度降低,则K________(填“增大”“减小”或“不变”)。
(3)已知1 100 ℃时,K=0.263。若1 100 ℃时测得c(CO2)=0.025 ml·L-1,c(CO)=0.01 ml·L-1,此时该反应________(填“处于”或“不处于”)化学平衡状态,化学反应速率:正反应速率______(填“>”“”“=”或“”“=”或“”“=”或“0。298 K时,将一定量N2O4气体充入恒容的密闭容器中发生反应。t1时刻反应达到平衡,混合气体平衡总压强为p,N2O4气体的平衡转化率为25%,则NO2的分压为________(分压=总压×物质的量分数),反应N2O4(g)2NO2(g)的平衡常数Kx=________[对于气相反应,用某组分B的物质的量分数x(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kx]。
4.设Keq \\al(r,p)为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以p0(p0=100 kPa)。在某温度下,原料组成n(CO)∶n(NO)=1∶1,发生反应:2CO(g)+2NO(g)N2(g)+2CO2(g),初始总压为100 kPa的恒容密闭容器中进行上述反应,体系达到平衡时N2的分压为20 kPa,则该反应的相对压力平衡常数Keq \\al(r,p)=________。
02 平衡常数的综合计算
(1)“三段式”法的计算模式
①根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度。
②计算各气体组分的物质的量分数或体积分数。
③根据分压计算公式求出各气体物质的分压,某气体的分压=气体总压强×该气体的体积分数(或物质的量分数)。
④根据平衡常数计算公式代入计算。
(2)“原子守恒法”计算平衡常数
原子守恒法解题的基本思路
【跟踪训练】
1.(2025·安徽卷)恒温恒压密闭容器中,时加入,各组分物质的量分数x随反应时间t变化的曲线如图(反应速率,k为反应速率常数)。
下列说法错误的是( )
A.该条件下
B.时间段,生成M和N的平均反应速率相等
C.若加入催化剂,增大,不变,则和均变大
D.若和均为放热反应,升高温度则变大
2.氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
工业上常用甲烷、水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.CH4(g)+H2O(g) CO(g)+3H2(g)
Ⅱ.CO(g)+H2O(g) CO2(g)+H2(g)
恒温恒压条件下,1 ml CH4(g)和1 ml H2O(g)反应达平衡时,CH4(g)的转化率为a,CO2(g)的物质的量为b ml,则反应Ⅰ的平衡常数Kx= (写出含有a、b的计算式;对于反应mA(g)+nB(g) pC(g)+qD(g),Kx=xp(C)·xq(D)xm(A)·xn(B),x为物质的量分数)。其他条件不变,H2O(g)起始量增加到5 ml,达平衡时,a=0.90,b=0.65,平衡体系中H2(g)的物质的量分数为 (结果保留两位有效数字)。
3.亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g)2NOCl(g)。
(1)在1 L恒容密闭容器中充入2 ml NO(g)和1 ml Cl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:
①反应开始到10 min时NO的平均反应速率v(NO)=________ ml·L-1·min-1。
②T2时该反应的平衡常数K=________。
③T2时Cl2的平衡转化率为__________。
(2)若按投料比n(NO)∶n(Cl2)=2∶1把NO和Cl2加入一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图B所示:
①该反应的ΔH____(填“>”“
相关试卷
这是一份2026届高三化学二轮专题试题解析复习第7章专题试题解析03化学平衡常数及相关计算(Word版附解析),文件包含第7章专题03化学平衡常数及相关计算原卷版docx、第7章专题03化学平衡常数及相关计算Word版含解析docx等2份试卷配套教学资源,其中试卷共30页, 欢迎下载使用。
这是一份2026届高三化学二轮专题试题解析复习第7章专题试题解析02化学平衡状态化学平衡的移动(Word版附解析),文件包含第7章专题02化学平衡状态化学平衡的移动原卷版docx、第7章专题02化学平衡状态化学平衡的移动Word版含解析docx等2份试卷配套教学资源,其中试卷共43页, 欢迎下载使用。
这是一份2026届高三化学二轮复习专题7化学反应速率与化学平衡试题(Word版附解析),文件包含专题7化学反应速率与化学平衡原卷版docx、专题7化学反应速率与化学平衡Word版含解析docx等2份试卷配套教学资源,其中试卷共34页, 欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




