所属成套资源:高考化学一轮复习讲练测 (2份,原卷版+解析版)
高考化学一轮复习讲练测第7章第03讲 化学平衡常数及其相关计算(练习)(2份,原卷版+解析版)
展开 这是一份高考化学一轮复习讲练测第7章第03讲 化学平衡常数及其相关计算(练习)(2份,原卷版+解析版),文件包含高考化学一轮复习讲练测第7章第03讲化学平衡常数及其相关计算练习原卷版docx、高考化学一轮复习讲练测第7章第03讲化学平衡常数及其相关计算练习解析版docx等2份试卷配套教学资源,其中试卷共32页, 欢迎下载使用。
题型一 化学平衡常数的含义与应用
1.(2024·甘肃平凉·模拟预测)催化氧化法将转化为的反应为。下列关于催化氧化法制的说法中错误的是
A.该反应的
B.该反应的平衡常数
C.使用合适的催化剂可提高化学反应速率,但不影响的平衡转化率
D.该反应在高温下可自发进行
2.(2024·江苏·模拟预测)对于二氧化硫的催化氧化反应:2SO2(g)+O2(g)2SO3(g),下列有关说法正确的是
A.该反应的ΔS>0
B.该反应平衡常数的表达式为K=
C.反应中每消耗22.4LO2(标准状况),转移电子数约为2×6.02×1023
D.温度不变,提高O2的起始浓度或增大反应压强,均能提高反应速率和SO2的转化率
3.(2024·天津·二模)反应可用于去除氮氧化物。催化该反应的过程如图所示。下列说法不正确的是
A.反应过程中,参与反应,降低了反应的焓变
B.该反应的平衡常数
C.其他条件不变时,增大,NO的平衡转化率增大
D.步骤Ⅲ中每消耗,转移电子数目为
7.(2024·江苏南京·模拟预测)在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式:
反应Ⅰ:CO2(g)+4H2(g)=CH4(g)+2H2O(g)△H=﹣164.7kJ•ml﹣1;反应Ⅱ:CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ•ml﹣1;反应Ⅲ:2CO(g)+2H2(g)=CO2(g)+CH4(g)△H=﹣247.1kJ•ml﹣1。
向恒压、密闭容器中通入1ml CO2和4ml H2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示。下列说法正确的是
A.反应II的平衡常数可表示为K=
B.图中曲线B表示CO的物质的量随温度的变化
C.该反应最佳控制温度在800℃~1000℃之间
D.提高CO2转化为CH4的转化率,需要研发在低温区高效的催化剂
5.(2024·江苏·二模)用消除的反应为 。下列说法正确的是
A.平衡时升高温度,增大,减小
B.反应平衡常数
C.反应中生成22.4 L ,转移电子数目为
D.实际应用中,适当增加的量有利于消除,减轻空气污染程度
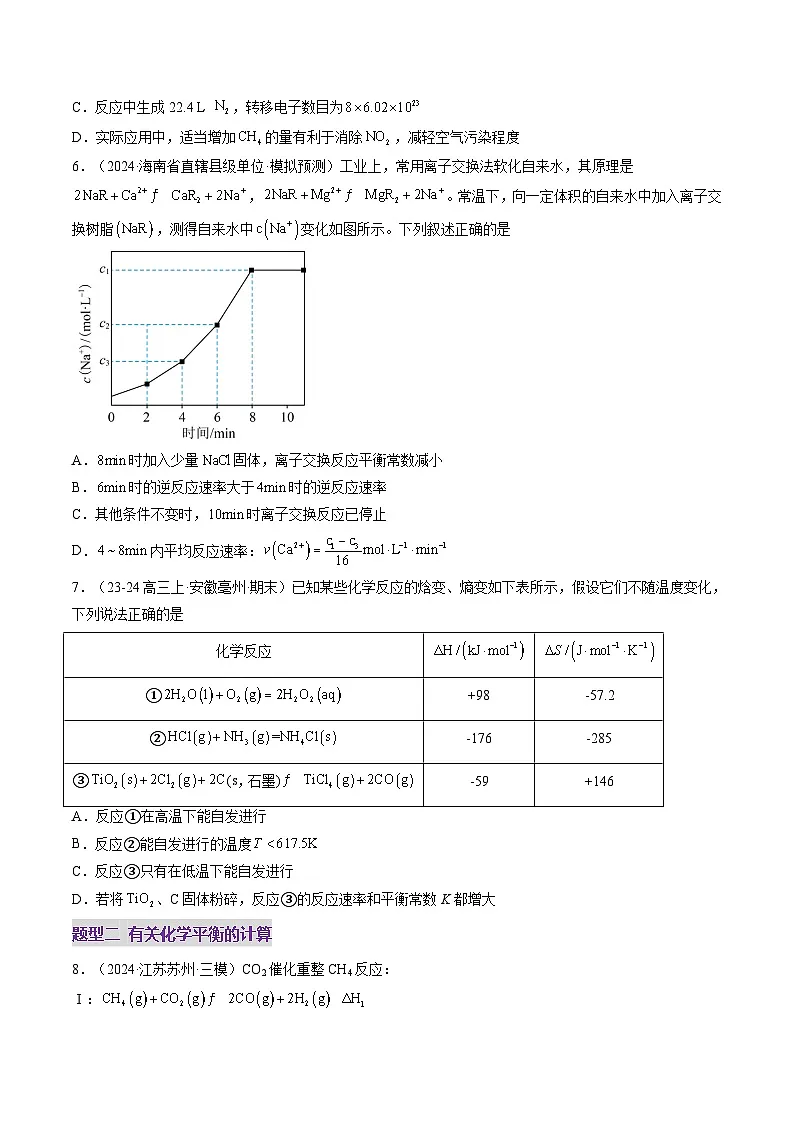
6.(2024·海南省直辖县级单位·模拟预测)工业上,常用离子交换法软化自来水,其原理是,。常温下,向一定体积的自来水中加入离子交换树脂,测得自来水中变化如图所示。下列叙述正确的是
A.时加入少量固体,离子交换反应平衡常数减小
B.时的逆反应速率大于时的逆反应速率
C.其他条件不变时,时离子交换反应已停止
D.内平均反应速率:
7.(23-24高三上·安徽亳州·期末)已知某些化学反应的焓变、熵变如下表所示,假设它们不随温度变化,下列说法正确的是
A.反应①在高温下能自发进行
B.反应②能自发进行的温度
C.反应③只有在低温下能自发进行
D.若将、C固体粉碎,反应③的反应速率和平衡常数K都增大
题型二 有关化学平衡的计算
8.(2024·江苏苏州·三模)CO2催化重整CH4反应:
Ⅰ:
Ⅱ:
Ⅲ:
在恒容反应器中按体积分数CH4:CO2=50%:50%投料。平衡时各物质的体积分数与温度的关系如图所示。若仅考虑上述反应,下列说法不正确的是
A.
B.其他条件不变,适当增大起始时CH4的体积分数,可抑制反应Ⅱ、Ⅲ的进行
C.T℃时,在2.0L容器中加入2mlCH4、2mlCO2以及催化剂进行重整反应,测得CO2的平衡转化率为75%,则反应Ⅰ的平衡常数小于81
D.300~580℃时,H2O的体积分数增大因为反应Ⅲ生成H2O的量大于反应Ⅱ消耗的量
9.(2024·湖南·模拟预测)利用测压法在恒容反应器中研究25℃时分解反应:
其中二聚为的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示:
已知:①时,完全分解;②;③为红棕色气体。下列说法错误的是
A.完全分解后,
B.若升高温度到35℃,则完全分解后体系压强(35℃)大于63.1kPa
C.若缩小起始时容器的体积,反应达到平衡后颜色将变浅
D.25℃时,反应达到平衡后,反应的平衡常数
10.(2024·黑龙江·三模)已知HCOOH水溶液在密封石英管中的分解反应如下:
I.
Ⅱ.
某温度下,在密封石英管内完全充满的HCOOH水溶液,使HCOOH分解,分解产物均完全溶于水,时刻测得、的浓度分别为、,反应Ⅱ达平衡时,测得的浓度为。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。下列有关说法错误的是
A.反应I比反应Ⅱ先达到平衡状态
B.反应I的平衡常数
C.体系达平衡后
D.对反应I有催化作用,若体系中还含有盐酸,则增大
11.(2024·广东佛山·模拟预测)某1L恒容密闭容器发生反应: 。向容器中通入0.2mlM和nmlN发生上述反应,测得M的平衡转化率与投料比以及温度的关系如图。下列说法正确的是
A.
B.时,C点的平衡常数值为2500
C.当时,反应达到平衡
D.其它条件不变,增大压强,可使B点移向C点
12.(2024·辽宁大连·一模)乙烯的产量是衡量一个国家石油化工发展水平的重要标志。一定条件下和合成乙烯的反应为。向1L恒容密闭容器中充入1ml 和3ml ,测得不同温度下的平衡转化率及催化剂的催化效率如题图所示。下列说法正确的是
A.升高温度,平衡向逆反应方向移动,催化剂的催化效率降低
B.图中M点乙烯的体积分数约为7.7%
C.250℃时,当的转化率位于点时,保持其他条件不变,仅延长反应时间不可能使转化率达到50%
D.向N点的平衡体系中充入1ml 和3ml ,其他条件不变,再次达到平衡时,增大
13.(23-24高三下·广东深圳·开学考试)氨催化氧化是硝酸工业的基础。工业上以氨气和氧气为原料,利用“氨催化氧化法”生产NO,在Pt-Rh合金催化剂作用下,发生主反应Ⅰ和副反应Ⅱ:
Ⅰ.
Ⅱ.
现将1 ml NH3、2 ml O2充入1 L恒容密闭容器中,在上述催化剂作用下,反应相同时间内,生成物的物质的量随温度变化曲线如图所示:
已知:有效转化率
下列说法不正确的是
A.工业上氨催化氧化生成NO时,最佳温度应控制在840℃左右
B.520℃时,NH3的有效转化率约为66.7%
C.反应Ⅱ可能是放热反应
D.该催化剂在高温时对反应Ⅰ的选择性更好
14.(23-24高三下·北京·开学考试)在恒容密闭容器中充入和,发生反应,实验数据如下表:
下列说法正确的是
A.实验①中,若时测得,则0至时间内,用N表示的平均反应速率
B.实验②中,若某时刻测得,则此时混合气体中的体积分数为
C.实验③中,达到平衡时,X的转化率为
D.实验④中,达到平衡时,
15.(2024·湖南长沙·模拟预测)向体积均为1L的两恒容容器中分别充入2ml X和1ml Y发生反应: ,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是
A.反应速率:B.气体的总物质的量:
C.a点平衡常数:D.
16.(2024·湖南邵阳·三模)汽车尾气净化反应为:、。向密闭容器中充入、,测得和的物质的量浓度与时间关系如图所示。下列说法正确的是
A.当体系中和浓度比不变时达到平衡状态
B.段反应速率
C.上述正反应在任何温度下都能自发进行
D.该温度下,上述反应的逆反应平衡常数
17.(2024·广东深圳·模拟预测)在甲、乙均为1L的恒容密闭容器中均充入2mlNO和2mlCO,在恒温和绝热两种条件下仅发生反应2NO(g)+2CO(g)N2(g)+2CO2(g) ∆H=-747kJ/ml,测得压强变化如图所示。下列说法错误的是
A.甲容器中的反应条件为绝热
B.乙容器中0~4min内υ(NO)=0.4ml•L-1•min-1
C.a点放出的热量为597.6kJ
D.Kb>Ka
18.(2024·河北衡水·模拟预测)某研究学习小组把一定量的固体X放入容积为2L的真空密闭容器中,在下分解:时达到化学平衡,随时间t变化曲线(时间段)如图所示.下列说法错误的是
A.在时间内该化学反应速率
B.T℃时,该反应的化学平衡常数K的值为0.0005
C.Z的体积分数不变证明该分解反应已经达到平衡
D.若其他条件不变,时将容器体积压缩到1L,时达到新的平衡,c(Z)在时间内的变化曲线如上图所示
19.(2024·上海·模拟预测)某研究组模拟三种已装固体V2O5催化剂的密闭容器装置,发生的反应为:2SO2(g)+O2(g)2SO3(g) ΔH1=-197.7kJ·ml-1
(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2mlSO2、1mlO2投料,达平衡时;三个容器中SO2的转化率从大到小的顺序为 (用“甲、乙、丙”表示)。
(2)下列均能作为容器甲和容器乙达平衡标志的是___________(填字母)。
A.温度不变B.密度保持不变C.压强保持不变D.O2浓度保持不变
(3)400℃,在容器丙中投入4mlSO2、2mlO2进行反应时,放出akJ热量;若在500℃,投入2mlSO2、1mlO2进行反应,放出bkJ热量,则a 2b(填“﹥”、“﹤”或“=”)。
20.(2024·贵州黔西·一模)氨具有较高的含氢量,可用作内燃机的燃料。
(1)液氨是重要的非水溶剂,和水类似,液氨的电离平衡为。写出与在液氨中发生中和反应的离子方程式为 。
(2)合成氨反应的方程式为,恒压密闭容器中,起始时,不同温度(T)下平衡混合物中物质的量分数随压强的变化曲线如图所示。
①25℃时,和的燃烧热分别为和,上述合成氨反应的焓变为 。
②A点温度迅速从变为,则此时浓度商Q (填“>”“<”或“=”)。
③ (为以分压表示的平衡常数,分压=总压×物质的量分数)。
④合成氨逆反应速率方程为v(逆)=k(逆),式中k(逆)为逆反应的速率常数(只与温度有关)。从C点开始减小压强,平衡发生移动,直至达到新的平衡,v(逆)的变化过程为 。
1.(2024·浙江·高考真题)二氧化碳氧化乙烷制备乙烯,主要发生如下两个反应:
I.
II.
向容积为的密闭容器中投入和,不同温度下,测得时(反应均未平衡)的相关数据见下表,下列说法不正确的是
注:乙烯选择性
A.反应活化能:
B.时,反应I的平均速率为:
C.其他条件不变,平衡后及时移除,可提高乙烯的产率
D.其他条件不变,增大投料比投料,平衡后可提高乙烷转化率
2.(2024·吉林·高考真题)异山梨醇是一种由生物质制备的高附加值化学品,时其制备过程及相关物质浓度随时间变化如图所示,后异山梨醇浓度不再变化。下列说法错误的是
A.时,反应②正、逆反应速率相等
B.该温度下的平衡常数:①>②
C.平均速率(异山梨醇)
D.反应②加入催化剂不改变其平衡转化率
3.(2023·湖南·高考真题)向一恒容密闭容器中加入和一定量的,发生反应:。的平衡转化率按不同投料比随温度的变化曲线如图所示。下列说法错误的是
A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为,当容器内压强不变时,反应达到平衡状态
4.(2022·海南·高考真题)某温度下,反应CH2=CH2(g)+H2O(g)CH3CH2OH(g)在密闭容器中达到平衡,下列说法正确的是
A.增大压强,,平衡常数增大
B.加入催化剂,平衡时的浓度增大
C.恒容下,充入一定量的,平衡向正反应方向移动
D.恒容下,充入一定量的,的平衡转化率增大
5.(2022·江苏·高考真题)用尿素水解生成的催化还原,是柴油机车辆尾气净化的主要方法。反应为,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中消耗,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
6.(2022·重庆·高考真题)两种酸式碳酸盐的分解反应如下。某温度平衡时总压强分别为p1和p2。
反应1:NH4HCO3(s)NH3(g)+H2O(g)+CO2(g) p1=3.6×104Pa
反应2:2NaHCO3(s)Na2CO3(s)+H2O(g)+CO2(g) p2=4×103Pa
该温度下,刚性密闭容器中放入NH4HCO3和Na2CO3固体,平衡后以上3种固体均大量存在。下列说法错误的是
A.反应2的平衡常数为4×106Pa2B.通入NH3,再次平衡后,总压强增大
C.平衡后总压强为4.36×105PaD.缩小体积,再次平衡后总压强不变
第03讲 化学平衡常数及其相关计算
01 模拟基础练
【题型一】化学平衡常数的含义与应用
【题型二】有关化学平衡的计算
02 重难创新练
03 真题实战练
化学反应
①
+98
-57.2
②
-176
-285
③(s,石墨)
-59
+146
t/min
0
40
80
160
260
1300
1700
p/kPa
35.8
40.3
42.5
45.9
49.2
61.2
62.3
63.1
实验编号
温度/℃
起始时物质的量/ml
平衡时物质的量/ml
①
700
0.40
0.10
0.090
②
800
0.10
0.40
0.080
③
800
0.20
0.30
a
④
900
0.10
0.15
b
温度()
400
500
600
乙烷转化率()
2.2
9.0
17.8
乙烯选择性()
92.6
80.0
61.8
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 








.png)
.png)



