






所属成套资源:人教版高中化学高二上册(选必二)知识点串讲课件+分层训练+易错点精练+专题强化练+综合拔高练
人教版 (2019)选择性必修2分子的空间结构一等奖课件ppt
展开 这是一份人教版 (2019)选择性必修2分子的空间结构一等奖课件ppt,文件包含22分子的空间结构知识点串讲课件人教版高中化学高二上册选必二pptx、222杂化轨道理论分层训练-人教版高中化学高二上册选必二docx、221分子结构的测定多样的分子空间结构价层电子对互斥模型分层训练-人教版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共36页, 欢迎下载使用。
1.三原子分子的空间结构有直线形和V形(又称角形)两种。如:
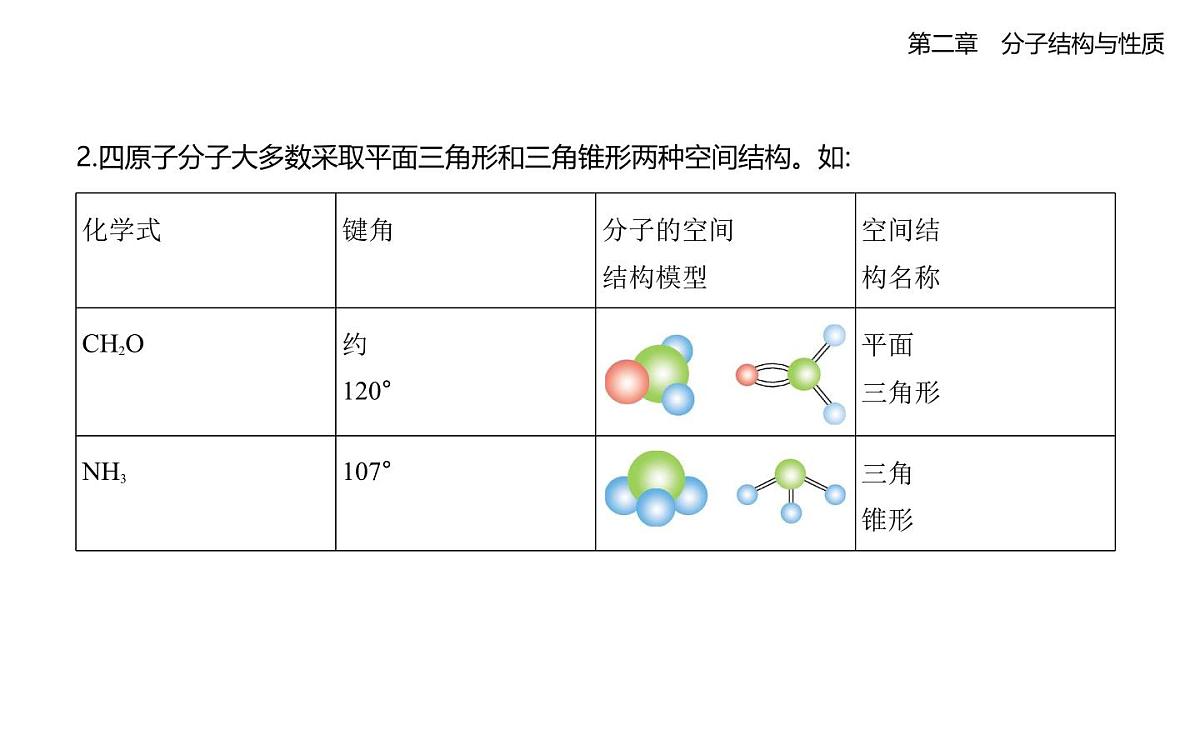
2.四原子分子大多数采取平面三角形和三角锥形两种空间结构。如:
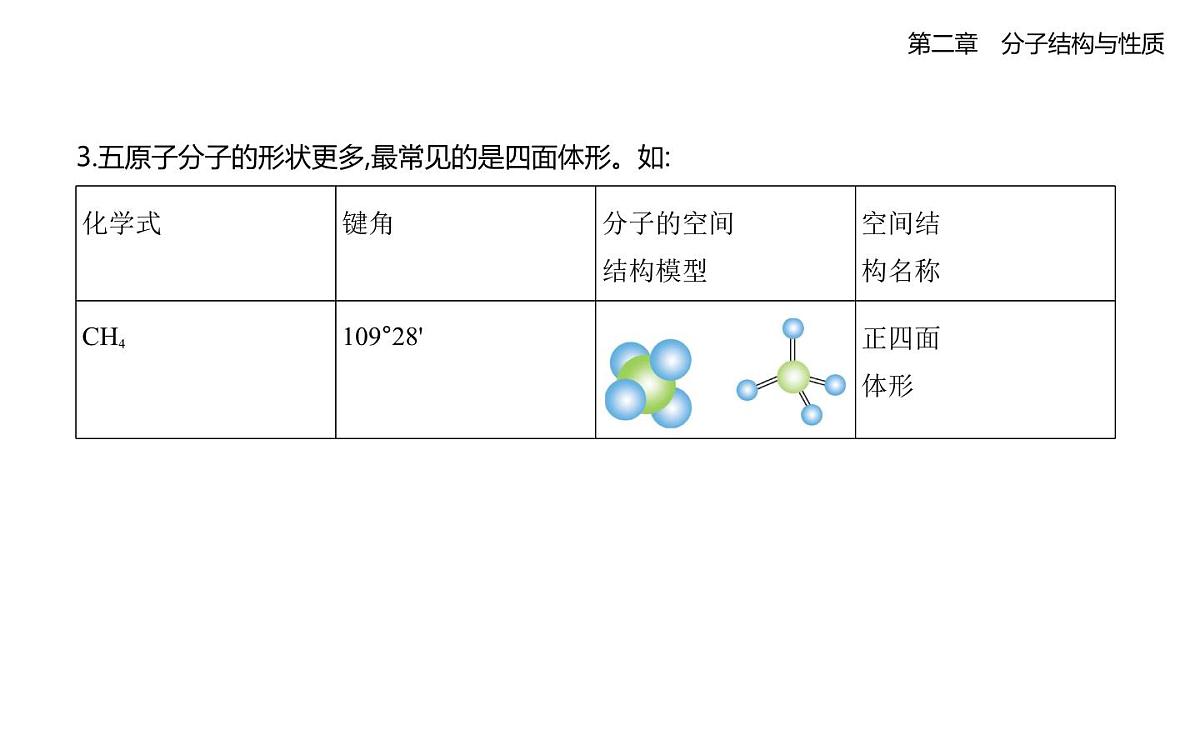
3.五原子分子的形状更多,最常见的是四面体形。如:
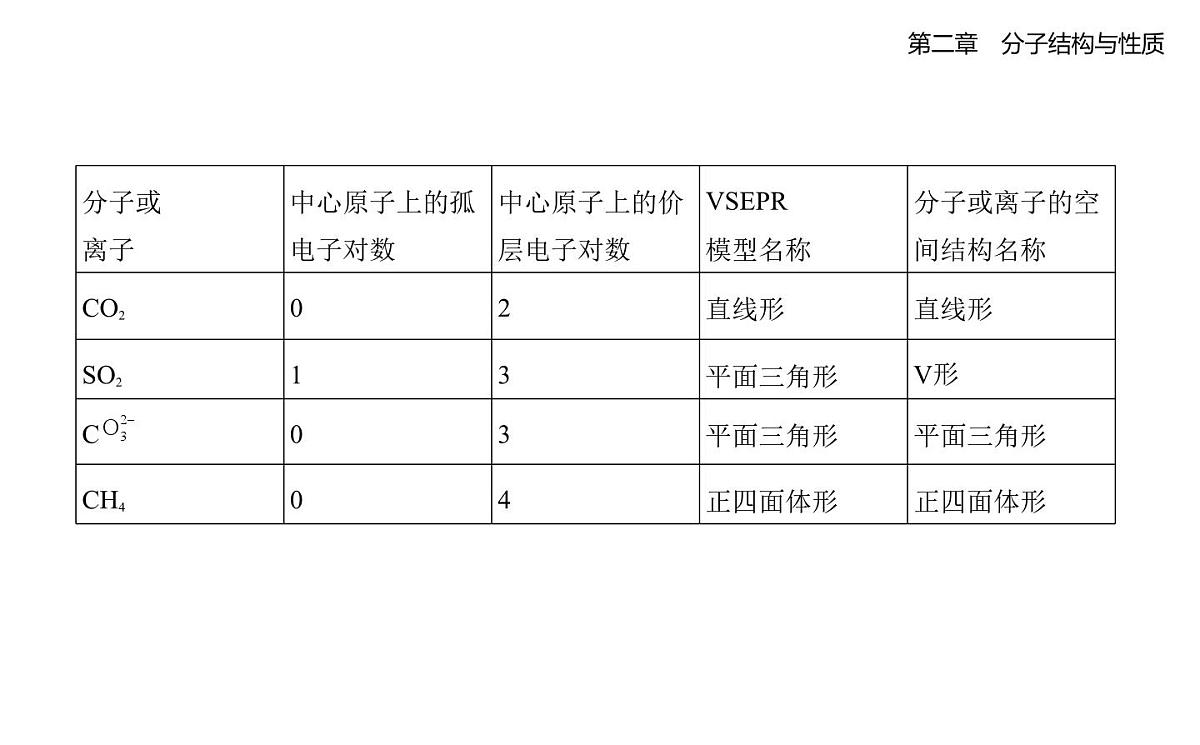
1.价层电子对互斥模型 对于ABn型的分子,分子的空间结构是中心原子A周围的“价层电子对”相互排斥的结果。2.价层电子对数的计算(详见定点1)3.VSEPR模型与分子或离子的空间结构σ键电子对数+中心原子上的孤电子对数=中心原子上的价层电子对数 VSEPR模型 分子或离子的空间结构。根据价层电子对互斥模型对几种分子或离子的空间结构的推测如下:
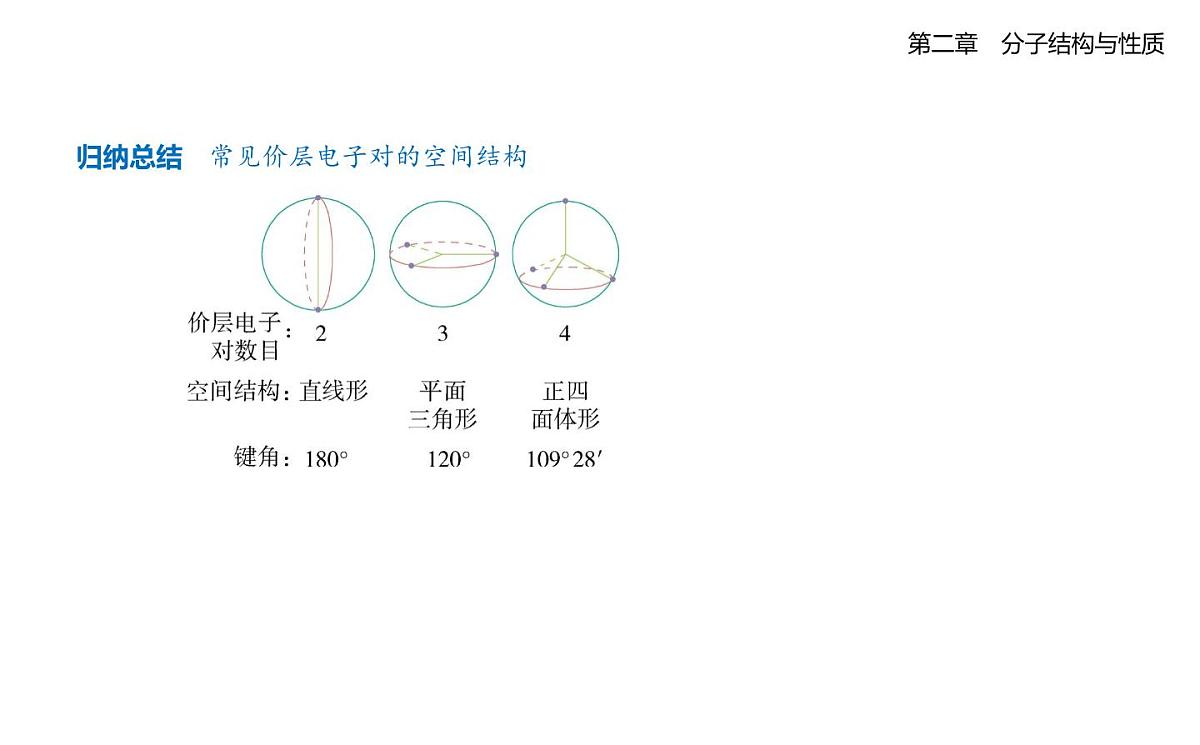
归纳总结 常见价层电子对的空间结构
1.杂化轨道的含义 在外界条件影响下,原子内部能量相近的原子轨道重新组合形成新的原子轨道的过程叫做原子轨道的杂化。重新组合后形成的一组新的原子轨道,叫做杂化原子轨道,简称杂化轨道。2.杂化的条件(1)只有在形成化学键时才能杂化;(2)只有能量相近的原子轨道间才能杂化。3.杂化轨道理论要点(1)杂化前后原子轨道数目不变(参加杂化的轨道数目等于形成的杂化轨道数目),且杂化轨道的能量相同。(2)杂化改变了原子轨道的形状、方向,杂化使原子的成键能力增强。(3)杂化轨道只用于形成σ键和容纳孤电子对。
归纳总结 对杂化过程的理解
4.杂化轨道的类型与分子或离子空间结构的关系 杂化后原子轨道在空间取最大夹角分布,能使相互间排斥力最小。(1)当杂化轨道全部用于形成σ键时,分子或离子的空间结构与杂化轨道的空间结构相同,见下表:
(2)当杂化轨道中有未参与成键的孤电子对时,孤电子对对成键电子对的排斥作用,会使分子或离子的空间结构与杂化轨道的形状有所不同。
知识拓展 sp3d杂化:三角双锥形,如PCl5。sp3d2杂化:八面体(等性杂化为正八面体)形,如SF6。sp杂化和sp2杂化这两种形式中,原子还有未参与杂化的p轨道,可用于形成π键,而杂化轨道用于形成σ键或者用来容纳未参与成键的孤电子对。
1.科学家研制出有望成为高效火箭推进剂的N(NO2)3,其结构为 。已知该分子中N—N—N键角都是108.1°,四个氮原子围成的空间是正四面体形,这种说法正确吗? 由于N—N—N键角都是108.1°,所以四个氮原子围成的空间不是正四面体形,而是三角锥形。2.CH4中C—H间的键角为109°28',NH3中N—H间的键角为107°,H2O中O—H间的键角为105°,说明孤电子对与成键电子对间的斥力大于成键电子对与成键电子对间的斥力,这种说法正确吗? 孤电子对与成键电子对间的斥力大于成键电子对间的斥力。
知识辨析 判断正误,正确的画“ √” ,错误的画“ ✕” 。
3.NF3的VSEPR模型和分子空间结构相同,这种说法正确吗? NF3的中心原子价层电子对数为4,VSEPR模型为四面体形,孤电子对数为1,分子空间结构为三角锥形。4.中心原子的价层电子都用于形成共价键的分子,其空间结构与VSEPR模型相同,这种说法正确吗? 中心原子的价层电子都用于形成共价键的分子,其空间结构与VSEPR模型相同,如CH4。5.CH4、NH3、H2O的中心原子的杂化轨道类型都为sp3,键角依次减小,这种说法正确吗? CH4、NH3、H2O的中心原子都采取sp3杂化,中心原子上的孤电子对数依次为0、1、2。由于孤电子对对成键电子对的排斥作用较大,使键角变小,孤电子对数越多排斥作用越大,键角越小。
6.分子的空间结构与化学式有必然联系,这种说法正确吗? AB2(或A2B)型分子可能是直线形分子,也可能是V形分子;AB3(或A3B)型分子可能是平面三角形分子,也可能是三角锥形分子。
1.利用价层电子对互斥模型判断分子或离子的空间结构的解题思路
定点 1 利用价层电子对互斥模型判断分子或离子的空间结构
2.确定中心原子价层电子对数(以ABx型分子为例) 价层电子对数=σ键电子对数+中心原子上的孤电子对数=x+ (a-xb)(1)σ键电子对数:根据与中心原子结合的原子数判断(由化学式确定)。(2)中心原子上的孤电子对数1)a的确定①对于主族元素:a=中心原子的价电子数;②对于阳离子:a=中心原子的价电子数-离子的电荷数;③对于阴离子:a=中心原子的价电子数+|离子的电荷数|。2)b表示与中心原子结合的原子最多能接受的电子数(氢为1;其他原子为“8减去该原子的价电子数”)。
特别提醒 当孤电子对数为0.5时,按1对待。3)举例①SO2分子中S原子的孤电子对数= (6-2×2)=1,SO2分子的中心原子价层电子对数=2+1=3;②S 中S原子的孤电子对数= (6+2-3×2)=1,S 的中心原子价层电子对数=3+1=4;③N 中N原子的孤电子对数= (5-1-4×1)=0,N 的中心原子价层电子对数=4+0=4。
特别提醒 多重键只计σ键电子对数,不计π键电子对数。即共价单键、双键、三键计算时,都只计一个σ键电子对。3.确定分子或离子的空间结构(1)若中心原子没有孤电子对,则VSEPR模型与分子或离子的空间结构一致。(2)若中心原子有孤电子对,孤电子对与成键电子对相互排斥规律:孤电子对—孤电子对>孤电子对—成键电子对>成键电子对—成键电子对。随着孤电子对数目的增多,成键电子对与成键电子对之间的键角减小。如CH4、NH3和H2O分子中的键角依次减小。
知识拓展 键角大小规律①相同类型的分子,中心原子相同时,周围原子电负性越大,键角越小,如键角NH3>NCl3>NF3。②相同类型的分子,中心原子不同,周围原子相同时,中心原子电负性越大,键角越大,如键角NH3>PH3>AsH3。
(3)常见分子或离子空间结构的判断①中心原子不含孤电子对
典例1 下列分子或离子中,VSEPR模型名称与分子或离子的空间结构名称不一致的是 ( )A.CO2 B.C C.H2O D.CCl4
思路点拨 VSEPR模型即价层电子对互斥模型,分子或离子的空间结构是指分子或离子中的原子在空间的排布,不包括中心原子的孤电子对。若中心原子上的价层电子对数为4,不含孤电子对,则分子或离子的空间结构为四面体形;含有一个孤电子对,为三角锥形;含有两个孤电子对,为V形。若中心原子上的价层电子对数为3,不含孤电子对,则分子或离子的空间结构为平面三角形;含有一个孤电子对,为V形。若中心原子上的价层电子对数为2且不含孤电子对,则分子或离子的空间结构为直线形。
解析 A项,CO2分子中每个O原子和C原子形成两对共用电子,所以C原子价层电子对数是2,VSEPR模型为直线形,且中心原子上没有孤电子对,CO2分子的空间结构为直线形,VSEPR模型与空间结构一致,故A不符合题意;B项,C 的中心原子C原子上有3个σ键电子对,中心原子上的孤电子对数= ×(4+2-3×2)=0,所以C原子价层电子对数是3,VSEPR模型为平面三角形,且不含孤电子对,C 的空间结构为平面三角形,VSEPR模型与空间结构一致,故B不符合题意;C项,水分子的中心原子O原子价层电子对数=2+ ×(6-2×1)=4,VSEPR模型为四面体形,孤电子对数为2,略去孤电子对后,实际空间结构是V形,VSEPR模型与空间结构不一致,故C符合题意;D项,CCl4分子中,中心原子C原子上的价层电子对数=σ键电子对数+孤电子对数=4+ ×(4-1×4)=4,VSEPR模型为正四面体形,中心原子上没有孤电子对,空间结构为正四面体形,VSEPR模型与空间结构一致,故D不符合题意。
典例2 用价层电子对互斥模型可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是 ( )A.PCl3为平面三角形分子B.SO3与C 均为平面三角形结构C.SO2键角大于120°D.BF3是三角锥形分子
思路点拨 先计算中心原子的价层电子对数,再结合中心原子的孤电子对数确定微粒的空间结构。
解析 PCl3分子中,P原子的价层电子对数为3+ ×(5-3×1)=4,含有1个孤电子对,分子应为三角锥形,A错误;SO3和C 中S和C的价层电子对数均为3,中心原子均无孤电子对,空间结构均为平面三角形,B正确;SO2的中心原子为硫原子,其价层电子对数为2+ ×(6-2×2)=3,有1个孤电子对,孤电子对对两个成键电子对的斥力大,键角小于120°,C错误;BF3的中心原子为B原子,其价层电子对数为3+ ×(3-3×1)=3,无孤电子对,空间结构为平面三角形,D错误。
特别提醒 利用VSEPR模型确定分子的空间结构的注意事项(1)对于ABn型分子,成键电子对数等于与中心原子相连的原子个数。(2)分子的中心原子上孤电子对数为0时,VSEPR模型与分子空间结构相同。(3)分子的空间结构与分子类型有关,如AB2型分子只能为直线形或V形结构,AB3型分子只能为平面三角形或三角锥形结构,故根据分子类型(ABn型)和孤电子对数能很快确定分子的空间结构。
1.根据价层电子对数、杂化轨道的空间结构判断
2.根据杂化轨道之间的夹角判断
3.根据杂化轨道数判断 杂化轨道数=中心原子上的孤电子对数+中心原子结合的原子数,故由杂化轨道数可判断杂化轨道类型。
4.根据共价键类型判断 由杂化轨道理论可知,原子之间成键时,未参与杂化的p轨道可形成π键,杂化轨道用于形成σ键或容纳未参与成键的孤电子对。对于能够明确结构式的分子,其中心原子的杂化轨道数=中心原子形成的σ键数+中心原子上的孤电子对数。例如:①SiF4分子中,基态硅原子有4个价层电子,与4个氟原子形成4个σ键,中心原子上无孤电子对,杂化轨道数为4,则SiF4分子中硅原子采取sp3杂化。②基态碳原子有4个价层电子,在HCHO分子中,1个碳原子与2个氢原子形成2个σ键,与1个氧原子形成 键, 键中有1个σ键、1个π键,碳原子上无孤电子对,杂化轨道数为3,则HCHO分子中碳原子采取sp2杂化。
典例 下表中各粒子对应的空间结构及解释均正确的是 ( )
相关课件
这是一份人教版 (2019)选择性必修2分子的空间结构一等奖课件ppt,文件包含22分子的空间结构知识点串讲课件人教版高中化学高二上册选必二pptx、222杂化轨道理论分层训练-人教版高中化学高二上册选必二docx、221分子结构的测定多样的分子空间结构价层电子对互斥模型分层训练-人教版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共36页, 欢迎下载使用。
这是一份苏教版 (2019)选择性必修2分子的空间结构课堂教学ppt课件,文件包含第一单元分子的空间结构知识点串讲课件-苏教版高中化学高二上册选必二pptx、第1课时分子的空间结构模型分层训练含答案解析-苏教版高中化学高二上册选必二docx、第2课时分子的极性手性分子分层训练含答案解析-苏教版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
这是一份选择性必修2共价键与分子的空间结构课堂教学课件ppt,文件包含22共价键与分子的空间结构知识点串讲课件-鲁科版高中化学高二上册选必二pptx、221分子空间结构的理论分析分层训练含答案解析-鲁科版高中化学高二上册选必二docx、222分子的空间结构与分子性质分层训练含答案解析-鲁科版高中化学高二上册选必二docx等3份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)
.png)



