




所属成套资源:新苏教版化学选择性必修1课件PPT+知识清单+分层练习+单元测试
选择性必修1化学平衡的移动完美版课件ppt
展开 这是一份选择性必修1化学平衡的移动完美版课件ppt,文件包含苏教版高中化学选择性必修第一册231《影响化学平衡移动的因素》课件pptx、浓度对平衡的影响mp4等2份课件配套教学资源,其中PPT共44页, 欢迎下载使用。
1.从变化角度认识化学平衡的移动,即浓度、压强、温度对化学平衡的影响。2.从Qc与K关系及浓度、温度、压强对反应速率、平衡的影响,推断平衡移动的方向。3.通过实验论证浓度、压强、温度对化学平衡的影响。
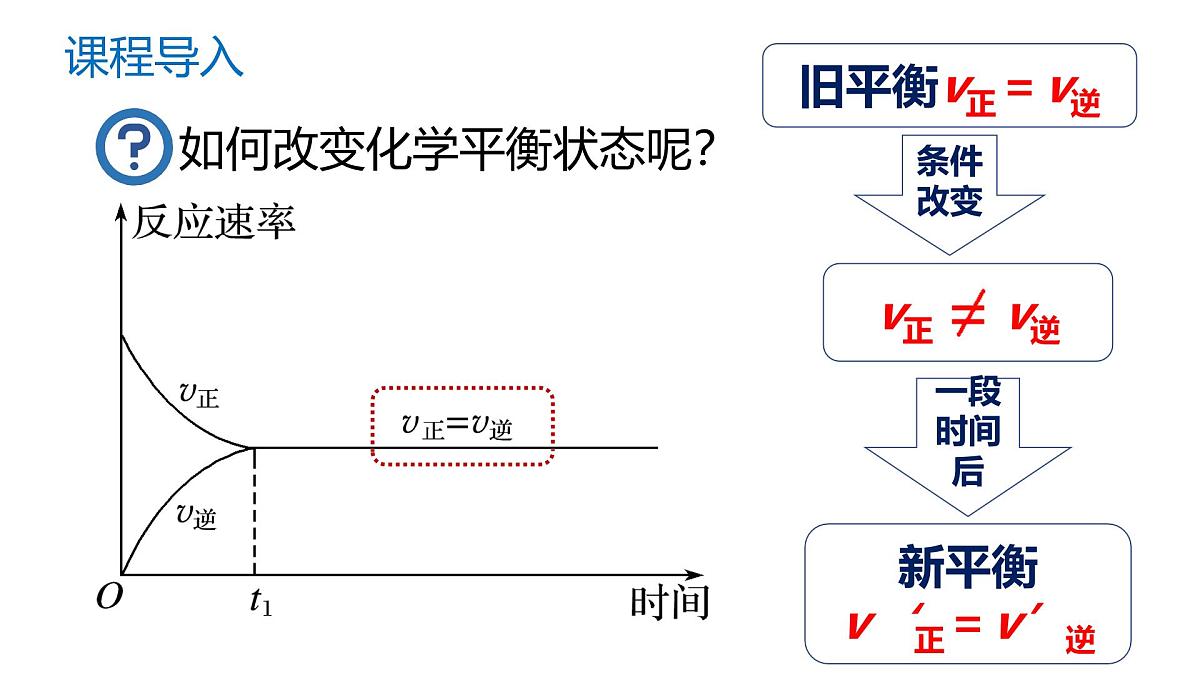
如何改变化学平衡状态呢?
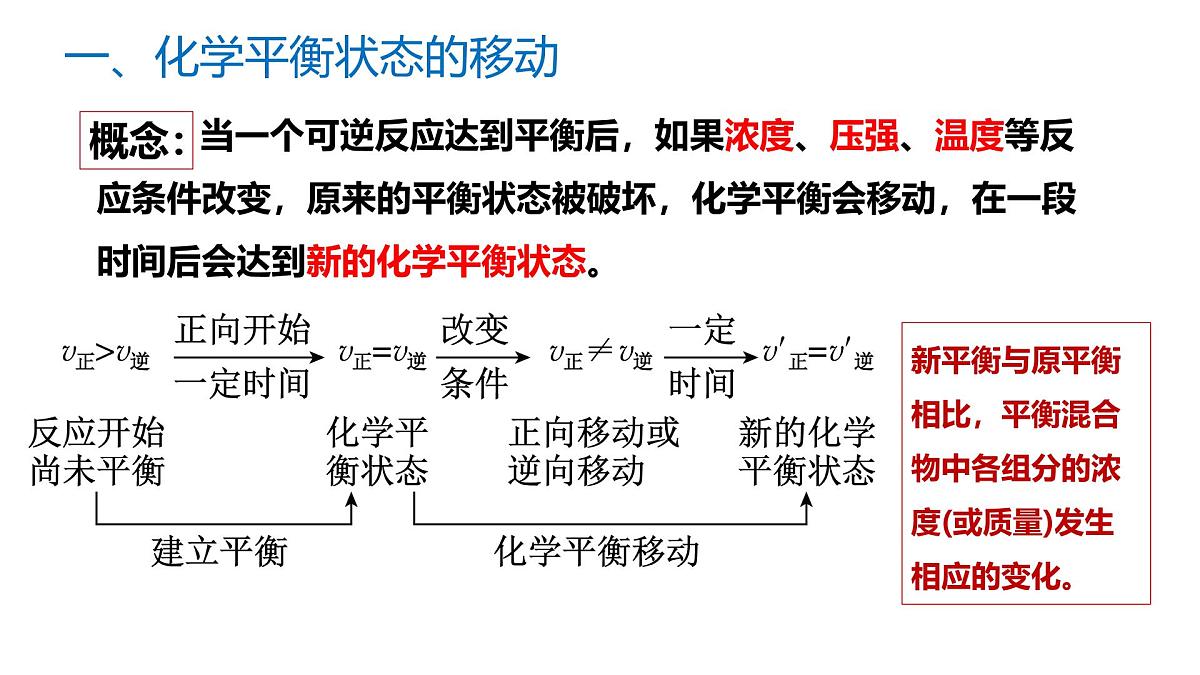
一、化学平衡状态的移动
当一个可逆反应达到平衡后,如果浓度、压强、温度等反应条件改变,原来的平衡状态被破坏,化学平衡会移动,在一段时间后会达到新的化学平衡状态。
新平衡与原平衡相比,平衡混合物中各组分的浓度(或质量)发生相应的变化。
改变条件后,①v正≠v逆,②各组分的百分含量发生改变。
化学平衡移动方向的判断:
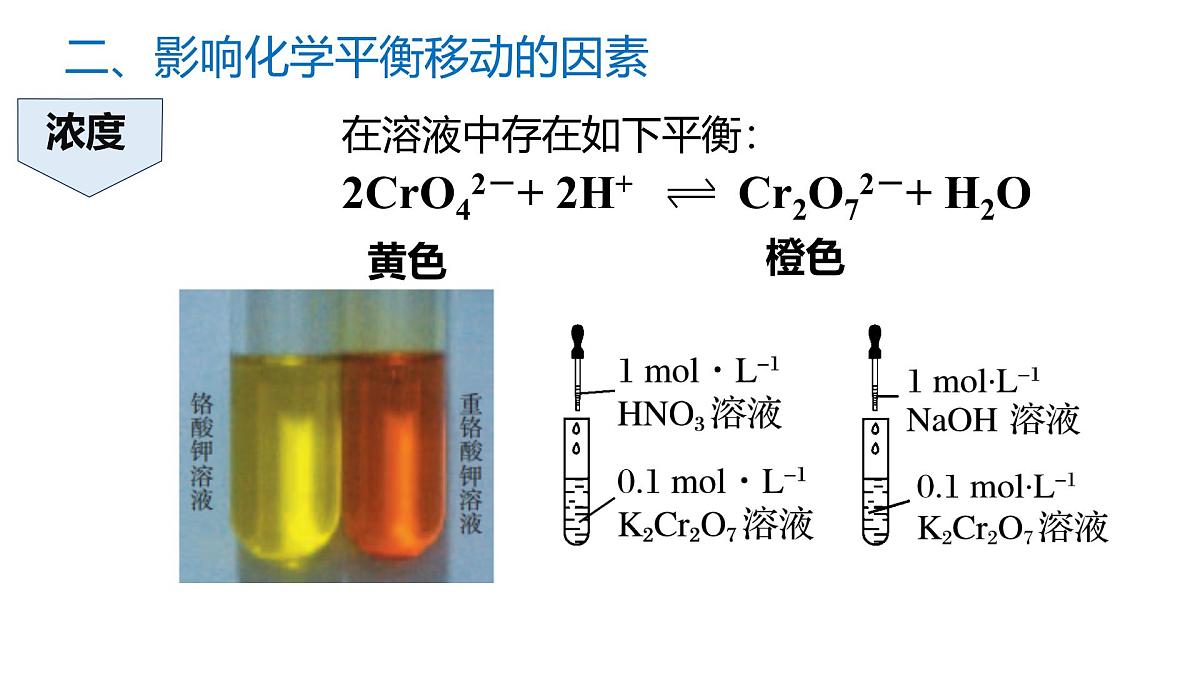
2CrO42-+ 2H+ Cr2O72-+ H2O
在溶液中存在如下平衡:
二、影响化学平衡移动的因素
NaOH溶液使c(H+)变小
平衡向生成Cr2O72-或CrO42-减小方向移动
平衡向生成CrO42-或Cr2O72-减小方向移动
②c(反应物)减小或c(生成物)增大,平衡向逆反应方向移动。
浓度对化学平衡移动的影响规律
①c(反应物)增大或c(生成物)减小,平衡向正反应方向移动。
反应物 生成物
浓度对化学平衡的影响规律的解释
m A(g) + n B(g) p C(g) + q D(g)
增大c(反应物)减小c(生成物)
减小c(反应物)增大c(生成物)
用v-t图像分析浓度变化对化学平衡移动的影响
t1时刻,增大反应物浓度
v′正增大,而v′逆不变
t1时刻,减小生成物浓度
v′逆减小,而v′正不变
总结:在其他条件不变的情况下,增大反应物的浓度或减小生成物的浓度,都可以使化学平衡向正反应方向移动;
t1时刻,增大生成物浓度
v′逆增大,而v′正不变
t1时刻,减小反应物浓度
v′正减小,而v′逆不变
总结:在其他条件不变的情况下,增大生成物的浓度或减小反应物的浓度,都可以使化学平衡向逆反应方向移动
固体或纯液体的浓度是常数,改变固体或纯液体的量并不影响v正、v逆的大小,平衡不移动。
“浓度对化学平衡移动的影响”中的“浓度”是指与反应有关的气体或溶液中参加反应的离子的浓度。
对于离子平衡体系,注意离子浓度的改变方式,排除不参与反应的离子的干扰。
在工业生产中,常通过适当增大廉价的反应物的浓度,使化学平衡向正反应方向移动,可提高价格较高原料的转化率,从而降低生产成本。
NO2浓度比②中的减小
向气体分子数减小方向移动
通过计算Q2 =K/2 ,
即Q2 < K 向正反应方移动
NO2浓度比②中的增大
向气体分子数增大方向移动
通过计算Q2 =2 K, 即Q2 > K 向逆反应方向移动
②减小压强,化学平衡向气体体积增大的方向移动。
压强对化学平衡移动的影响规律
①增大压强,化学平衡向气体体积减小的方向移动。
③对于反应前后气体分子数目不变的反应,改变压强平衡不移动。
用v-t图像分析压强变化对化学平衡移动的影响
平衡向正反应(气体体积减小)方向移动
N2(g)+3H2(g) ⇌2NH3(g)为例
平衡向逆反应(气体体积增大)方向移动
aA(g)+bB(g)
cC(g)+dD(g)
若:a+b = c+d
充入“惰性”气体对化学平衡的影响
恒容时,通入“惰性”气体
恒压时,通入“惰性”气体
平衡向气体体积增大的方向移动
对于反应前后气体体积相等的反应[如H2(g)+I2(g)⇌2HI(g)],当向平衡体系中充入“惰性”气体时,则无论任何情况下平衡都不发生移动。
在恒容容器中,改变其中一种物质的浓度时,必然同时引起压强的改变,但判断平衡移动的方向时,应以浓度的影响进行分析,得出Qc与K的关系。
[C(H2O)6]2++4Cl- [CCl4]2-+6H2O
升高温度,平衡向正反应方向移动(即吸热方向)降低温度,平衡向逆反应方向移动(即放热方向)
②降低温度,平衡向放热反应方向移动。
温度对化学平衡移动的影响规律
①升高温度,平衡向吸热反应方向移动。
任何化学反应都伴随着能量的变化(放热或吸热),所以任意可逆反应的化学平衡状态都受温度的影响。
用v-t图像分析温度变化对化学平衡移动的影响
吸热反应方向的v′逆增大幅度大v′逆>v′正
已知反应:mA(g)+nB(g) pC(g) ΔH<0,当反应达平衡后,若温度改变:
吸热反应方向的v′逆减小幅度大v′正>v′逆
当其他条件不变时,催化剂能够同等程度地改变正逆反应速率,因此它对化学平衡移动无影响,即不能改变平衡混合物的组成,但可缩短达到化学平衡所需的时间。
催化剂能影响化学平衡的移动吗?
向减少反应物浓度的方向
向增大反应物浓度的方向
如果改变影响平衡的一个因素(如温度、压强及参加反应的物质的浓度),平衡就向能够减弱这种改变的方向移动。
(1850—1936)
平衡移动的结果只能是“减弱”外界条件的改变,但不能完全“消除”这种改变。可概括为“外变大于内变”。
所有的动态平衡,用于定性判断平衡移动的方向,解释平衡移动造成的结果或现象等。
如:原平衡(100℃)→升温到200℃→减弱(降温)→向吸热方向移动→新平衡(温度介于100-200℃之间)
如图为合成氨反应在不同温度、压强下平衡时氨的物质的量分数。应用勒夏特列原理解释对于工业合成氨采用相关措施及原因。
促进平衡正向移向,提高H2的转化率
有利于平衡向正反应方向移动
加快反应速率,同时提高催化剂的活性
影响化学平衡移动的因素
1、利用反应:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH=-746.8 kJ·ml-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )A.降低温度B.增大压强同时加催化剂C.升高温度同时充入N2D.及时将CO2和N2从反应体系中移走
2、如图是可逆反应A+2B 2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况。由此可推断下列说法正确的是( )
A.正反应是放热反应B.D可能是气体C.逆反应是放热反应 D.A、B、C、D均为气体
相关课件
这是一份选择性必修1化学平衡的移动完美版课件ppt,文件包含苏教版高中化学选择性必修第一册231《影响化学平衡移动的因素》课件pptx、浓度对平衡的影响mp4等2份课件配套教学资源,其中PPT共44页, 欢迎下载使用。
这是一份高中化学苏教版 (2019)选择性必修1化学平衡的移动评课课件ppt,共28页。PPT课件主要包含了保持不变,某条件下平衡Ⅰ,不平衡,新条件下平衡Ⅱ,改变条件,一定时间,化学平衡移动,实验原理,实验操作,实验现象等内容,欢迎下载使用。
这是一份高中化学苏教版 (2019)选择性必修1第三单元 化学平衡的移动优秀课件ppt,共41页。PPT课件主要包含了课前导入,v正v逆,v正≠v逆,v’正v’逆,v正>v逆,v正<v逆,实验探究一,注意事项,总结·归纳,习题研究等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 






.png)
.png)



