
化学人教版 (2019)金属的腐蚀与防护教案及反思
展开 这是一份化学人教版 (2019)金属的腐蚀与防护教案及反思,共6页。教案主要包含了教材分析,学情分析,教学目标,核心素养目标,教学重难点,教学用具,教学方法,教学过程等内容,欢迎下载使用。
【学情分析】学生在知识储备上,通过必修及前三节的学习已掌握原电池的基本原理及金属的还原性与活泼性的关系;在能力水平上,具备一定的实验设计能力、实验操作能力、比较归纳能力;在心理特点上,他们有强烈的好奇心和求知欲,有利于新知识的学习。而且,本节内容紧密联系实际,学生学习兴趣浓厚,具备了主动探究的原动力。存在的问题是学生对知识的学习只注重表面现象,缺少生活经验,缺乏一定的 综合思维能力。
【教学目标】
了解金属发生腐蚀的原因
了解金属的化学腐蚀与电化学腐蚀的区别与联系
掌握金属发生析氢腐蚀和吸氧腐蚀的电化学原理
【核心素养目标】
1.科学探究与创新意识:通过实验科学探究金属腐蚀的本质及其原因,认识金属腐蚀的主要类型,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式
2.科学态度与社会责任:认识金属腐蚀产生的危害和影响,树立防止金属腐蚀的意识
3.宏观辨识与微观探析:从生活中常见的金属腐蚀现象这一宏观角度对腐蚀的原因进行探析
【教学重难点】
1.重点:金属的电化学腐蚀的原理
2.难点:金属的吸氧腐蚀电化学原理及其对生活中现象的理解和应用
【教学用具】
铁粉、碳粉、稀盐酸、电流表、铁钉、碳棒、U型管、酚酞、铁氰化钾、三颈瓶、溶解氧传感器、压强传感器等
【教学方法】
讲授法、实验法、讨论法
【教学过程】
【板书设计】
4.3 金属的电化学腐蚀与防护
一、金属的电化学腐蚀
1.吸氧腐蚀 2.析氢腐蚀
负极: Fe - 2e- = Fe2+ 负极: Fe - 2e- = Fe2+
正极: O2 + 2H2O + 4e-= 4OH- 正极: 2H+ + 2e- = H2 ↑
电池总反应: 2Fe+O2+2H2O =2Fe(OH)2 电池总反应: Fe + 2H+ = Fe2+ +H2 ↑
4Fe(OH)2 + O2 + 2H2O = 4 Fe(OH)3
Fe(OH)3 Fe2O3·xH2O
金属的防腐
物理
化学:牺牲阳极的阴极保护法
外加电源的阴极保护法
【教学反思】:
1.学生认识方式的转变
学生系统学学习了金属的腐蚀的有化学腐蚀和电化学腐蚀(原电池原理)。金属的防腐有物理的、有化学的(有原电池原理和电解池两种原理的应用)。健全了认知。
2.创设问题情境,在解决问题中学习知识,提升能力
创设真实情境,充分利用素材,组织学生开展分析解释、推论预测、设计评价等学习活动,发展学生“宏观辨识与微观探析”“证据推理和模 型认知”“科学探究与创新意识”和“科学态度与社会责任”的化学学科核心素养。
3提升自我
形成关注学科本质、促进学生认识发展的教学方式
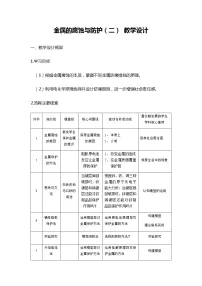
教学环节
教师活动
学生活动
设计意图
创设情境
导入新课
展示金属被腐蚀的图片,介绍金属腐蚀造成的影响,播放金属腐蚀的视频
认真观看,阅读,思考,获得认同感
用生活实例引入,激发学生的探究欲望。
任务一、
了解金属腐蚀的概念,思考金属腐蚀的本质
提供金属腐蚀的概念,给出实例
通过实例思考金属腐蚀的本质
引发学生思考、猜测,
了解金属腐蚀的类型
展示金属腐蚀的类型并讲解二者的区别
学生掌握金属的腐蚀有两种类型
培养学生归纳总结的能力
任务二、
探究钢铁是如何生锈的
提出问题;1、钢铁的成分
2、钢铁生锈所处的环境
学生思考并回答问题
培养用已有知识解决问题的能力,检验学生平时对生活现象的观察能力
提供模拟钢铁腐蚀的实验装置
尝试写出电极反应式。
负极: Fe - 2e- = Fe2+
正极: O2 + 2H2O + 4e-= 4OH-
电池总反应: 2Fe+O2+2H2O =2Fe(OH)2
引导学生构建原电池模型,对原电池的原理加深认识
提问
负极生成Fe2+还是Fe3+如何检验?
正极生成的OH-如何检验?
学习新知
学习Fe2+的检验方法
教师实验
6小时后
一天后
观察、思考
通过小组讨论猜想并设计方案,然后再实验验证。完成科学探究的先猜后证的研究过程
吸氧腐蚀
4Fe(OH)2 + O2 + 2H2O = 4 Fe(OH)3
Fe(OH)3 Fe2O3·xH2O
回忆必修一铁的化合物相关知识
巩固旧知
析氢腐蚀
若水膜的酸性很强,反应是怎样的?
学生尝试写出电极反应式
负极: Fe - 2e- = Fe2+ 正极: 2H+ + 2e- = H2 ↑
电池总反应: Fe + 2H+ = Fe2+ + H2 ↑
培养学生在比较中发现问题
能力提升
提供证据证明
思考、讨论
加深对金属电化学腐蚀的理解
任务三、
根据金属腐蚀的实质,提出金属的防护方法
隔绝氧气、
思考、猜测、
覆盖保护膜
培养思考能力
给予电子
让被保护的金属作原电池的正极或电解池的阴极
新旧知识结合,培养用旧知识解决新问题的能力
实验验证
提供实验器材
学生做实验、观察现象并思考
培养动手能力
归纳总结
展示电化学防护的知识总结
学生记笔记 理解记忆
培养学生归纳总结的能力
课堂检测
提出问题:如何防止铁锅生锈
学生积极思考,
培养发散思维
小结
金属的腐蚀以及防护
理清知识逻辑
培养逻辑思维
相关教案
这是一份化学人教版 (2019)金属的腐蚀与防护教案及反思,共6页。教案主要包含了教材分析,学情分析,教学目标,核心素养目标,教学重难点,教学用具,教学方法,教学过程等内容,欢迎下载使用。
这是一份化学选择性必修1第三节 金属的腐蚀与防护教案,共6页。教案主要包含了教学设计框架,教学设计等内容,欢迎下载使用。
这是一份高中化学第三节 金属的腐蚀与防护教案,共3页。
相关教案 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 


.png)




