






第六章 化学反应与能量 第1讲 化学反应的热效应 第二课时 课件-2026年高考化学一轮复习 课件(全国通用)
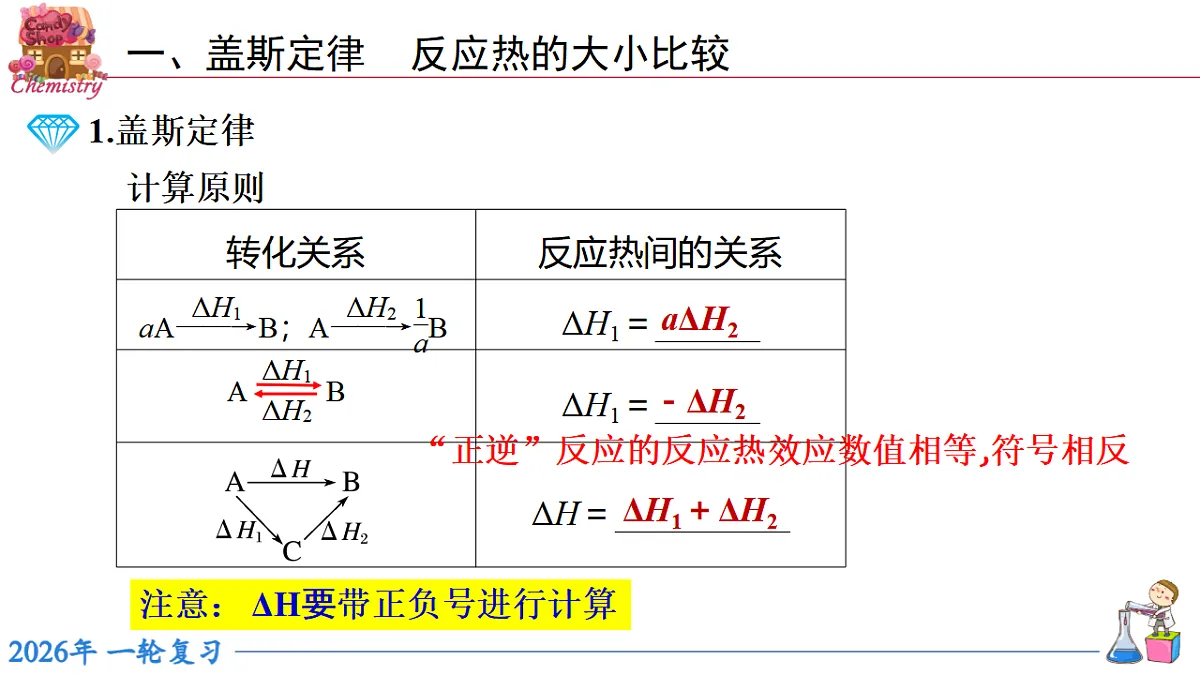
展开目录CONTENTS01盖斯定律一、盖斯定律 反应热的大小比较 一个化学反应,不管是一步完成的还是几步完成的,其反应热是相同的。 盖斯定律表明,在一定条件下化学反应的反应热只与反应体系的始态(各反应物)和终态(各生成物)有关,而与具体反应进行的途径无关。 盖斯定律的应用:有些反应进行得很慢;有些反应不容易直接发生;有些反应的产品不纯(有副反应发生)。这些都给测量反应热造成了困难,利用盖斯定律可以间接地把它们的反应热计算出来aΔH2-ΔH2ΔH1+ΔH2注意: ΔH要带正负号进行计算“正逆”反应的反应热效应数值相等,符号相反计算原则一、盖斯定律 反应热的大小比较解题步骤与技巧①确定待求的反应方程式;②找出待求方程式中各物质出现在已知方程式的什么位置;③根据待求方程式中各物质计量数和位置的需要,对已知方程式进行处理,或调整计量数,或调整反应方向;④实施叠加并检验上述分析的正确与否。关 键:通过加、减、乘、除“四则运算式”导出目标方程式ΔH一、盖斯定律 反应热的大小比较1.(2023·浙江6月选考节选)水煤气变换反应是工业上的重要反应,可用于制氢。水煤气变换反应:CO(g)+H2O(g)⥫⥬CO2(g)+H2(g) ΔH=-41.2 kJ· mol-1该反应分两步完成:3Fe2O3(s)+CO(g)⥫⥬2Fe3O4(s)+CO2(g) ΔH1=-47.2 kJ·mol-12Fe3O4(s)+H2O(g)⥫⥬3Fe2O3(s)+H2(g) ΔH2 ΔH2=____ kJ·mol-1。+6 2V2O5(s)+2SO2(g)===2VOSO4(s)+V2O4(s) ΔH=-351 kJ·mol-102反应热的大小比较二、反应热的大小比较 同种物质:E(g)>E(l)>E(s) g→l ΔH
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




