
湖北省孝感市新高考协作体2025-2026学年高二上学期11月期中考试化学试卷(学生版)
展开 这是一份湖北省孝感市新高考协作体2025-2026学年高二上学期11月期中考试化学试卷(学生版),共9页。试卷主要包含了选择题的作答,非选择题的作答,5 Cu 64,6 kJ·ml-1, 已知①等内容,欢迎下载使用。
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证号条形码粘贴在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。写在试卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷、草稿纸和答题卡上的非答题区域均无效。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Cu 64
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 下列措施能降低反应物的活化能的是
A. 降低温度B. 加入催化剂C. 扩大容器体积D. 增大反应物浓度
2. 实验室配制溶液时,需区分电解质的强弱以控制溶解和电离效果。下列物质属于强电解质的是
A. CH3COOHB. NH3·H2OC. H2OD. NaClO
3. 热化学方程式是工业生产中计算反应热、优化工艺的重要依据。下列热化学方程式书写正确的是
A. 工业制硫酸中SO2的催化氧化:2SO2+O22SO3 ΔH=-196.6 kJ·ml-1
B. 氢气的燃烧热(25℃、101 kPa): ΔH=-285.8 kJ·ml-1
C. 焦炭燃烧生成CO2:C(s)+O2(g)=CO2(g) ΔH=+393.5 kJ·ml-1
D. 电解水制氢气:2H2(g)+O2(g)=2H2O(g) ΔH=-571.6 kJ
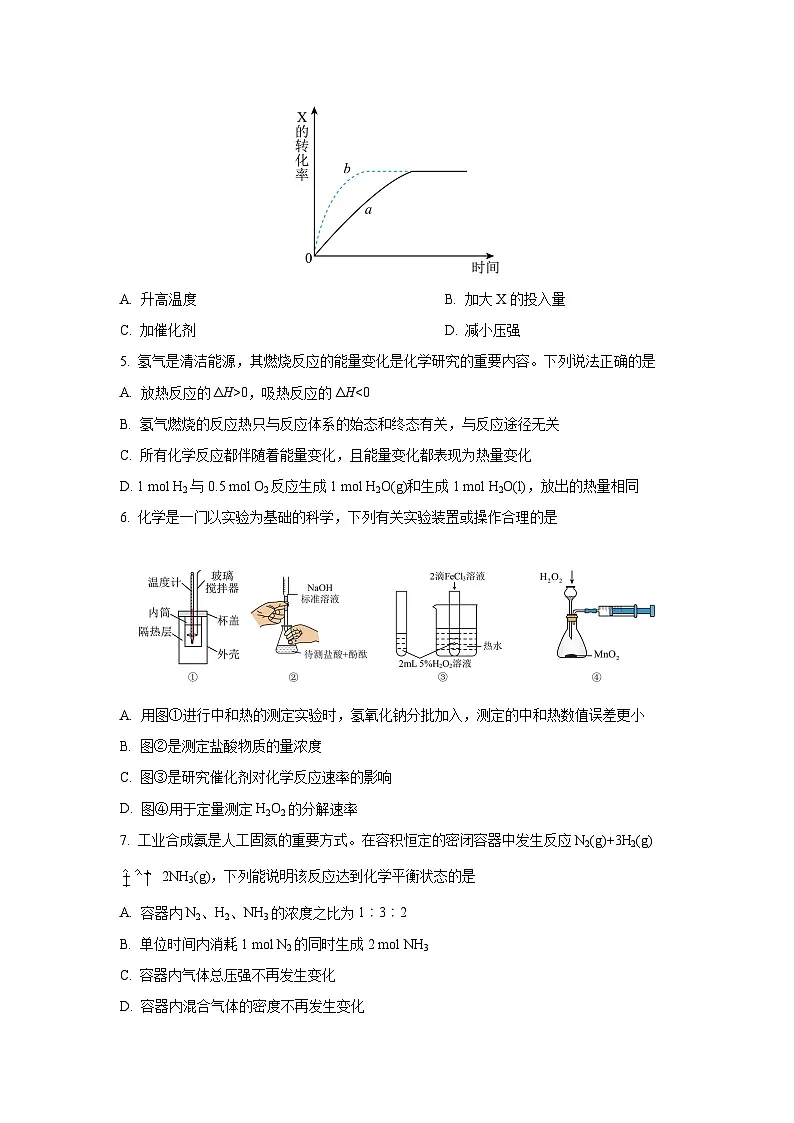
4. 如图所示曲线a表示放热反应X(g)+Y(g)Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
A. 升高温度B. 加大X的投入量
C. 加催化剂D. 减小压强
5. 氢气是清洁能源,其燃烧反应的能量变化是化学研究的重要内容。下列说法正确的是
A. 放热反应的ΔH>0,吸热反应的ΔH0。该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是
A. AB. BC. CD. D
二、非选择题:本题共4小题,共55分。
16. 化学反应过程中,不仅有物质的变化,同时伴随有能量的变化。化学反应的反应热是研究的重点内容之一,回答下列问题:
(i)黄铁矿(主要成分为FeS2)的燃烧是工业上制硫酸时得到SO2的途径之一,研究其热效应有利于工业生产。在25℃、101 kPa下,FeS2燃烧的热化学方程式为4FeS2(s)+11O2(g)=2Fe2O3(s)+8SO2(g) ΔH=-3412 kJ·ml-1。
(1)该反应属于______(填“放热”或“吸热”)反应,据此可推理,反应物总能量比生成物总能量______(填“高”或“低”)。
(2)FeS2的燃烧热ΔH=______kJ·ml-1。
(3)下列过程中的ΔH>0的是______(填标号)。
A. 镁条与盐酸反应B. 灼热的木炭与二氧化碳反应
C. 将浓硫酸缓慢注入蒸馏水中D. Ba(OH)2·8H2O与NH4Cl晶体混合
(ii)测定化学反应的热效应是研究反应热的路径之一。在25℃、101 kPa下,某实验兴趣小组利用如图所示装置进行中和反应反应热的测定。
(4)仪器a名称为______。
(5)该装置有一处明显的错误,该错误为______。
(6)已知:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH=-67.7 kJ·ml-1
②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·ml-1
则HF电离的热化学方程式为______。
17. 化学反应的快慢是研究化学反应原理的重要内容之一。某兴趣小组为研究影响化学反应速率的因素,设计了50 mL不同浓度的盐酸和1 g不同状态的碳酸钙反应,实验数据如下表所示。
回答下列问题:
(1)该反应的离子方程式为______。体系与环境是研究化学反应热的两个不同对象,上述反应中“体系”是指______(填标号)。
A.盐酸、碳酸钙及发生的反应
B.盐酸、碳酸钙、烧杯及发生的反应
C.盛溶液的烧杯和溶液之外的空气
(2)控制变量是研究化学反应规律的重要方法。实验1和实验2控制的变量为______。由实验6和实验7得出的结论为______,反应速率越快;能证明同一规律的实验还有______(填实验序号)。
(3)根据表格数据,实验3和4、6和8是研究______(填影响因素)对反应速率的影响。
(4)为减慢实验5的反应速率且不影响产生气体的物质的量(忽略CO2溶于水),可向盐酸溶液中______(填标号)。
A.滴加少量NaCl溶液
B.滴加几滴浓盐酸
C.加入少量CH3COONa固体
18. 已知:25℃时,0.1 ml·L-1的HA溶液中,0.01 ml·L-1 BOH溶液pH=12。回答下列问题:
(1)HA是______(填“强酸”或“弱酸”),BOH的电离方程式为______。
(2)25℃时,0.1 ml·L-1 HA溶液中由水电离出的c(OH-)=______ml·L-1。
(3)在加水稀释0.1 ml·L-1的HA的过程中,随着水量的增加而减小的是______(填标号)。
A. B. C. c(H+)与c(OH-)的乘积D. c(OH-)
(4)常温下,部分物质的电离平衡常数如表所示:
回答下列问题:
①常温下,CH3COOH、H2CO3、HClO的酸性由弱到强的顺序为______。
②向NaClO溶液中通入少量CO2发生反应的化学方程式为______。
③常温下,将氯气通入水中发生反应Cl2+H2OHCl+HClO。为提高c(HClO)可向新制氯水中加入______(填化学式,至少写出两种)固体。
19. 二氧化碳是当今最主要温室气体,将其进行资源化利用是实现“碳中和”的途径之一。回答下列问题:
I.利用CO2制备CO
一定温度下,恒容密闭容器中进行反应CO2(g)+H2(g)CO(g)+H2O(l) ΔH>0
(1)该反应______(填“能”或“否”)自发进行,理由是该反应的ΔG______(填“>”“
相关试卷
这是一份湖北省孝感市新高考协作体2025-2026学年高二上学期11月期中考试化学试卷(学生版),共9页。试卷主要包含了选择题的作答,非选择题的作答,5 Cu 64,6 kJ·ml-1, 已知①等内容,欢迎下载使用。
这是一份湖北省孝感新高考协作体2025-2026学年高二上学期11月期中考试化学试卷,共8页。
这是一份湖北省孝感市新高考协作体2025-2026学年高二上学期11月期中化学试题(含答案),共10页。试卷主要包含了5 Cu 64,6kJ•ml-1,如下图所示曲线a表示放热反应X,工业合成氨是人工固氮的重要方式等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 









