



所属成套资源:备战2026年高考化学真题汇编专题(Word版附解析)
备战2026年高考化学精品试题汇编专题28化学反应原理综合题——能量主线型(Word版附解析)
展开 这是一份备战2026年高考化学精品试题汇编专题28化学反应原理综合题——能量主线型(Word版附解析),文件包含备战2026年高考精品试题汇编化学专题28化学反应原理综合题能量主线型原卷版docx、备战2026年高考精品试题汇编化学专题28化学反应原理综合题能量主线型Word版含解析docx等2份试卷配套教学资源,其中试卷共69页, 欢迎下载使用。
1.(2025·湖北卷)粉末可在较低温度下还原。回答下列问题:
(1)已知一定温度下:
则的 (用m和n表示)。
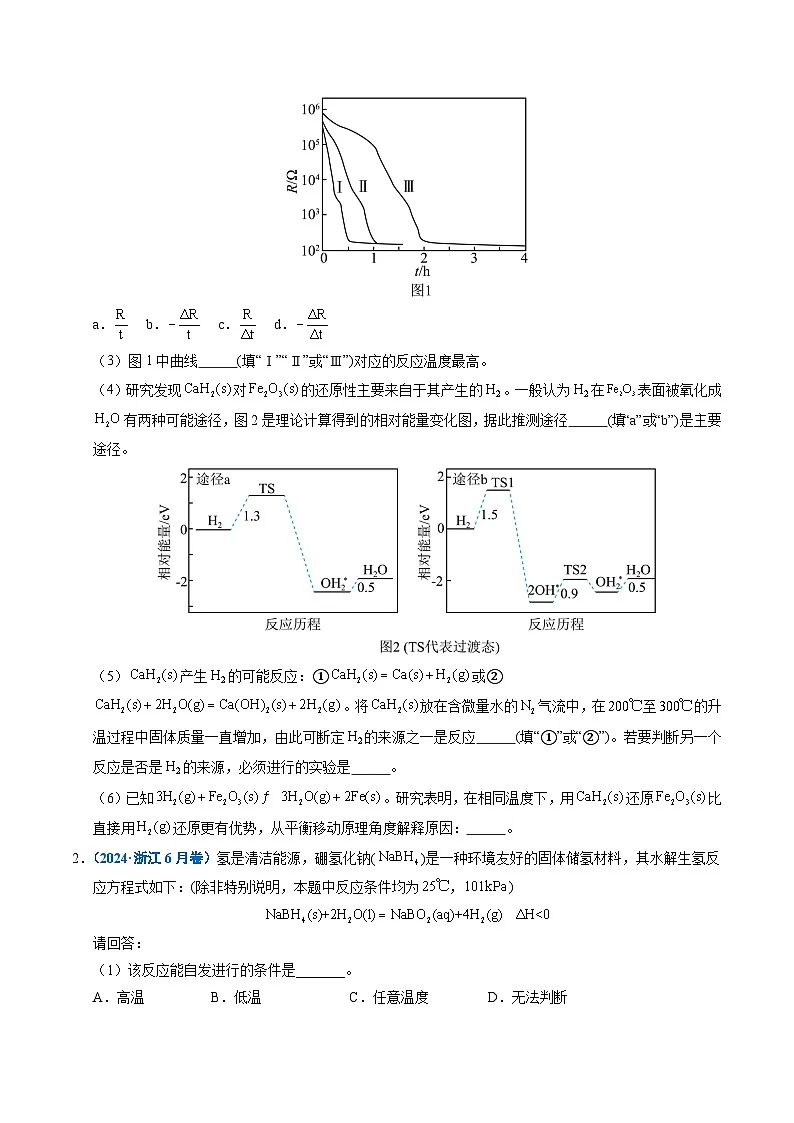
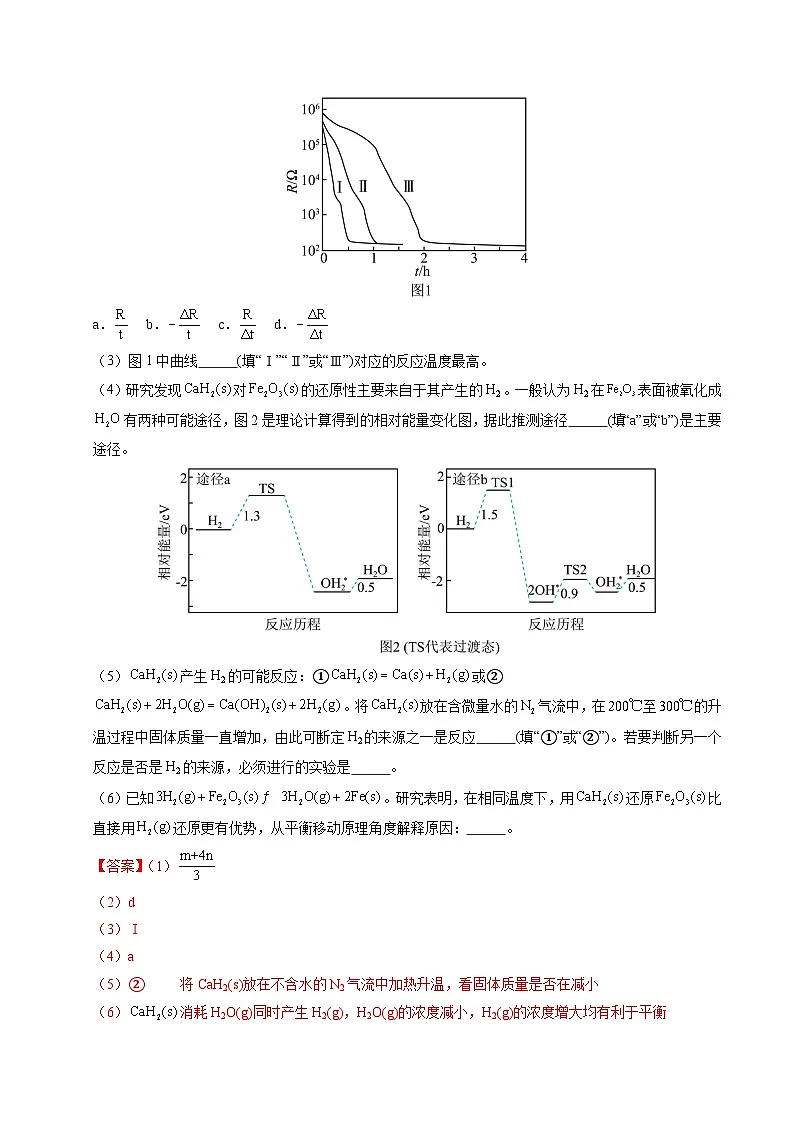
(2)图1分别是和下还原过程中反应体系电阻随反应时间变化的曲线,可用 (填标号)表示反应的快慢。
a. b. c. d.
(3)图1中曲线 (填“Ⅰ”“Ⅱ”或“Ⅲ”)对应的反应温度最高。
(4)研究发现对的还原性主要来自于其产生的。一般认为在表面被氧化成有两种可能途径,图2是理论计算得到的相对能量变化图,据此推测途径 (填“a”或“b”)是主要途径。
(5)产生的可能反应:①或②。将放在含微量水的气流中,在至的升温过程中固体质量一直增加,由此可断定的来源之一是反应 (填“①”或“②”)。若要判断另一个反应是否是的来源,必须进行的实验是 。
(6)已知。研究表明,在相同温度下,用还原比直接用还原更有优势,从平衡移动原理角度解释原因: 。
【答案】(1)
(2)d
(3)Ⅰ
(4)a
(5)② 将CaH2(s)放在不含水的N2气流中加热升温,看固体质量是否在减小
(6)消耗H2O(g)同时产生H2(g),H2O(g)的浓度减小,H2(g)的浓度增大均有利于平衡正向移动,提高Fe的产率
【解析】(1)①
②
③
×①+×②得到反应③,根据盖斯定律可知=×+×=;
(2)随着铁的生成,电阻变小,可用单位时间内电阻的变化量来表示反应速率,即,选d;
(3)其它条件相同,温度越高,反应速率越快,曲线Ⅰ电阻变化最快,故曲线Ⅰ对应的反应温度最高;
(4)由图可知途径a中能垒为1.3eV,比途径b中小,故途径a反应速率更快,途径a是主要途径;
(5)固体质量一直增加,则氢气的来源之一是反应②;若要判断另一个反应是否是H2的来源,必须进行的实验是:将CaH2(s)放在不含水的N2气流中加热升温,看固体质量是否在减小;
(6)在相同温度下,用还原比直接用还原更有优势,从平衡移动原理角度解释原因:消耗H2O(g)同时产生H2(g),H2O(g)的浓度减小,H2(g)的浓度增大均有利于平衡正向移动,提高Fe的产率。
2.(2024·浙江6月卷)氢是清洁能源,硼氢化钠()是一种环境友好的固体储氢材料,其水解生氢反应方程式如下:(除非特别说明,本题中反应条件均为,)
请回答:
(1)该反应能自发进行的条件是_______。
A.高温B.低温C.任意温度D.无法判断
(2)该反应比较缓慢。忽略体积变化的影响,下列措施中可加快反应速率的是_______。
A.升高溶液温度B.加入少量异丙胺
C.加入少量固体硼酸D.增大体系压强
(3)为加速水解,某研究小组开发了一种水溶性催化剂,当该催化剂足量、浓度一定且活性不变时,测得反应开始时生氢速率v与投料比之间的关系,结果如图1所示。请解释ab段变化的原因 。
(4)氢能的高效利用途径之一是在燃料电池中产生电能。某研究小组的自制熔融碳酸盐燃料电池工作原理如图2所示,正极上的电极反应式是 。该电池以恒定电流工作14分钟,消耗体积为,故可测得该电池将化学能转化为电能的转化率为 。[已知:该条件下的摩尔体积为;电荷量电流时间;;。]
(5)资源的再利用和再循环有利于人类的可持续发展。选用如下方程式,可以设计能自发进行的多种制备方法,将反应副产物偏硼酸钠()再生为。(已知:是反应的自由能变化量,其计算方法也遵循盖斯定律,可类比计算方法;当时,反应能自发进行。)
I.
II.
III.
请书写一个方程式表示再生为的一种制备方法,并注明 。(要求:反应物不超过三种物质;氢原子利用率为。)
【答案】(1)C
(2)A
(3)随着投料比增大,NaBH4的水解转化率降低
(4)O2+4e-+2CO2=2 70%
(5)
【解析】(1)反应, ,由可知,任意温度下,该反应均能自发进行,故答案选C;
(2)A.升高温度,活化分子数增多,有效碰撞几率增大,反应速率加快,A符合题意;
B.加入少量异丙胺,H2O的量减少,化学反应速率降低,B不符合题意;
C. 加入少量固体硼酸,H2O的量减少,化学反应速率降低,C不符合题意;
D.增大体系压强,忽略体积变化,则气体浓度不变,化学反应速率不变,D不符合题意;
答案选A。
(3)随着投料比增大,NaBH4的水解转化率降低,因此生成氢气的速率不断减小。
(4)根据题干信息,该燃料电池中H2为负极,O2为正极,熔融碳酸盐为电解质溶液,故正极的电极反应式为:O2+4e-+2CO2=2, 该条件下,0.49L H2的物质的量为,工作时,H2失去电子:H2-2e-=2H+,所带电荷量为:2×0.02ml×6.0×1023ml-1×1.60×10-19= 3840C,工作电荷量为:3.2×14×60=2688C,则该电池将化学能转化为电能的转化率为:;
(5)结合题干信息,要使得氢原子利用率为100%,可由(2×反应3)-(2×反应Ⅱ+反应Ⅰ)得, 。
3.(2024·甘肃卷)是制备半导体材料硅的重要原料,可由不同途径制备。
(1)由制备:
已知
时,由制备硅 (填“吸”或“放”)热 。升高温度有利于制备硅的原因是 。
(2)在催化剂作用下由粗硅制备:。,密闭容器中,经不同方式处理的粗硅和催化剂混合物与和气体反应,转化率随时间的变化如下图所示:
①,经方式 处理后的反应速率最快;在此期间,经方式丙处理后的平均反应速率 。
②当反应达平衡时,的浓度为 ,平衡常数K的计算式为 。
③增大容器体积,反应平衡向 移动。
【答案】(1)吸 587.02 该反应为吸热反应,升高温度,反应正向移动,有利于制备硅
(2)甲 0.1952 逆反应方向
【解析】(1)由题给热化学方程式:①,;②,;则根据盖斯定律可知,①+②,可得热化学方程式,,则制备56gSi,即2mlSi,需要吸收热量为;该反应为吸热反应,升高温度,反应正向移动,有利于制备硅。
(2)①由转化率图像可知,0-50min,经方式甲处理后反应速率最快;经方式丙处理后,50min时SiCl4的转化率为4.2%,反应的SiCl4的物质的量为0.1ml×4.2%=0.0042ml,根据化学化学计量数可得反应生成的SiHCl3的物质的量为,平均反应速率;
②反应达到平衡时,SiCl4的转化率为14.6%,列出三段式为:
当反应达平衡时,H2的浓度为,平衡常数K的计算式为;
③增大容器体积,压强减小,平衡向气体体积增大的方向移动,即反应平衡向逆反应方向移动。
4.(2024·湖南卷)丙烯腈()是一种重要的化工原料。工业上以为载气,用作催化剂生产的流程如下:
已知:①进料混合气进入两釜的流量恒定,两釜中反应温度恒定:
②反应釜Ⅰ中发生的反应:
ⅰ:
③反应釜Ⅱ中发生的反应:
ⅱ:
ⅲ:
④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应 (用含、、和的代数式表示);
(2)进料混合气中,出料中四种物质(、、、)的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:
①表示的曲线是 (填“a”“b”或“c”);
②反应釜Ⅰ中加入的作用是 。
③出料中没有检测到的原因是 。
④反应后,a、b、c曲线对应物质的流量逐渐降低的原因是 。
(3)催化剂再生时会释放,可用氨水吸收获得。现将一定量的固体(含水)置于密闭真空容器中,充入和,其中的分压为,在℃下进行干燥。为保证不分解,的分压应不低于 (已知 分解的平衡常数);
(4)以为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得,其阴极反应式 。
【答案】(1)ΔH1+ΔH2+ΔH3
(2)c 降低分压有利于反应i平衡正向移动且提高醇的浓度可以使酯的水解程度降低从而提高产率 CH2=CHCONH2在反应釜Ⅱ的温度下发生分解 反应时间过长,催化剂中毒活性降低,反应速率降低,故产物减少
(3)40
(4)Sn+4CH2=CHCN+4e-+4H+=Sn(CH2CH2CN)4
【分析】工业上以N2为载气,用TiO2作催化剂,由HOCH2CH2COOC2H5和C2H5OH为进料气体生产CH2=CHCN,在反应釜I中发生反应i:HOCH2CH2COOC2H5(g)→CH2=CHCOOC2H5(g)+H2O(g),加入NH3后,在反应釜Ⅱ中发生反应ii:CH2=CHCOOC2H5(g)+NH3(g)→CH2=CHCONH2(g)+C2H5OH(g),反应iii:CH2=CHCONH2(g)→CH2=CHCN(g)+H2O(g),故产物的混合气体中有CH2=CHCN、未反应完的C2H5OH、CH2=CHCOOC2H5(g)和水;
【解析】(1)根据盖斯定律,总反应HOCH2CH2COOC2H5(g)+NH3(g)→CH2=CHCN(g)+C2H5OH(g)+2H2O(g)可以由反应i+反应ii+反应iii得到,故ΔH=ΔH1+ΔH2+ΔH3;
(2)①根据总反应HOCH2CH2COOC2H5(g)+NH3(g)→CH2=CHCN(g)+C2H5OH(g)+2H2O(g),设进料混合气中n(HOCH2CH2COOC2H5)=1ml,n(C2H5OH)=2ml,出料气中CH2=CHCOOC2H5含量很少,则生成CH2=CHCN(g)、C2H5OH(g)物质的量约为1ml,生成H2O(g)的物质的量约为2ml,故出料气中C2H5OH(g)物质的量共约3ml,故出料气中CH2=CHCN、C2H5OH、H2O物质的量之比约为1:3:2,故曲线c表示CH2=CHCN的曲线;
②反应釜Ⅰ中发生反应i是气体体积增大的反应,故加入C2H5OH降低分压有利于反应i平衡正向移动且提高醇的浓度可以使酯的水解程度降低从而提高产率;
③丙烯酰胺(CH2=CHCONH2)的分解温度约为160°C至170°C,出料中没有检测到CH2=CHCONH2的原因是CH2=CHCONH2在反应釜Ⅱ的温度下发生分解;
④反应11h后,a、b、c曲线对应物质的流量逐渐降低的原因是反应时间过长,催化剂中毒活性降低,反应速率降低,故产物减少;
(3)0.72g水的物质的量为0.04ml,故p(H2O)=2.5×102kPa⋅ml−1×n(H2O)=10kPa,NH4HCO3分解的反应式为NH4HCO3=NH3↑+CO2↑+H2O↑,故NH4HCO3分解的平衡常数Kp=p(NH3)p(CO2)p(H2O)=4×104(kPa)3,解得p(NH3)=40kPa,故为保证NH4HCO3不分解,NH3的分压应不低于40kPa;
(4)Sn(CH2CH2CN)4是有机化合物,与水不溶,水中不电离,以CH2=CHCN为原料在Sn做的阴极得电子制得Sn(CH2CH2CN)4,故阴极的电极反应式为Sn+4CH2=CHCN+4e-+4H+=Sn(CH2CH2CN)4。
5.(2024·江苏卷)氢能是理想清洁能源,氢能产业链由制氢、储氢和用氢组成。
(1)利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有 ;含CO和各1ml的混合气体通过该方法制氢,理论上可获得 。
(2)一定条件下,将氮气和氢气按混合匀速通入合成塔,发生反应。海绵状的作催化剂,多孔作为的“骨架”和气体吸附剂。
①中含有CO会使催化剂中毒。和氨水的混合溶液能吸收CO生成溶液,该反应的化学方程式为 。
②含量与表面积、出口处氨含量关系如图所示。含量大于,出口处氨含量下降的原因是 。
(3)反应可用于储氢。
①密闭容器中,其他条件不变,向含有催化剂的溶液中通入,产率随温度变化如图所示。温度高于,产率下降的可能原因是 。
②使用含氨基物质(化学式为,CN是一种碳衍生材料)联合催化剂储氢,可能机理如图所示。氨基能将控制在催化剂表面,其原理是 ;用重氢气(D2)代替H2,通过检测是否存在 (填化学式)确认反应过程中的加氢方式。
【答案】(1)C、H、Fe
(2) 多孔 Al2O3可作为气体吸附剂,含量过多会吸附生成的NH3,Al2O3含量大于2%时,α-Fe表面积减小,反应速率减小,产生NH3减少。
(3)NaHCO3受热分解,导致HCOO-产率下降 -NH2可以与形成氢键 HDO
【解析】(1)①反应器I中参与反应的物质有CO、H2、Fe2O3,产物有 CO2、H2O、Fe,发生反应、化合价发生改变的元素有 C、H、Fe。
②CO、H2各1 ml参与上述反应,各生成ml Fe,共生成mlFe,mlFe在反应器Ⅱ中发生反应,列比例计算,共生成ml H₂。
(2)①根据题给反应物及生成物书写即可。②多孔 Al2O3可作为气体吸附剂,含量过多会吸附生成的NH3,Al2O3含量大于2%时,α-Fe表面积减小,反应速率减小,这也会导致产生的NH3减少。
(3)①NaHCO3受热易分解,导致HCOO-产率下降。②氨基中的H原子连在电负性较大的N原子上,中的H原子连在电负性较大的O原子上,二者之间可以形成氢键③总反应为,用D2代替H2,若生成 HDO,则可确认反应过程中的加氢方式。
6.(2023·全国甲卷)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
反应③的_______,平衡常数_______(用表示)。
(2)电喷雾电离等方法得到的(等)与反应可得。与反应能高选择性地生成甲醇。分别在和下(其他反应条件相同)进行反应,结果如下图所示。图中的曲线是_______(填“a”或“b”。、时的转化率为_______(列出算式)。
(3)分别与反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以示例)。
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是_______(填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则与反应的能量变化应为图中曲线_______(填“c”或“d”)。
(ⅲ)与反应,氘代甲醇的产量_______(填“>”“<”或“=”)。若与反应,生成的氘代甲醇有_______种。
【答案】(1) 或
(2) b
(3)Ⅰ c < 2
【解析】(1)根据盖斯定律可知,反应③=(反应②-①),所以对应;根据平衡常数表达式与热化学方程式之间的关系可知,对应化学平衡常数或,故答案为:;或;
(2)根据图示信息可知,纵坐标表示-lg(),即与MO+的微粒分布系数成反比,与M+的微粒分布系数成正比。则同一时间内,b曲线生成M+的物质的量浓度比a曲线的小,证明化学反应速率慢,又因同一条件下降低温度化学反应速率减慢,所以曲线b表示的是300 K条件下的反应;
根据上述分析结合图像可知,、时-lg()=0.1,则=10-0.1,利用数学关系式可求出,根据反应可知,生成的M+即为转化的,则的转化率为;故答案为:b;;
(3)(ⅰ)步骤Ⅰ涉及的是碳氢键的断裂和氢氧键的形成,步骤Ⅱ中涉及碳氧键形成,所以符合题意的是步骤Ⅰ;
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则此时正反应活化能会增大,根据图示可知,与反应的能量变化应为图中曲线c;
(ⅲ)与反应时,因直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则单位时间内产量会下降,则氘代甲醇的产量<;根据反应机理可知,若与反应,生成的氘代甲醇可能为或共2种,故答案为:<;2。
7.(2023·海南卷)磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与反应制备,反应方程式为一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为 。
(2)该制备反应的随温度变化关系如图2所示。该条件下反应为 反应(填“吸热”或“放热”),且反应热随温度升高而 。
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸 ;通入水蒸气 。
(4)298K时,的平衡常数 。(已知的)
【答案】(1)70%
(2)吸热 降低
(3)使用浓磷酸作反应物可以提高磷酸的浓度,促使反应正向进行 使得气体中氯化氢的分压减小,促使反应正向进行
(4)
【解析】(1)由图可知,该条件下,反应至1h时KCl的转化率为70%;
(2)由图可知,焓变为正值,则该条件下反应为吸热反应,且反应热随温度升高而降低;
(3)使用浓磷酸作反应物可以提高磷酸的浓度,促使反应正向进行;向系统中不断通入水蒸气,使得气体中氯化氢的分压减小,促使反应正向进行;都可以促进氯化钾的转化率的提高;
(4)298K时,的离子方程式为,其平衡常数。
8.(2023·江苏卷)空气中含量的控制和资源利用具有重要意义。
(1)燃煤烟气中的捕集可通过如下所示的物质转化实现。
“吸收”后所得的溶液与石灰乳反应的化学方程式为 ;载人航天器内,常用LiOH固体而很少用KOH固体吸收空气中的,其原因是 。
(2)合成尿素[]是利用的途径之一。尿素合成主要通过下列反应实现
反应Ⅰ:
反应Ⅱ:
①密闭体系中反应Ⅰ的平衡常数(K)与温度的关系如图甲所示,反应Ⅰ的 (填“=0”或“>0”或“
相关试卷
这是一份备战2026年高考化学精品试题汇编专题28化学反应原理综合题——能量主线型(Word版附解析),文件包含备战2026年高考精品试题汇编化学专题28化学反应原理综合题能量主线型原卷版docx、备战2026年高考精品试题汇编化学专题28化学反应原理综合题能量主线型Word版含解析docx等2份试卷配套教学资源,其中试卷共69页, 欢迎下载使用。
这是一份2026届高三化学二轮专题练习专题28化学反应原理综合题——能量主线型(Word版含解析),文件包含专题28化学反应原理综合题能量主线型原卷版docx、专题28化学反应原理综合题能量主线型Word版含解析docx等2份试卷配套教学资源,其中试卷共69页, 欢迎下载使用。
这是一份2021-2025年高考化学真题分类精编专题28化学反应原理综合题——能量主线型(Word版附解析),文件包含专题28化学反应原理综合题能量主线型原卷版docx、专题28化学反应原理综合题能量主线型Word版含解析docx等2份试卷配套教学资源,其中试卷共69页, 欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




