





2026年高考化学总复习备课课件 高考热点2 越考越热的阿伏加德罗常数(NA)
展开 这是一份2026年高考化学总复习备课课件 高考热点2 越考越热的阿伏加德罗常数(NA),共28页。
一、22.4 L·ml-1的适用对象与条件1.若题中出现物质的体积,先看该物质是否是气体,如果是气体再看是否为标准状况(0 ℃、1.01×105 Pa)。2.标准状况下不是气体的物质,常考的有:H2O、液溴、HF、CHCl3、CH2Cl2、CCl4、SO3、NO2、酒精、乙酸、碳原子数大于4的烃(除新戊烷)、苯等。
【例1】 下列说法正确的是 。 (1)25 ℃、101 kPa下,28 L氢气中质子的数目为2.5NA。(2)11.2 L乙烷和丙烯的混合气体中所含碳氢键数为3NA。(3)标准状况下,22.4 L HCl气体中H+数目为NA。(4)22.4 L(标准状况)氟气所含的质子数为18NA。(5)11.2 L NO与11.2 L O2混合后的分子数目为NA。(6)标准状况下,1.12 L 18O2中含有中子数为NA。
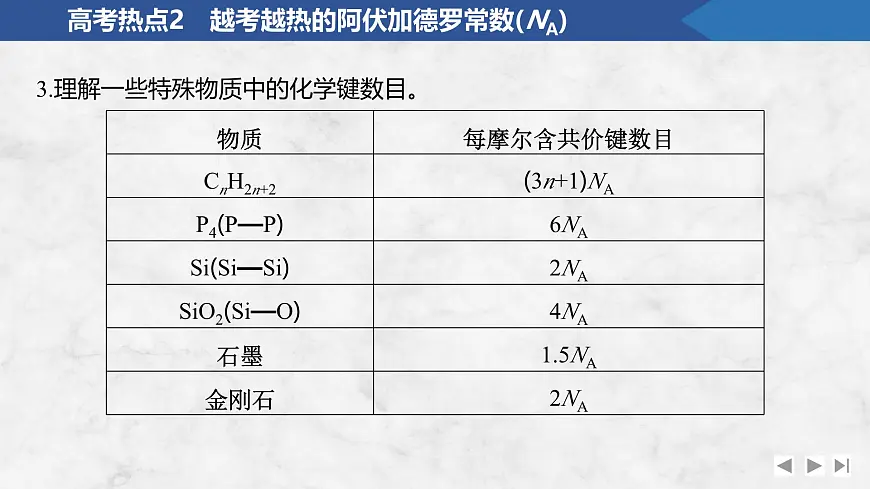
3.理解一些特殊物质中的化学键数目。
【例2】 下列说法错误的是 。 (1)2.8 g C2H4分子中含有的σ键数目为4NA。(2)1.8 g重水(D2O)中所含质子数为NA。(3)32 g甲醇的分子中含有C—H键的数目为4NA。(4)0.20 ml苯甲酸完全燃烧,生成CO2的数目为1.4NA。(5)23 g Na与足量H2O反应生成的H2分子数目为NA。(6)3.9 g Na2O2中含有的共价键的数目为0.1NA。(7)0.1 ml肼(H2N—NH2)含有的孤电子对数为0.2NA。
(1)(2)(3)(5)(6)
三、特殊氧化还原反应中的电子转移数目1.判断电子转移总数做到“三注意”
(1)注意是否发生歧化反应,如Na2O2与H2O、CO2的反应;Cl2、NO2与H2O或NaOH的反应。(2)注意变价元素,如Fe与足量硝酸反应生成Fe3+,与少量硝酸反应生成Fe2+。(3)注意氧化还原反应的竞争及用量问题,如向FeBr2溶液中通入Cl2,Cl2的量不同,转移的电子数不同。
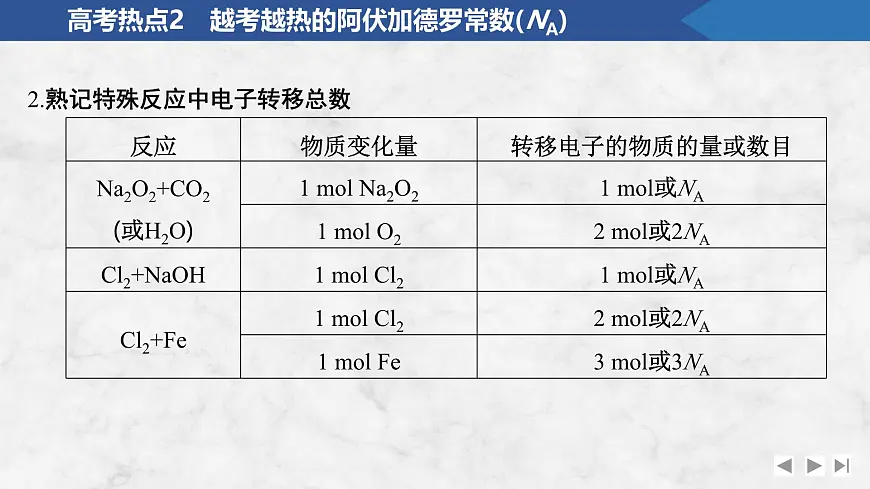
2.熟记特殊反应中电子转移总数
【例3】 下列说法错误的是 。 (1)足量的浓盐酸与8.7 g MnO2反应,转移电子的数目为0.4NA。(2)电解熔融CuCl2,阴极增重6.4 g,外电路中通过电子的数目为0.10NA。(3)3 ml NO2与水完全反应时转移的电子数为4NA。(4)用惰性电极电解饱和食盐水时,若阴、阳两极产生气体的总质量为73 g,则转移电子数为NA。(5)1 ml SO2与1 ml O2完全反应转移的电子数为4NA。(6)用惰性电极电解熔融MgCl2制2.4 g Mg,电路中通过的电子数为0.1NA。
(1)(2)(3)(4)(5)(6)
四、电解质溶液中的粒子数目
抓住电解质强弱,理清粒子的存在形式和数目
五、化学反应中的隐含反应和信息1.隐含的可逆反应
2.注意盐溶液中是否涉及弱碱阳离子、弱酸酸根阴离子。
3.有些反应的反应物浓度不一样,反应就不一样。(1)MnO2与浓盐酸的反应,随着反应的进行,浓盐酸变为稀盐酸,反应停止。(2)Cu与浓硫酸的反应,随着反应的进行,浓硫酸变为稀硫酸,反应停止。(3)Cu与浓硝酸反应,随着反应的进行,浓硝酸变为稀硝酸,得到NO2和NO的混合气体。(4)Zn与浓硫酸反应,随着反应的进行,浓硫酸变为稀硫酸,得到SO2和H2的混合气体。
【例5】 下列说法错误的是 。 (1)0.1 ml H2和0.1 ml I2于密闭容器中充分反应,HI分子总数为0.2NA。(2)2 ml NO与1 ml O2在密闭容器中充分反应后的分子数为2NA。(3)0.1 ml CH4与足量Cl2反应生成CH3Cl的分子数为0.1NA。(4)常温下,56 g铁片投入足量浓硫酸中生成NA个SO2分子。(5)标准状况下,将22.4 L Cl2通入足量水中充分反应,转移电子数为NA。(6)常温下,将64 g Cu投入一定量的浓硝酸(含4 ml HNO3)中,生成NO2的分子数为2NA。
2.设NA为阿伏加德罗常数的值。下列说法错误的是( )
3.NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.2 g H2分别与足量的Cl2和N2充分反应后转移的电子数均为2NAB.一定条件下,2.3 g Na与O2完全反应生成3.6 g产物时失去的电子数为0.1NAC.用浓盐酸分别和KMnO4、KClO3反应制备1 ml氯气,转移的电子数均为2NAD.2H2S+SO2===3S↓+2H2O反应中,每生成1 ml氧化产物时转移电子数为NA
4.NA表示阿伏加德罗常数的值。下列说法不正确的是( )
A.0.1 ml Fe和0.1 ml Cu分别与0.1 ml Cl2完全反应,转移电子数均为0.2NAB.分别用Na2O2与CO2反应和KMnO4分解,制得1 ml O2,转移的电子数均为4NAC.标准状况下,锌与某浓度的H2SO4反应生成11.2 L气体,反应中转移的电子数为6.02×1023D.在2CuH+2HCl===CuCl2+Cu+2H2↑反应中,每生成22.4 L(标况)H2,反应转移的电子为1.5NA
解析 A项,0.1 ml Fe与0.1 ml Cl2反应,Cl2不足,0.1 ml Cu与0.1 ml Cl2恰好完全反应,转移的电子数均为0.2NA,正确;B项,Na2O2和KMnO4制得1 ml O2转移的电子数分别是2NA和4NA,错误;C项,标准状况下,锌与某浓度的H2SO4反应不论生成SO2还是H2,每生成1 ml气体都转移2 ml电子,正确;D项,在2CuH+2HCl===CuCl2+Cu+2H2↑反应中,反应生成2 ml H2共转移3 ml电子,正确。
5.(2023·浙江6月选考)NA为阿伏加德罗常数的值,下列说法正确的是( )
A.4.4 g C2H4O中含有σ键数目最多为 g H2O2中含有氧原子数为0.2NAC.向1 L 0.1 ml·L-1 CH3COOH溶液通氨气至中性,铵根离子数为0.1NAD.标准状况下,11.2 L Cl2通入水中,溶液中氯离子数为0.5NA
A.9 g水中含有的未成键电子对为2NAB.每产生34 g NH3,N2失去的电子数为6NAC.1 ml·L-1氨水中,含有的NH3·H2O分子数少于NAD.消耗11.2 L N2(已折算为标况)时,产生的O2分子数为0.75NA
7.已知2F2+2H2O===4HF+O2,用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1 ml O2中共用电子对数目为0.1NAB.2 L 0.2 ml·L-1 HF溶液中F-数目为 L F2中氟原子数目约为0.2NAD.该反应中每消耗3.6 g H2O时转移的电子数目为0.4NA解析 A.O2中两个氧原子间共用了2对电子,共用电子对数目为0.2NA,A错误;B.HF只能部分电离出H+、F-,2 L 0.2 ml·L-1 HF溶液中F-数目小于0.4NA,B错误;C.没有指明温度、压强,无法计算,C错误;D.3.6 g水的物质的量为0.2 ml,由方程式可得每消耗2 ml H2O转移4 ml电子,D正确。
相关课件
这是一份2026年高考化学总复习备课课件 高考热点2 越考越热的阿伏加德罗常数(NA),共28页。
这是一份2024年高考化学一轮复习 热点强化2 包罗万象的阿伏加德罗常数(NA)课件PPT,共41页。PPT课件主要包含了热点精讲,热点专练等内容,欢迎下载使用。
这是一份2024年高考化学一轮复习(新高考版) 第2章 热点强化4 包罗万象的阿伏加德罗常数(NA),文件包含2024年高考化学一轮复习新高考版第2章热点强化4包罗万象的阿伏加德罗常数NApptx、2024年高考化学一轮复习新高考版第2章热点强化4包罗万象的阿伏加德罗常数NAdocx、第2章热点强化4包罗万象的阿伏加德罗常数NAdocx等3份课件配套教学资源,其中PPT共39页, 欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




