





2026年人教版高考化学一轮复习课件 第五章 微专题11 分子结构与性质答题规范
展开 这是一份2026年人教版高考化学一轮复习课件 第五章 微专题11 分子结构与性质答题规范,共32页。PPT课件主要包含了原子半径FCl,TiCl键,四面体形,HCHBHA,sp3,四面体,sp2等内容,欢迎下载使用。
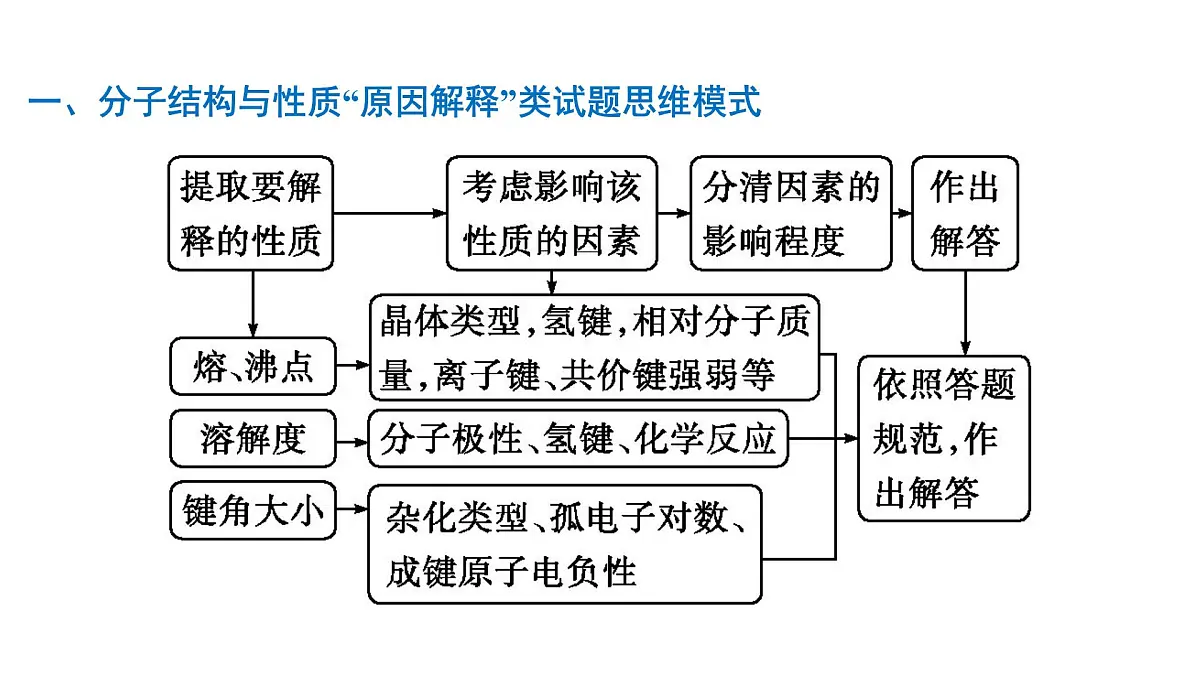
一、分子结构与性质“原因解释”类试题思维模式
二、分题型,练规范题型1 分子稳定性【思维角度】 分子稳定性取决于化学键(共价键)强弱,影响共价键强弱的因素有键长(原子半径)、键能。[典例1] (1)气态氢化物热稳定性HF大于HCl的主要原因是 。 (2)TiCl4稳定性比CCl4差,极易水解,试从结构角度分析其原因: 。
键长H—F键sp2>sp3。
【答题规范】 ××分子(离子)中心原子X采取××杂化,键角为××,而××分子(离子)中心原子X采取××杂化,键角为××。
2.价电子对的空间结构(或中心原子的杂化方式)相同,看中心原子孤电子对数,孤电子对数越多,斥力越大,键角越小。
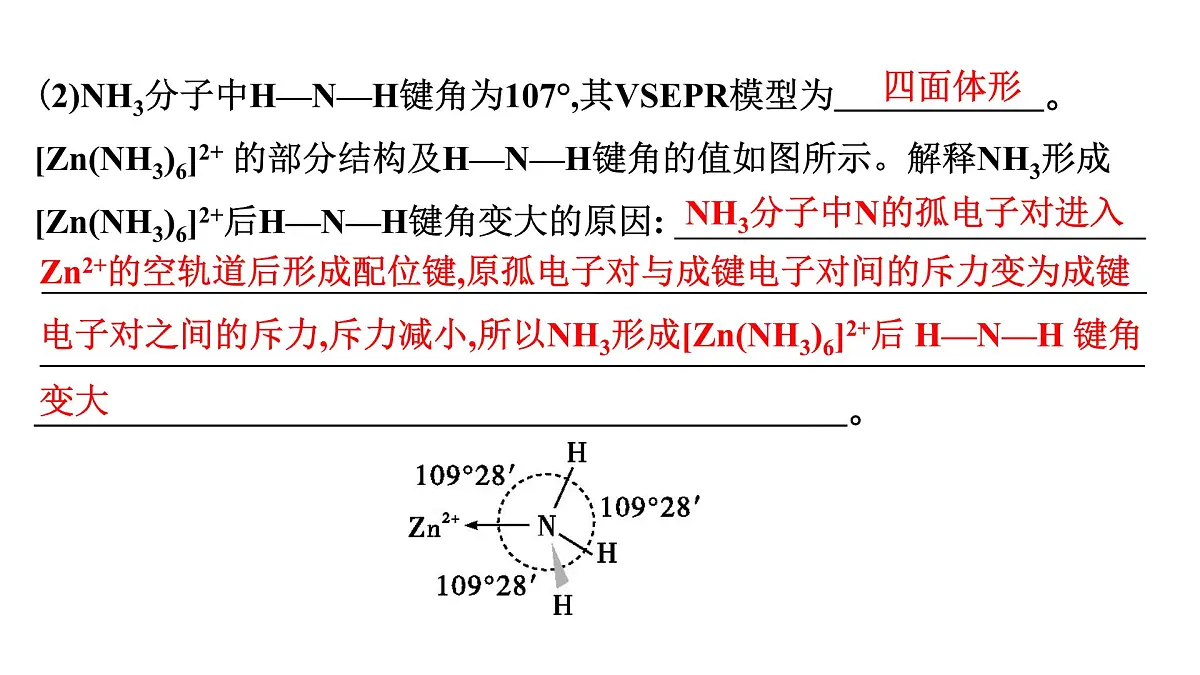
(2)NH3分子中H—N—H键角为107°,其VSEPR模型为 。[Zn(NH3)6]2+ 的部分结构及H—N—H键角的值如图所示。解释NH3形成[Zn(NH3)6]2+后H—N—H键角变大的原因: 。
NH3分子中N的孤电子对进入
Zn2+的空轨道后形成配位键,原孤电子对与成键电子对间的斥力变为成键电子对之间的斥力,斥力减小,所以NH3形成[Zn(NH3)6]2+后 H—N—H 键角变大
【答题规范】 ××分子中心原子孤电子对数为××,××分子中心原子孤电子对数为××,孤电子对对成键电子对的排斥作用较大,因而××键角小于××键角。
3.空间结构相同,中心原子相同或配位原子相同,看配位原子或中心原子的电负性。[典例4] (1)NH3的键角 (填“>”或“C。电负性B>C,在两种分子中成键电子对更靠近B原子,成键电子对相距更远,斥力更小,键角更小。
题型3 氢键对物质熔、沸点的影响【思维角度】 有氢键的分子熔、沸点高于没有氢键的分子;氢键多的分子熔、沸点高于氢键少的分子。[典例5] (2021·全国甲卷,35节选)甲醇的沸点(64.7 ℃)介于水(100 ℃)和甲硫醇(CH3SH,7.6 ℃)之间,其原因是 。
同为分子晶体,甲醇和水均能形成
分子间氢键,而甲硫醇不能形成分子间氢键,只有范德华力,且水分子间氢键比甲醇分子间氢键多
【答题规范】 ①同为分子晶体,××分子间存在氢键,而××分子间仅存在较弱的范德华力。②同为分子晶体,××存在分子间氢键,而××存在分子内氢键。
题型4 物质溶解性【思维角度】 ①“相似相溶”原理;②与溶剂分子能否形成氢键;③同为极性分子,极性大的溶解度大。[典例6] 在碘水中加入 1 mL 四氯化碳,振荡试管,观察碘被四氯化碳萃取,形成 色的碘的四氯化碳溶液。碘在四氯化碳中比在纯水中的溶解性好,试从分子结构角度解释其原因: 。
I2、CCl4都是非极性分子,而H2O
是极性分子,非极性溶质一般易溶于非极性溶剂
【答题规范】 ①××分子属于极性分子(或非极性分子),根据“相似相溶”规律,××易溶于水(或有机溶剂)。②××分子与水(或其他物质)形成分子间氢键,所以××易溶于水(或其他物质)。
题型5 分子极性大小比较【思维角度】 先考虑分子极性,同为极性分子,考虑共价键的极性大小(成键原子的电负性之差)。[典例7] (1)CCl4、COCl2极性大小比较及原因: 。 (2)OF2的极性 (填“大于”或“小于”)H2O的极性,解释原因: 。
CCl4的极性小于COCl2的
极性;因为前者是正四面体结构,正、负电荷重心重合,属于非极性分子,后者是平面三角形分子,正、负电荷重心不重合,属于极性分子
O与H的电负性差值比F与O的电负性差值大,则H2O的极性大于OF2的极性
【答题规范】 ①因为××分子是××空间结构,所以正、负电荷重心重合(或不重合),因此该分子属于非极性分子(或极性分子)。②因为××电负性大于(或小于)××电负性,所以××键极性大于(或小于)××键,因此××分子极性大于(或小于)××分子。
1.(2024·浙江6月选考,17节选)化合物HA、HB、HC和HD的结构如图。
(1)HA、HB和HC中羟基与水均可形成氢键(—O—H…OH2),按照氢键由强到弱对三种酸排序 ,请说明理由 。
(2)已知HC、HD钠盐的碱性NaC>NaD,请从结构角度说明理由: 。
S的原子半径大于O的原子半径,S—H键的键长大于O—H键的,S—H键的键能小于O—H键的,同时HC可形成分子间氢键,使得HD比HC更易电离出H+,所以酸性HD>HC,C-的水解能力大于D-的,碱性NaC>NaD
【解析】 (2)HC、HD钠盐的碱性NaC>NaD,说明酸性HCHC,C-的水解能力大于D-的,钠盐的碱性 NaC>NaD。
2.(2024·山东卷,16节选)MnOx可作HMF转化为FDCA的催化剂(如图)。FDCA的熔点远大于HMF,除相对分子质量存在差异外,另一重要原因是 。
FDCA形成的分子间氢键更多
【解析】 由HMF和FDCA的结构可知,HMF和FDCA 均能形成分子间氢键,但FDCA形成的分子间氢键更多,使得FDCA的熔点远大于HMF的。
—NH2的中心原子N上有
孤电子对,孤电子对对成键电子对排斥力大,键角变小
4.(2023·浙江1月选考,17节选)Si(NH2)4分子的空间结构(以Si为中心)名称为 ,分子中氮原子的杂化轨道类型是 。Si(NH2)4受热分解生成Si3N4和NH3,其受热不稳定的原因是 。
Si周围的NH2基团体积较大,
受热时斥力较强,Si(NH2)4中Si—N的键能相对较小;产物中气态分子数显著增多(熵增)
Cl—O的键长;原因是ClO2中既存在σ键,又存在大π键,原子轨道重叠的程度较大,因此其中Cl—O的键长较小,而Cl2O中只存在普通的σ键
ClO2中Cl—O的键长小于Cl2O中
因此,O的杂化方式为sp3,根据价层电子对互斥模型可知,n=4时,价层电子对的空间结构为四面体形,n=3时,价层电子对的空间结构为平面三角形,sp2杂化的键角一定大于sp3的,因此,虽然ClO2和Cl2O均为V形结构,但O—Cl—O键角大于Cl—O—Cl键角,孤电子对对成键电子对的排斥作用也改变不了这个结论。ClO2中Cl—O的键长小于Cl2O中Cl—O的键长,其原因是ClO2中既存在σ键,又存在大π键,原子轨道重叠的程度较大,而Cl2O中只存在普通的σ键。
(1)固态氟化氢中存在(HF)n形式,画出(HF)3的链状结构: 。
C—F的键能大于聚乙烯中C—H 的键能,键能越大,化学稳定性越高
7.(2020·山东卷,17节选)NH3、PH3、AsH3的沸点由高到低的顺序为 (填化学式,下同),还原性由强到弱的顺序为 ,键角由大到小的顺序为 。
NH3、AsH3、PH3
AsH3、PH3、NH3
NH3、PH3、AsH3
【解析】 NH3中存在分子间氢键,导致其沸点比与氮元素同主族的P、As的氢化物PH3、AsH3的沸点要高,而PH3、AsH3中均不存在分子间氢键,故影响PH3、AsH3沸点的因素为范德华力,相对分子质量越大,沸点越高,则沸点由高到低的顺序为NH3、AsH3、PH3。通常同主族元素随着原子序数的递增,气态氢化物的还原性逐渐增强,则还原性由强到弱的顺序是AsH3、PH3、NH3。同主族元素,随着原子序数的递增,电负性逐渐减小,则其气态氢化物中的成键电子对逐渐远离中心原子,致使成键电子对间的排斥力降低,键角逐渐减小,故键角由大到小的顺序是NH3、PH3、AsH3。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 
.png)




