






2026年人教版高考化学一轮复习课件 第五章 第5讲 晶体结构与性质
展开 这是一份2026年人教版高考化学一轮复习课件 第五章 第5讲 晶体结构与性质,共60页。PPT课件主要包含了认识晶体,考点一,周期性有序,各向异性,无各向异性,X射线衍射,平行六面体,任何间隙,②六棱柱晶胞,常见晶体结构与性质等内容,欢迎下载使用。
1.了解晶体与非晶体的区别;了解常见晶体的类型,了解不同类型晶体中结构微粒、微粒间作用力的区别。2.了解分子晶体、共价晶体、离子晶体、金属晶体结构与性质的关系。3.知道介于典型晶体之间的过渡晶体及混合型晶体是普遍存在的。
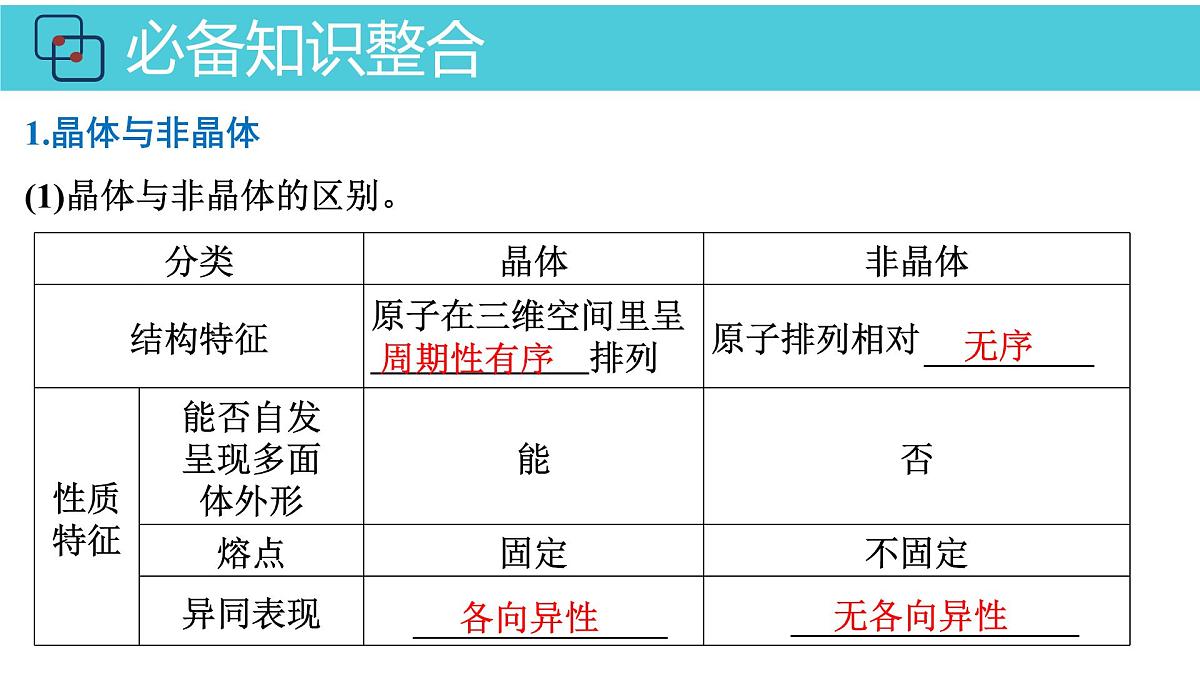
1.晶体与非晶体(1)晶体与非晶体的区别。
(2)获得晶体的三条途径。①熔融态物质凝固。如:从熔融态结晶出来的硫晶体。②气态物质冷却不经液态直接凝固(凝华)。如:凝华得到的碘晶体。③溶质从溶液中析出。如:从硫酸铜饱和溶液中析出的硫酸铜晶体。
2.晶胞(1)概念:晶胞是描述晶体结构的基本单元。(2)晶胞形状。常规的晶胞都是 。(3)晶体中晶胞的排列——无隙并置。①无隙:相邻晶胞之间没有 。②并置:所有晶胞 排列、 相同。
(4)晶胞中微粒数的计算方法——“切割法”。
[理解·辨析] 判断正误(1)具有规则几何外形的固体一定是晶体。( )(2)冰和固体碘晶体中相互作用力相同。( )(3)缺角的NaCl晶体在饱和NaCl溶液中会慢慢变为完美的立方体块。( )(4)区分晶体和非晶体最可靠的方法是对固体进行X射线衍射实验。( )(5)晶体内部的微粒按一定规律周期性排列。( )(6)晶胞是晶体中最小的“平行六面体”。( )
一、晶体与非晶体的区别1.(2024·河北衡水质检)下列物质中前者为晶体,后者为非晶体的是( )[A] 白磷、蓝矾[B] 玻璃、塑料[C] 碘、橡胶 [D] 食盐、蔗糖
【解析】 A中白磷和蓝矾都是晶体;B中二者均为非晶体;C中碘为晶体,橡胶为非晶体;D中二者均为晶体。
2.下列关于晶体和非晶体的说法正确的是( )[A] 晶体在三维空间里呈周期性有序排列,因此在各个不同的方向上具有相同的物理性质[B] 晶体在熔化过程中需要不断地吸热,温度不断地升高[C] 普通玻璃在各个不同的方向上力学、热学、电学、光学性质相同[D] 晶体和非晶体之间不可以相互转化
【解析】 晶体的许多物理性质常常会表现出各向异性,A不正确;晶体的熔点是固定的,所以在熔化过程中温度几乎不会变化,B不正确;在一定条件下晶体和非晶体是可以相互转化的,D不正确。
二、利用“均摊法”确定晶胞组成3.某晶体的晶胞如图所示,这种晶体中A、B、C三种微粒数目之比是( )[A] 3∶9∶4[B] 1∶4∶2[C] 2∶9∶4[D] 3∶8∶4
4.现有四种晶体,其构成微粒(均为单原子核微粒)排列方式如图所示,其化学式正确的是( )
[A] AB2 [B] EF2 [C] XY3Z [D] AB3
5.已知镧镍合金LaNin的晶胞结构如图,则LaNin中n= 。
6.下列(1)~(5)是几种常见的晶胞结构,填写每个晶胞中含有的粒子数。
(1)NaCl:含 个Na+、 个Cl-。 (2)干冰:含 个CO2。 (3)CaF2:含 个Ca2+、 个F-。 (4)金刚石:含 个C。 (5)铜:含 个原子。
1.四种常见晶体类型的比较
2.常见晶体的结构分析(1)典型的分子晶体——干冰和冰。
①干冰晶体中,每个CO2分子周围等距且紧邻的CO2分子有 个。②冰晶体中,每个水分子与相邻的 个水分子以氢键相连接,含1 ml H2O的冰中,最多可形成 ml氢键。
(2)典型的共价晶体——金刚石、二氧化硅。
(3)典型的离子晶体。①常见晶体结构模型。
a.NaCl型:在晶体中,每个Na+同时吸引 个Cl-,每个Cl-同时吸引 个Na+,配位数为 。每个晶胞含 个Na+和 个Cl-。b.CsCl型:在晶体中,每个Cl-吸引 个Cs+,每个Cs+吸引 个Cl-,配位数为 。每个晶胞含 个Cs+和 个Cl-。c.ZnS型:在晶体中,每个S2-吸引 个Zn2+,每个Zn2+吸引 个S2-。每个晶胞含 个Zn2+和 个 S2-。d.CaF2型:在晶体中,每个Ca2+吸引 个F-,每个F-吸引 个Ca2+。每个晶胞含 个Ca2+和 个 F-。
(4)常见金属晶体①常见金属晶体的结构
②金属晶体的物理性质及解释
(5)过渡晶体与混合型晶体。①过渡晶体:纯粹的分子晶体、共价晶体、离子晶体和金属晶体四种典型晶体是不多的,大多数晶体是它们之间的过渡晶体。人们通常把偏向离子晶体的过渡晶体当作离子晶体来处理,把偏向共价晶体的过渡晶体当作共价晶体来处理。
②混合型晶体(以石墨为例)。
石墨层状晶体中,层与层之间的作用是 ,平均每个正六边形拥有的碳原子个数是 ,碳原子采取的杂化方式是 。
[理解·辨析] 判断正误(1)在晶体中只要有阳离子就一定有阴离子。( )(2)金属元素和非金属元素组成的晶体不一定是离子晶体。( )(3)分子晶体的熔点一定比金属晶体的低。( )(4)离子晶体一定都含有金属元素。( )(5)离子晶体是由阴、阳离子构成的,所以离子晶体能够导电。( )(6)共价晶体的熔点一定比离子晶体的高。( )(7)金属导电是因为在外加电场作用下产生自由电子。( )(8)冰中包含的作用力有范德华力、氢键和共价键。( )
一、常见晶体类型的判断1.(2024·福建福州期中)下表列出的有关晶体的说法中错误的是( )
【解析】 碘化钾为离子晶体,组成粒子为离子,组成晶体粒子间的结合力为离子键,A正确;水银为金属晶体,组成粒子为金属阳离子和电子,组成晶体粒子间的结合力为金属键,B正确;干冰为分子晶体,组成粒子为分子,分子之间的结合力为范德华力,是分子间作用力,C正确;二氧化硅为共价晶体,组成粒子为原子,组成晶体粒子间的结合力为共价键,D错误。
2.根据下列物质的晶体结构特点,将对应序号填在横线上。(1)干冰晶体: 。 (2)氯化钠晶体: 。 (3)金刚石: 。 (4)氯化铯: 。 (5)氟化钙: 。 (6)冰晶体: 。 (7)硫化锌: 。
根据各类晶体的特征性质判断晶体类型(1)根据晶体性质判断晶体类型。①熔、沸点低的晶体为分子晶体。②熔、沸点较高,且在水溶液中或熔融状态下能导电的晶体为离子晶体。③熔、沸点很高,一般不导电,不溶于一般溶剂的晶体为共价晶体;④能导电、传热,具有延展性的晶体为金属晶体。(2)根据典型晶体的晶胞结构特征判断晶体类型。
二、常见晶体类型的结构特点3.金刚石和石墨是碳元素形成的两种单质。下列说法正确的是( )[A] 金刚石和石墨晶体中最小的环均含有6个碳原子[B] 在金刚石中每个C连接4个六元环,石墨中每个C连接3个六元环[C] 金刚石与石墨中碳原子的杂化方式均为sp2[D] 金刚石中碳原子数与C—C键数之比为1∶4,而石墨中碳原子数与C—C键数之比为1∶3
4.如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。
(1)其中代表金刚石的是 (填序号,下同),金刚石属于 晶体。
【解析】 (1)在金刚石晶体中,每个碳原子可与周围四个碳原子形成共价键,将这四个碳原子连接起来后可以形成正四面体,体心有一个碳原子,所以图④为金刚石,金刚石属于共价晶体。
(2)其中代表石墨的是 ,每个正六边形平均占有碳原子数为 。
【解析】 (2)石墨是层状结构,在层与层之间以范德华力相互作用,在层内碳原子之间以共价键相互作用,形成正六边形,每个六元环有6个碳原子,每个碳原子为3个六元环共有,所以每个正六边形平均占有 2个碳原子,所以图⑤为石墨。
(3)其中代表NaCl的是 ,每个Na+周围与它最接近且距离相等的Na+有 个。
【解析】 (3)在NaCl晶体中,每个钠离子周围有6个等距且紧邻的氯离子,每个氯离子周围也有6个等距且紧邻的钠离子,所以图①为NaCl的结构,根据题给结构,每个钠离子周围与它最接近且距离相等的Na+有12个。
(4)其中代表CsCl的是 ,它属于 晶体,每个Cs+与 个Cl-紧邻。
【解析】 (4)CsCl的晶体中每个铯离子周围有8个等距且紧邻的氯离子,每个氯离子周围也有8个等距且紧邻的铯离子,CsCl为离子晶体,所以图③为CsCl的结构。
(5)其中代表干冰的是 ,它属于 晶体,每个CO2分子与 个CO2分子紧邻。
【解析】 (5)干冰是分子晶体,CO2分子位于立方体的顶点和面心上,以顶点上的CO2分子为例,与它等距且紧邻的CO2分子分布在与该顶点相连的12个面的面心上,所以图②为干冰。
三、晶体熔、沸点比较5.下列关于物质的熔点、沸点高低顺序中,正确的是( )[A] 金刚石>晶体硅>金刚砂[B] NaF>NaCl>NaBr[C] 邻羟基苯甲酸>对羟基苯甲酸[D] 生铁>纯铁>钠
【解析】 三者均为共价晶体,共价晶体中共价键的键能越大,熔点、沸点越高,故熔点、沸点由高到低的顺序为金刚石>金刚砂>晶体硅,A错误;三者均为离子晶体,离子所带电荷数相同,因离子半径F-NaBr,B正确;邻羟基苯甲酸可以形成分子内氢键,使熔点、沸点偏低,而对羟基苯甲酸可以形成分子间氢键,使熔点、沸点偏高,故对羟基苯甲酸的熔点、沸点比邻羟基苯甲酸的高,C错误;生铁为铁合金,熔点要低于纯铁,D错误。
6.(1)(2022·浙江1月选考)四种晶体的熔点数据如下表:
CF4和SiF4熔点相差较小,BF3和AlF3熔点相差较大,原因是 。
分子晶体,结构相似,分子间作用力相差较小,所以熔点相差较小;BF3通过分子间作用力形成分子晶体,AlF3通过离子键形成离子晶体,破坏离子键需要的能量多得多,所以熔点相差较大
(2)K和Cr属于同一周期元素,且核外最外层电子排布相同,但金属K的熔点、沸点等都比金属Cr的低,原因是 。
K的原子半径较大且价电子数较少,
H2O>CH3OH>CO2>H2
H2O与CH3OH均为极性分子,水中的氢键比甲醇中的多;CO2与H2均为非极性分子,CO2的相对分子质量较大,范德华力较大
(4)GaF3的熔点高于1 000 ℃,GaCl3的熔点为77.9 ℃,其原因是 。 (5)单质氧有两种同素异形体,其中沸点高的是 (填化学式),原因是 。
GaF3为离子晶体,GaCl3为分子晶体
O3是极性分子,相对分子质量较大,范德华力较大
物质熔、沸点高低的比较方法(1)首先看物质的状态,一般情况下,固体>液体>气体;然后看物质的晶体类型,一般是共价晶体>离子晶体>分子晶体;晶体类型相同时再根据同种类型晶体熔、沸点比较的规律进行判断。
(2)同类型晶体熔、沸点比较的一般思路。
晶体密度和微粒间距离的计算
1.晶胞参数晶胞的形状和大小可以用6个参数来表示,包括晶胞的3组棱长a、b、c和3组棱相互间的夹角α、β、γ,即晶格特征参数,简称晶胞参数。
2.晶体中微粒配位数的计算(1)定义:一个微粒周围最邻近的微粒的数目称为配位数。(2)求算。①晶体中原子(或分子)的配位数:若晶体中的微粒为同种原子或同种分子,则某原子(或分子)的配位数指的是该原子(或分子)最接近且等距离的原子(或分子)的数目。②离子晶体的配位数:指一个离子周围最接近且等距离的异种电性离子的数目。
3.晶体结构的相关计算(1)空间利用率。
(2)晶胞中各线段之间的关系(立方晶胞,棱长为a)。
(3)宏观晶体密度与微观晶胞参数的关系。
[示例] 某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长为a pm,则该物质的化学式为 ;晶体中Pb2+与Cs+最短距离为 pm;晶体的密度ρ= g·cm-3(设阿伏加德罗常数的值为NA,用含a、NA的代数式表示;可能用到的相对原子质量:Cs—133 Pb—207 I—127)。
一、晶体密度的求算1.钒的某种氧化物的立方晶胞结构如图所示,晶胞参数为a pm。该晶体的密度为 (设NA为阿伏加德罗常数的值)。
2.(2024·河北师大实验中学质量检测)CaF2的晶胞结构如图所示,若该立方晶胞参数为a pm,CaF2的摩尔质量为M g/ml,用NA来表示阿伏加德罗常数的值,则CaF2晶体的密度为 g/cm3(写出表达式)。
二、晶胞中微粒间距的求算
4.如图是铁单质的晶胞模型。已知其晶体密度为 d g·cm-3,铁原子的半径为 nm (用含有d、NA的代数式表示)。
1.(2024·山东卷,4)下列物质均为共价晶体且成键结构相似,其中熔点最低的是( )[A] 金刚石(C)[B] 单晶硅(Si)[C] 金刚砂(SiC)[D] 氮化硼(BN,立方相)
【解析】 金刚石(C)、单晶硅(Si)、金刚砂(SiC)、立方氮化硼(BN)都为共价晶体,结构相似,则原子半径越大,键长越长,键能越小,熔、沸点越低,在这几种晶体中,键长Si—Si>Si—C>B—N>C—C,所以熔点最低的为单晶硅。
2.(2024·甘肃卷,12)β-MgCl2晶体中,多个晶胞无隙并置而成的结构如图甲所示,其中部分结构显示为图乙,下列说法错误的是( )[A] 电负性:MgSO2
(2)FeF3具有较高的熔点(高于1 000 ℃),其化学键类型是 ,FeBr3的相对分子质量大于FeF3的,但其熔点只有200 ℃,原因是 。 (3)已知氨(NH3,熔点-77.8 ℃、沸点-33.5 ℃),联氨(N2H4,熔点2 ℃、沸点113.5 ℃),解释其熔、沸点高低的主要原因: 。
FeF3属于离子晶体,
FeBr3的化学键以共价键为主,属于分子晶体
联氨分子间形成氢键的数目
多于氨分子间形成氢键的数目
(4)已知氮化硼与砷化镓属于同种类型的晶体。两种晶体中熔点较高的是 (填化学式),其理由是 。
两种晶体均为共价晶体,N和B的原子半径
较小,键能较大,熔点较高
13.(16分,每空2分)Ⅰ.C60、金刚石、石墨的结构如图所示(石墨仅表示出其中的一层结构):
【解析】 (1)金刚石、石墨和C60是由碳元素组成的不同单质,三者互为同素异形体,故选B。
(1)金刚石、石墨和C60三者互为 (填字母)。 A.同分异构体B.同素异形体C.同系物D.同位素
(2)C60的晶体类型为 。
【解析】 (2)C60属于分子晶体。
(3)晶体硅的结构跟金刚石相似,1 ml晶体硅中所含有硅硅单键的数目是 (设NA为阿伏加德罗常数的值)。
【解析】 (3)晶体硅的结构与金刚石相似,金刚石中1个碳碳键被两个碳原子共用,一个碳原子形成4个碳碳键,1 ml金刚石中有2 ml碳碳键,故1 ml晶体硅中含有硅硅单键的数目为2NA。
(4)石墨层状结构中,平均每个正六边形占有的碳原子数是 。
Ⅱ.类石墨相氮化碳(g-C3N4)作为一种新型光催化材料,在光解水产氢等领域具有广阔的应用前景,研究表明,非金属掺杂(O、S等)能提高其光催化活性。g-C3N4具有和石墨相似的层状结构,其中一种二维平面结构如图所示。(5)g-C3N4晶体中存在的微粒间作用力有 (填字母)。 a.非极性键b.金属键c.π键d.范德华力
【解析】 (5)根据题意,g-C3N4晶体具有和石墨相似的层状结构,结合二维平面结构图,判断其存在的微粒间作用力有极性键、π键和范德华力。
(6)g-C3N4中,碳原子的杂化轨道类型为 ,氮原子的配位数为 。
【解析】 (6)g-C3N4中,结合二维平面结构图可知,碳原子与氮原子形成三个σ键,层内存在大π键,不存在孤电子对,故碳原子的杂化轨道类型为sp2;根据二维平面结构图可知,氮原子的成键有两种情况,连两个碳原子和连三个碳原子,故氮原子的配位数为2、3。
(7)每个基本结构单元(图中实线圈部分)中两个氮原子(图中虚线圈所示)被氧原子代替,形成氧掺杂的g-C3N4(OPCN)。OPCN的化学式为 。
课时作业27 晶胞结构分析与简单计算
一、选择题(共10小题,每小题7分,共70分)1.某物质的晶体中含有A、B、C三种元素,其排列方式如图所示(其中前后两面面心中的B元素的原子未能画出)。则晶体中A、B、C的原子个数比为( )[A] 1∶3∶1[B] 2∶3∶1[C] 2∶2∶1[D] 1∶3∶3
2.我国科学家合成了富集11B的非碳导热材料立方相氮化硼晶体,晶胞结构如图所示。下列说法正确的是( )[A] 11BN和10BN的性质无差异[B] 该晶体具有良好的导电性[C] 该晶胞中含有14个B、4个N[D] 氮原子周围等距且最近的氮原子数为12
3.(2025·山东青岛阶段练习)硅材料在工业生产中具有重要的应用,下列说法正确的是( )[A] 熔、沸点比较:金刚石
相关课件
这是一份2026年人教版高考化学一轮复习课件 第五章 第5讲 晶体结构与性质,共60页。PPT课件主要包含了认识晶体,考点一,周期性有序,各向异性,无各向异性,X射线衍射,平行六面体,任何间隙,②六棱柱晶胞,常见晶体结构与性质等内容,欢迎下载使用。
这是一份2026届高考化学一轮专题复习课件:第五章 第四讲 晶体结构与性质,共23页。PPT课件主要包含了晶体结构模型,周期性有序,各向异性,各向同性,X射线衍射,必备知识,返回目录,特别提醒,面心立方最密,范德华力等内容,欢迎下载使用。
这是一份2026届高考化学一轮复习习题课件及答案解析:第五章 第四讲 晶体结构与性质,共44页。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




