
人教版 (2019)选择性必修2分子晶体与共价晶体导学案
展开 这是一份人教版 (2019)选择性必修2分子晶体与共价晶体导学案,共4页。学案主要包含了学习目标,知识梳理等内容,欢迎下载使用。
1、知道共价晶体的概念,能够从共价晶体的结构特点理解其物理特性
2、能描述金刚石、二氧化硅等共价晶体的结构与性质的关系
【知识梳理】
一、共价晶体的概念和组成
1、概念:相邻原子间以共价键相结合而形成空间立体网状结构的晶体叫做共价晶体
2、空间结构:整块晶体是一个三维的共价键网状结构,不存在单个的小分子,是一个“巨分子”
3、构成的微粒:原子
4、微粒间的作用力:共价键
5、熔化时破坏的作用力:共价键
【思考】①能否说有共价键的晶体是共价晶体?
②能否说构成微粒为原子的是共价晶体?
③能否说原子间均以共价键连接的为共价晶体?
④共价晶体中是否存在单个的小分子?
6、常见共价晶体
(1)某些单质:硼(B)、硅(Si)、金刚石、锗(Ge)等
(2)某些非金属化合物:金刚砂(SiC)、二氧化硅(SiO2)、氮化硼(BN)、氮化硅(Si3N4)等
(3)极少数金属化合物:刚玉(αAl2O3)、氮化铝(AlN)等
【微点拨】
①共价晶体中不存在单个分子,化学式仅仅表示的是物质中的原子个数比关系,不是分子式
②由原子组成的晶体不一定是共价晶体。如:稀有气体组成的晶体属于分子晶体
③共价晶体中一定存在共价键,但晶体中有共价键却不一定都是共价晶体,还可以是分子晶体或离子晶体
二、常见共价晶体的结构特征
1、金刚石
(1)每个碳原子与周围紧邻的4个碳原子以共价键结合成正四面体结构,向空间伸展形成空间网状结构
(2)碳原子采取sp3杂化,C—C—C夹角为109°28′
(3)金刚石晶胞的每个顶点和面心均有1个C原子,晶胞内部有4个C原子,每个金刚石晶胞中含有8×eq \f(1,8)+6×eq \f(1,2)+4=8个碳原子
(4)最小碳环由6个碳原子组成,并且不在同一平面(实际为椅式结构),但最小环上有4个碳原子在同一平面内
(5)每个碳原子被12个六元环共用,每个共价键被6个六元环共用,一个六元环实际拥有个碳原子
(6)C原子数与C—C键数之比为1∶2,12g金刚石中有2 ml共价键
(7)密度=eq \f(8×12 g·ml-1,NA×a3) (a为晶胞边长,NA为阿伏加德罗常数)
2、晶体Si:由于Si与碳同主族,晶体Si的结构同金刚石的结构相同。将金刚石晶胞中的C原子全部换成Si原子,健长稍长些便可得到晶体硅的晶胞
(1)每个硅原子均以4个共价键对称地与相邻的4个硅原子相结合,形成正四面体结构,键角均为109°28′
(2)每个硅晶胞中含有8个硅原子,最小的碳环为6元环,硅原子为sp3杂化
(3)每个硅原子被12个六元环共用,每个共价键被6个六元环共用,一个六元环实际拥有个硅原子
(4)硅原子数与Si—Si键数之比为1∶2,1ml Si中含有2 ml共价键
3、二氧化硅晶体
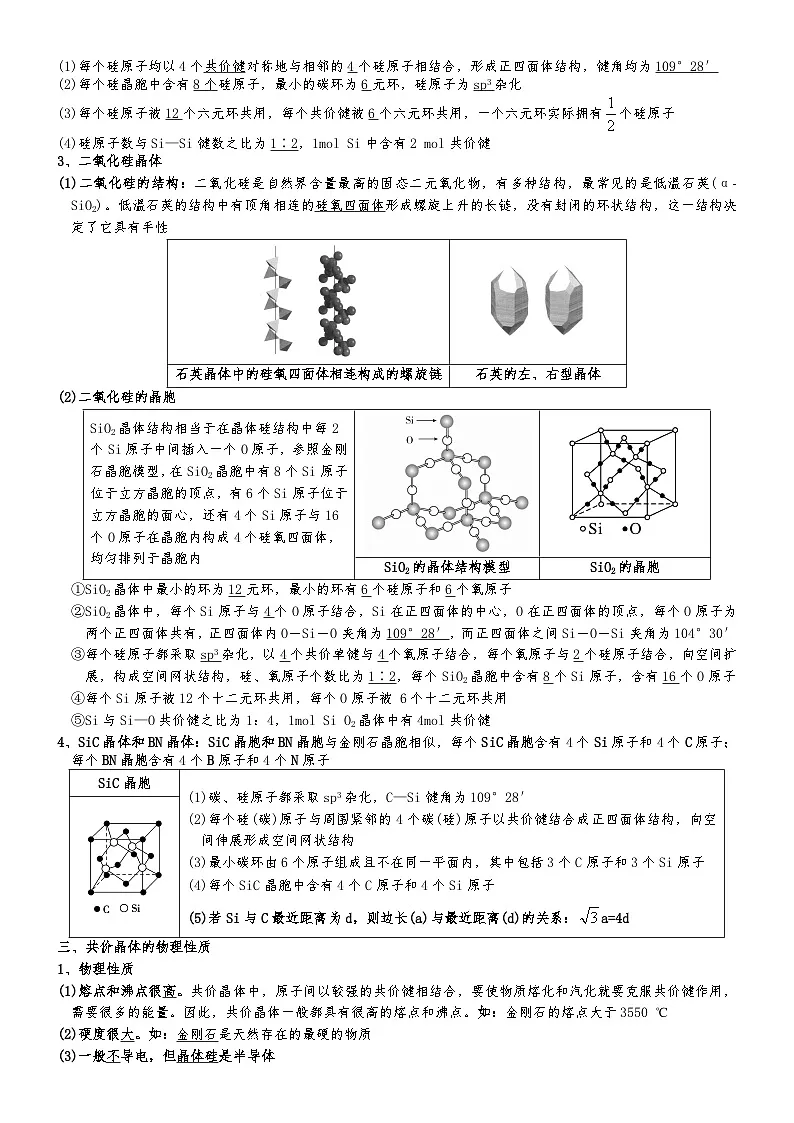
(1)二氧化硅的结构:二氧化硅是自然界含量最高的固态二元氧化物,有多种结构,最常见的是低温石英(αSiO2)。低温石英的结构中有顶角相连的硅氧四面体形成螺旋上升的长链,没有封闭的环状结构,这一结构决定了它具有手性
(2)二氧化硅的晶胞
①SiO2晶体中最小的环为12元环,最小的环有6个硅原子和6个氧原子
②SiO2晶体中,每个Si原子与4个O原子结合,Si在正四面体的中心,O在正四面体的顶点,每个O原子为两个正四面体共有,正四面体内O-Si-O夹角为109°28′,而正四面体之间Si-O-Si夹角为104°30′
③每个硅原子都采取sp3杂化,以4个共价单键与4个氧原子结合,每个氧原子与2个硅原子结合,向空间扩展,构成空间网状结构,硅、氧原子个数比为1∶2,每个SiO2晶胞中含有8个Si原子,含有16个O原子
= 4 \* GB3 \* MERGEFORMAT ④每个Si原子被12个十二元环共用,每个O原子被 6个十二元环共用
= 5 \* GB3 \* MERGEFORMAT ⑤Si与Si—O共价键之比为1:4,1ml Si O2晶体中有4ml共价键
4、SiC晶体和BN晶体:SiC晶胞和BN晶胞与金刚石晶胞相似,每个SiC晶胞含有4个Si原子和4个C原子;每个BN晶胞含有4个B原子和4个N原子
三、共价晶体的物理性质
1、物理性质
(1)熔点和沸点很高。共价晶体中,原子间以较强的共价键相结合,要使物质熔化和汽化就要克服共价键作用,需要很多的能量。因此,共价晶体一般都具有很高的熔点和沸点。如:金刚石的熔点大于3550 ℃
(2)硬度很大。如:金刚石是天然存在的最硬的物质
(3)一般不导电,但晶体硅是半导体
(4)难溶于一些常见的溶剂
2、共价晶体熔、沸点比较规律
结构相似的共价晶体,原子半径越小,键长越短,键能越大,晶体的熔、沸点越高
如:金刚石、金刚砂(碳化硅)、晶体硅的熔、沸点逐渐降低
3、共价晶体熔、沸点比较答题模板
四、共价晶体与分子晶体的比较
1、共价晶体与分子晶体的比较
2、判断晶体类型(共价晶体和分子晶体)的方法:非金属单质和共价化合物所形成的晶体是属于共价晶体还是分子晶体,可以从以下角度进行分析判断:
(1)依据组成晶体的粒子和粒子间的作用力判断:组成共价晶体的粒子是原子,粒子间的作用力是共价键;组成分子晶体的粒子是分子,粒子间的作用力是分子间作用力
(2)依据物质的分类判断
①常见的共价晶体有:金刚石、晶体硼、晶体硅、晶体锗等单质;SiO2、SiC、BN、AlN、Si3N4等化合物;新型无机非金属材料“家庭 ”的成员(如Si3N4、BN等)熔点高、硬度大、耐高温、抗氧化,它们大多属于共价晶体
②大多数非金属单质(金刚石、石墨、晶体硅等除外)、气态氢化物、非金属氧化物(SiO2除外)、酸、绝大多数有机物的晶体(有机盐除外)都是分子晶体
(3)依据晶体的熔点判断:共价晶体熔、沸点高,常在1000 ℃以上;分子晶体熔、沸点低,常在数百摄氏度以下甚至更低的温度
(4)依据物质的状态判断:常温下呈气态或液态的单质与化合物,其固态时都属于分子晶体
(5)依据物质的挥发性判断:易挥发的物质在固态时都属于分子晶体
(6)依据导电性判断:分子晶体为非导体,但部分分子晶体溶于水后能够导电;共价晶体多数为非导体,但晶体硅、晶体锗是半导体
(7)依据硬度和机械性能判断:共价晶体硬度大,分子晶体硬度小且较脆
金刚石晶体结构、键角和晶胞示意图
原子半径(r)与边长(a)的关系:a=8r
晶体结构模型
C—C—C夹角为109°28′
金刚石的晶胞
金刚石的晶胞
石英晶体中的硅氧四面体相连构成的螺旋链
石英的左、右型晶体
SiO2晶体结构相当于在晶体硅结构中每2个Si原子中间插入一个O原子,参照金刚石晶胞模型,在SiO2晶胞中有8个Si原子位于立方晶胞的顶点,有6个Si原子位于立方晶胞的面心,还有4个Si原子与16个O原子在晶胞内构成4个硅氧四面体,均匀排列于晶胞内
SiO2的晶体结构模型
SiO2的晶胞
SiC晶胞
(1)碳、硅原子都采取sp3杂化,C—Si键角为109°28′
(2)每个硅(碳)原子与周围紧邻的4个碳(硅)原子以共价键结合成正四面体结构,向空间伸展形成空间网状结构
(3)最小碳环由6个原子组成且不在同一平面内,其中包括3个C原子和3个Si原子
(4)每个SiC晶胞中含有4个C原子和4个Si原子
(5)若Si与C最近距离为d,则边长(a)与最近距离(d)的关系:a=4d
答题策略
看共价键的强弱,取决于键长;即:成键原子半径大小
答题模板
同为共价晶体,×××晶体的键长短,键能大,熔沸点高
1
Si单质比化合物SiC的熔点高,理由是:晶体硅与SiC均属于共价晶体,晶体硅中的Si—Si比SiC中Si—C的键长长,故键能也低,所以SiC熔点低
晶体类型
共价晶体
分子晶体
概念
相邻原子间以共价键相结合而形成的空间立体网状结构的晶体
分子间以分子间作用力相结合的晶体
组成微粒
原子
分子
微粒间作用力
共价键
分子间作用力
结构特点
空间网状结构
分子密堆积或非密堆积
堆积方式
在共价晶体中,各原子均以共价键结合,因为共价键有方向性和饱和性,所以中心原子周围的原子数目是有限的,原子不采取密堆积方式
①分子间不存在氢键的分子晶体,由于范德华力没有方向性和饱和性,分子尽可能采取密堆积方式
②分子间存在氢键的分子晶体,由于氢键具有方向性和饱和性,分子不能采取密堆积方式
物理性质
熔、沸点高,硬度大,不溶于常见的溶剂,不导电,个别为半导体
熔、沸点较低,硬度较小,部分溶于水,不导电,部分溶于水导电
熔化时破坏
的作用力
破坏共价键
一定破坏范德华力,有时还破坏氢键,如:冰熔化
熔、沸点比较
共价晶体>分子晶体,共价晶体的熔、沸点与共价键有关,分子晶体的熔、沸点与分子间作用力有关。共价键的作用力远大于分子间作用力
实例
金刚石、二氧化硅等
冰、干冰等
相关学案
这是一份人教版 (2019)选择性必修2分子晶体与共价晶体导学案,共4页。学案主要包含了学习目标,知识梳理等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修2分子晶体与共价晶体学案,共4页。学案主要包含了晶体熔沸点比较,均摊法的应用等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修2第二节 分子晶体与共价晶体导学案及答案,共5页。学案主要包含了学法指导,基础梳理,课堂练习等内容,欢迎下载使用。
相关学案 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




