

所属成套资源:2026届高三化学一轮总复习 学案(含答案)
第5讲 化学键与分子的性质 学案(含答案)2026届高三化学一轮总复习
展开 这是一份第5讲 化学键与分子的性质 学案(含答案)2026届高三化学一轮总复习,共14页。学案主要包含了 化学键, 共价键, 离子化合物和共价化合物, 电子式, 结构式等内容,欢迎下载使用。
考点一 化学键 物质组成 电子式
一、 化学键
1. 定义及分类
2. 化学反应的本质:反应物的旧化学键________与生成物的新化学键________。
3. 离子键和共价键的比较
二、 共价键
1. 分类
【思维拓展】
σ键和π键的识别和计算
(1)σ键和π键的识别
①键线式呈现的结构,不能忽略省去的碳氢键。
②含有苯环的结构,不能忽略苯环中的碳氢键。
1 ml苯分子中含有σ键的物质的量为12 ml。乙炔分子中σ键和π键的数目之比是3∶2。HCOONa中σ键和π键的数目之比是3∶1。
(2)配合物中的σ键和π键(一般,配位键是σ键)
①由内界与外界组成的配合物:内界和外界之间一般存在离子键,如[Cu(NH3)4]SO4中,[Cu(NH3)4]2+与SOeq \\al(2-,4)之间是离子键,内界与外界中均含有σ键。1 ml [Cu(NH3)4]SO4中含有σ键的物质的量为20 ml。
②无外界的配合物,直接计算内界中的σ键数目。1 ml [Fe(CO)5]中含有σ键的物质的量为10 ml,π键的物质的量为10 ml。
2. 键参数—键能、键长、键角
(1)概念
(2)键参数对分子性质的影响
①键能越大,键长越短,分子越稳定。
②
三、 离子化合物和共价化合物
四、 电子式
1. 概念:在元素符号周围用“·”或“×”来表示原子的____________的式子。
2. 常见物质电子式的书写
(1)原子
Na:________,Cl:________。
(2)简单离子
Na+:________,F-:________。
(3)复杂离子
NHeq \\al(+,4):____________,OH-:________。
(4)离子化合物
MgCl2:________________,
Na2O:____________,
Na2O2:____________。
(5)非金属单质及共价化合物
N2:________,
H2O:________,H2O2:________。
3. 用电子式表示化合物的形成过程
(1)离子化合物
NaCl:。
(2)共价化合物
HCl:H+Cl, ―→HCl, 。
五、 结构式
1. 定义:用一根短线“—”表示一个共用电子对的式子。
2. 写出下列物质的结构式:
N2:________;H2O:________;
NH3:________;CO2:________;
CS2:________;HClO:________;
HCN:________;N2H4:________;
HCHO:________;(CN)2:________;
(SCN)2:________________。
【易错辨析】
1. (2024·南京、盐城一模)CaC2只含有离子键。( )
2. (2023·南京、盐城一模)Ca(OH)2的电子式为Ca2+[O, H]eq \\al(-,2)。( )
3. 在任何情况下,都是σ键比π键强度大。( )
4. σ键可以绕键轴旋转,π键不能绕键轴旋转。( )
5. 碳碳三键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍。( )
1. (2025·南通模拟)我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2eq \(――→,\s\up7(催化剂))CO2+H2O。下列有关说法正确的是( )
A. CO2只含有非极性共价键
B. 0.5 ml HCHO含有1 ml σ键
C. HCHO、CO2分子中只含有σ键
D. H2O中含有极性键
2. (2024·镇江一中期初学情检测)工业上制备保险粉的反应为HCOONa+NaOH+2SO2===Na2S2O4+CO2+H2O。下列有关说法正确的是( )
A. Na+的结构示意图为
B. NaOH的电子式为NaO, H
C. HCOONa中含有σ键和π键的数目之比为3∶1
D. 基态S原子核外价电子的轨道表达式为
3. (1)N2H4·2HCl为离子化合物,1 ml N2H4·2HCl中含有________ ml σ键。
(2)(2024·扬州三模)1 ml [Zn(NH3)4]2+中含有的σ键的数目为________。
(3)(2024·南通通州)分子中,σ键和π键的数目之比为________。
(4)(2024·南通高三三模)中σ键与π键数目之比为____________。
考点二 分子(或离子)的空间结构及中心原子杂化类型
一、 价层电子对互斥模型(VSEPR)
1. 理论要点
(1)价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
(2)孤电子对排斥力较大,孤电子对越多,排斥力越强,键角越小。
2. ABm型分子的价电子对数计算方法
对于ABm型分子(A是中心原子,B是配位原子),分子的价电子对数可以通过下式确定:
n=eq \f(1,2)(中心原子的价电子数+每个配位原子提供的价电子数×m)
其中,中心原子的价电子数等于中心原子的最外层电子数,配位原子中卤素原子、氢原子提供1个价电子,氧原子和硫原子按不提供价电子计算。
3. 孤电子对数=价电子对数(n)-配位原子数(m)。
例如,SOCl2的空间结构的判断:
SOCl2的中心原子为S,价层电子对数为eq \f(6+1×0+2×1,2)=4,这些价层电子对互相排斥,形成四面体形的价层电子对互斥模型,由于中心原子上有1个孤电子对,则SOCl2的空间结构为三角锥形。
二、 杂化轨道理论
1. 理论要点
中心原子上若干不同类型(主要是s、p轨道)、能量相近的原子轨道混合起来,重新组合成同等数目、能量完全相同的新轨道。杂化轨道数不同,轨道间的夹角就不同,形成分子的空间结构就不同。
2. 杂化轨道三种类型
3. 由杂化轨道数判断中心原子的杂化类型
杂化轨道用来形成σ键和容纳孤电子对,所以有公式:杂化轨道数=中心原子的孤电子对数+中心原子的σ键个数=中心原子的价层电子对数。
4. 分子(或离子)的空间结构分析示例
【思维拓展】
影响键角大小的因素
(1)杂化类型不同
键角(中心原子):sp3杂化Br—I,A错误;P4为非极性分子,B错误;IF3是由极性键构成的极性分子,C错误。
考点四 分子间作用力
知识归纳
一、 无 有 氢键 范德华力 ①越大 ②越大
二、 1. 非极性 极性 极性 极性 非极性 非极性
2. 好
【易错辨析】
1. × 2. × 3. √ 4. √ 5. ×
命题突破
1. A 解析:过氧化氢和水均为极性分子,四氯化碳是非极性分子,根据相似相溶原理,过氧化氢能溶于水而难溶于四氯化碳,故A正确;由于邻羟基苯甲醛形成分子内氢键,而对羟基苯甲醛能够形成分子间氢键,所以邻羟基苯甲醛比对羟基苯甲醛熔、沸点低,故B错误;H—O的键能较大,故水加热到很高的温度都难以分解,与氢键无关,故C错误;烷基是推电子基团,烃基越长推电子效应越大,这一效应使羧基中的氧氢键极性减小,导致氢离子更难电离,所以甲酸、乙酸、丙酸的酸性逐渐减弱,故D错误。
2. (1)能形成分子间氢键,而不能形成分子间氢键
(2)CF4是非极性分子,NF3和N2H4是极性分子,但N2H4易与水形成分子间氢键 (3)乙醇可与水形成氢键 (4)中含有—NH2,可以形成氢键
解析:(2)三种物质都是分子,CF4是非极性分子,根据相似相溶原理,CF4在水中溶解度最小,NF3和N2H4都是极性分子,且N2H4能与水形成氢键,故溶解度最大。
(4)中含有—NH2,可以形成氢键,导致沸点升高。
考点五 分子的手性
知识归纳
一、 镜像 不能重叠
二、 手性异构体
三、 四个不同基团或原子
【易错辨析】
1. × 2. × 3. √ 4. × 5. ×
命题突破
B 解析:中,只有次甲基上的碳原子为手性碳原子,A不符合题意;中,除醛基外的碳原子都为手性碳原子,B符合题意;中,除羧基外的碳原子都为手性碳原子,C不符合题意;中,与苯环相连的碳原子为手性碳原子,D不符合题意。
素养评估
1. D 解析:CaCl2、Na2O都是离子化合物,且都含有离子键,HI是共价化合物,只含有共价键,A错误;H2O、NH3都是共价化合物,都只含有共价键,NaNO3是离子化合物,含有离子键和共价键,B错误;MgCl2、NaOH、NH4Cl都是离子化合物,但MgCl2中只含有离子键,NaOH、NH4Cl中除了离子键还含有共价键,C错误;H2SO4、H2S、CO2都是共价化合物,都只含有共价键,D正确。故选D。
2. A 解析:NHeq \\al(+,4)中氮原子价层电子对数=4+eq \f(5-1-4×1,2)=4且不含孤电子对,所以该微粒为正四面体形,A正确;NOeq \\al(-,2)中N原子价层电子对数=2+eq \f(5-2×2+1,2)=3,则杂化方式为sp2,B错误;N2中N和N原子共用3对电子对,结构式为NN,C错误;H2O中含有2个O—H极性共价键,而不是非极性键,D错误。故选A。
3. C 解析:甲烷分子与水分子间不能形成氢键,A错误;“X—H…Y”三原子不在一条直线上时,也可能形成氢键,B错误;卤素单质随着摩尔质量的增大,分子间作用力增大,熔、沸点升高,碱金属单质的熔沸点随着摩尔质量的增大而降低,D错误。故选C。
4. C 解析:该分子中,碳原子所连接的四个基团只有两种,不含手性碳原子,A错误;该分子中,所有的碳原子所连接的四个基团都有一样的,故不含手性碳原子,B错误;该分子中,有一个碳原子所连的四个取代基分别是羟基、甲基、氢原子和羧基,该碳原子具有手性,C正确;该分子中,所有的碳原子所连接的四个基团中都有相同的,故不含手性碳原子,D错误。故选C。
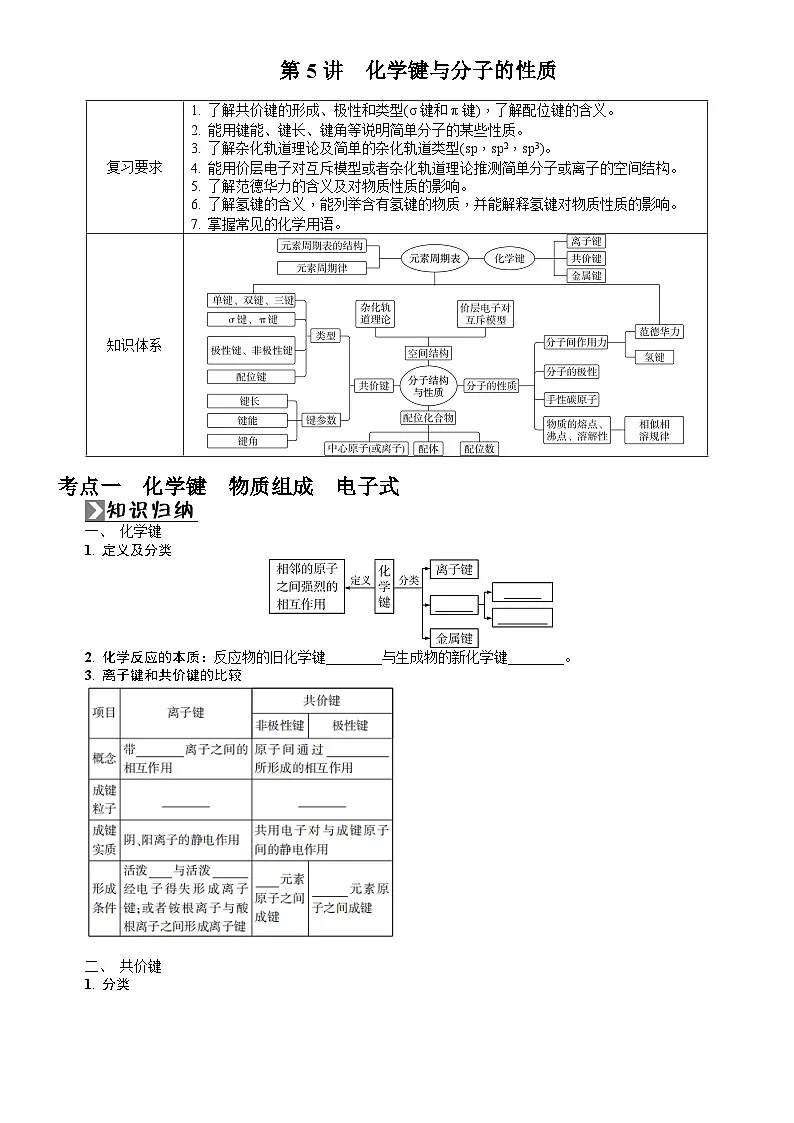
复习要求
1. 了解共价键的形成、极性和类型(σ键和π键),了解配位键的含义。
2. 能用键能、键长、键角等说明简单分子的某些性质。
3. 了解杂化轨道理论及简单的杂化轨道类型(sp,sp2,sp3)。
4. 能用价层电子对互斥模型或者杂化轨道理论推测简单分子或离子的空间结构。
5. 了解范德华力的含义及对物质性质的影响。
6. 了解氢键的含义,能列举含有氢键的物质,并能解释氢键对物质性质的影响。
7. 掌握常见的化学用语。
知识体系
项目
离子化合物
共价化合物
定义
由________构成的化合物
以________形成分子的化合物
构成微粒
________
________
化学键类型
一定含有______,可能含有______
只含有______
化合物类型
大多数金属氧化物、强碱、大多数盐
非金属氢化物、非金属氧化物、有机物(有机盐除外)
化合物性质
熔融状态能导电
熔融状态不能导电
杂化类型
杂化轨
道数目
杂化轨道
间夹角
空间结构
实例
sp
2
180°
____________
BeCl2
sp2
3
120°
____________
BF3
sp3
4
109°28′
____________
CH4
极性键
非极性键
成键原子
______元素的原子间
______元素的原子间
电子对
______偏移
(电荷分布不均匀)
______偏移
(电荷分布均匀)
成键原子
的电性
eq \(H,\s\up6(δ+))—Ceq \(l,\s\up6(δ-))
呈电中性
范德华力
氢键
概念
分子之间普遍存在的一种把分子聚集在一起的相互作用力
已经与电负性很大的原子形成共价键的氢原子与另一个电负性很大的原子之间的作用力
作用
微粒
分子或原子(稀有气体分子)
H与N、O、F等电负性很大的原子
分类
分子内氢键和分子间氢键
特征
__方向性和饱和性
__饱和性和方向性
强度
共价键>____>________
影响其
强度的
因素
①组成和结构相似的物质,相对分子质量越大,范德华力____;
②分子的极性____,范德华力越大
X—H…Y强弱与X和Y的电负性有关
对物质
性质的
影响
①组成和结构相似的物质,随着相对分子质量的增加,物质的熔、沸点升高。如熔、沸点:F2
相关学案 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 



.png)
.png)



