



所属成套资源:【同步教案】 苏教版(2019) 高中化学 必修一 教案
- 苏教版(2019)高中化学必修一教案:专题5 微观结构与物质的多样性 元素周期表 ( Word版含解析,2课时打包) 教案 1 次下载
- 苏教版(2019)高中化学必修一教案:专题5 微观结构与物质的多样性 同素异形现象 ( Word版含解析,2课时打包) 教案 1 次下载
- 苏教版(2019)高中化学必修一教案:专题5 微观结构与物质的多样性 离子键 ( Word版含解析,2课时打包) 教案 1 次下载
- 苏教版(2019)高中化学必修一教案:专题5 微观结构与物质的多样性 共价键 ( Word版含解析,2课时打包) 教案 1 次下载
- 苏教版(2019)高中化学必修一教案:第一单元 物质的分类( 2课时打包) 教案 2 次下载
苏教版(2019)高中化学必修一教案:专题5 微观结构与物质的多样性 晶体 非晶体 ( Word版含解析,2课时打包)
展开
这是一份2020-2021学年苏教版(2019)高中化学必修一教案:专题5 微观结构与物质的多样性 晶体 非晶体 ( Word版含解析,2课时打包),文件包含2020-2021学年苏教版2019高中化学必修一教案专题5微观结构与物质的多样性晶体非晶体2Word版含解析docx、2020-2021学年苏教版2019高中化学必修一教案专题5微观结构与物质的多样性晶体非晶体1Word版含解析docx等2份教案配套教学资源,其中教案共8页, 欢迎下载使用。
![]() 5.3.2 晶体 非晶体
5.3.2 晶体 非晶体![]() 本节内容是化学必修1专题五第三单元第2课时内容。在这第一节里让学生知道固体由晶体与非晶体之分,晶体与非晶体之间的本质差异,并通过实验进一步了解获得晶体的途径及鉴别方法使学生理解结构对物质性质的影响,提高分析问题和解决问题的能力。
本节内容是化学必修1专题五第三单元第2课时内容。在这第一节里让学生知道固体由晶体与非晶体之分,晶体与非晶体之间的本质差异,并通过实验进一步了解获得晶体的途径及鉴别方法使学生理解结构对物质性质的影响,提高分析问题和解决问题的能力。![]() 1、宏观辨识与微观探析:能依据物质的微观结构特征对物质进行分类;2、变化观念与平衡思想:能构建微观结构与物质多样性之间的联系;3、证据推理与模型认知:能解释或预测物质具有的一些典型性质。
1、宏观辨识与微观探析:能依据物质的微观结构特征对物质进行分类;2、变化观念与平衡思想:能构建微观结构与物质多样性之间的联系;3、证据推理与模型认知:能解释或预测物质具有的一些典型性质。![]() 1、熟知晶体的类型及其分类依据,学分判断晶体类型的方法2、知道晶体类型与物质性质的关系,会比较晶体的熔点、沸点
1、熟知晶体的类型及其分类依据,学分判断晶体类型的方法2、知道晶体类型与物质性质的关系,会比较晶体的熔点、沸点![]() 课件、相关图片、晶体模型
课件、相关图片、晶体模型![]() 引入新课:日常生活中我们遇到很多固态物质,常见的固态物质一般可分为晶体和非晶体,那么,什么样的固态物质属于晶体,构成微粒有哪些,有什么样的性质?什么样的固态物质属于非晶体,与晶体有哪些不同?今天这节课我们就来学习晶体和非晶体的知识。PPT展示:常见的晶体:石英、紫水晶、雪花、食盐、干冰和钻石等图片交流讨论:根据你所知道的相关晶体的知识,观察这些晶体在外观上有什么特点?它们的物理性质(如硬度、熔点、沸点、导电性等)有什么特点?讲解:这些晶体都有规则的几何外形,但性质有很大的差异。用X射线进行晶体的衍射实验时发现,在晶体内部,构成晶体的微粒在空间呈有规则的重复排列。晶体规则的几何外形是其内部构成微粒有规则排列的结果。晶体有固定的熔、沸点,构成微粒有原子、分子、离子。板书:一、晶体1、定义:具有规则几何外形的固体2、构成微粒:原子、分子、离子讲解:根据晶体的组成微粒的不同,把晶体分成了离子晶体、分子晶体、原子晶体和金属晶体。下面我们就分别来学习晶体的知识。板书:1、离子晶体PPT展示:氯化钠晶体,学生观察,并思考下列问题(1)氯化钠属于哪一类化合物,其晶体中有没有单个氯化钠分子?(2)组成微粒是什么,微粒间有什么作用力?(3)离子晶体物理性质有什么特点板书:(1)定义:阴、阳离子按一定方式有规则地排列形成的晶体叫作离子晶体。(2)微粒:阴、阳离子,(3)微粒间作用力:离子键(4)物理性质:熔沸点较高,硬度较大。水溶液或者熔融状态下均导电。提问:哪些类别的物质属于离子晶体呢?板书:(5)判断:强碱、部分金属氧化物、部分盐类思考:二氧化碳,在常温和压强为6079.8千帕压力下,冷凝成无色的液体,再在低压下迅速蒸发,便凝结成一块块冰雪状固体物质,其温度是零下78.5℃,即干冰.干冰也是一种晶体,那么组成微粒是什么,微粒间有什么样的作用力,有哪些性质呢?PPT展示:干冰及其模型板书:2、分子晶体(1)定义:由分子构成的物质所形成的晶体属于分子晶体(2)微粒:分子(3)作用力:分子间作用力(或范德华力)(4)物理性质:分子间的作用力很弱,分子晶体具有较低的熔点、沸点,硬度小、易挥发,许多物质在常温下呈气态或液态。讲解:同类型分子的晶体,其熔、沸点随分子量的增加而升高。例如卤素单质的熔、沸点按F2、Cl2、Br2、I2顺序递增;但HF、H2O、NH3、CH3CH2OH等分子间,除存在范德华力外,还有氢键的作用力,它们的熔沸点较高。在固态和熔融状态时都不导电。PPT展示:水晶、紫水晶、钻石(金刚石)的图片,思考下面问题水晶、紫水晶和钻石(金刚石)的主要成分都是二氧化硅,钻石(金刚石)的成分是碳,这些固体物质硬度都很大,熔、沸点很高,不同于离子晶体和分子晶体,那么,这些固体又属于哪一类晶体,组成微粒是什么,微粒间的作用力是怎么样的呢?板书:3、原子晶体(1)定义:相邻原子之间只通过强烈的共价键结合而成的空间网状结构的晶体叫做原子晶体。(2)微粒:原子(可以是同种原子,也可以是不同种原子)(3)作用力:共价键讲解:在SiO2晶体中,1个硅原子和4个氧原子形成4个共价键,每个硅原子周围结合4个氧原子;同时,每个氧原子跟2个硅原子相结合:实际上,SiO2晶体是由硅原子和氧原子按1:2的比例所组成的立体网状的晶体:金刚石晶体中每个碳原子与相邻的四个碳原子以共价健结合,形成空间网状结构。(4)物理性质:高熔点、沸点和硬度,在通常情况下不导电,热的不良导体。原子晶体不导电、不易溶于任何溶剂,化学性质十分稳定。讲解:常见的原子晶体有:晶体硅、二氧化硅、碳化硅、金刚石等过度:还有一类晶体,是由金属原子构成的,我们称之为金属晶体。板书:4、金属晶体(1)定义:金属原子通过金属键形成的晶体称为金属晶体(2)微粒:金属原子(3)作用力:金属键(4)物理性质:容易导电、导热、有延展性、有金属光泽;熔沸点差距很大。PPT展示:1、离子晶体、分子晶体、原子晶体的比较2、(1)晶体类型判断方法:①分析微粒种类:离子、分子、原子。②微粒间的相互作用力:离子键、分子间作用力、共价键、金属键。(2)物质类别与晶体类型①离子化合物(强碱和大多数盐)都是离子晶体;②共价分子(单质或化合物)是分子晶体;③常见的原子晶体,如二氧化硅、碳化硅、金刚石、晶体硅等。板书:二、非晶体1、定义:内部原子或分子的排列呈现杂乱无章的分布状态的固体物质。2、结构特点:没有一定规则的外形。3、物理性质:没有固定的熔点
引入新课:日常生活中我们遇到很多固态物质,常见的固态物质一般可分为晶体和非晶体,那么,什么样的固态物质属于晶体,构成微粒有哪些,有什么样的性质?什么样的固态物质属于非晶体,与晶体有哪些不同?今天这节课我们就来学习晶体和非晶体的知识。PPT展示:常见的晶体:石英、紫水晶、雪花、食盐、干冰和钻石等图片交流讨论:根据你所知道的相关晶体的知识,观察这些晶体在外观上有什么特点?它们的物理性质(如硬度、熔点、沸点、导电性等)有什么特点?讲解:这些晶体都有规则的几何外形,但性质有很大的差异。用X射线进行晶体的衍射实验时发现,在晶体内部,构成晶体的微粒在空间呈有规则的重复排列。晶体规则的几何外形是其内部构成微粒有规则排列的结果。晶体有固定的熔、沸点,构成微粒有原子、分子、离子。板书:一、晶体1、定义:具有规则几何外形的固体2、构成微粒:原子、分子、离子讲解:根据晶体的组成微粒的不同,把晶体分成了离子晶体、分子晶体、原子晶体和金属晶体。下面我们就分别来学习晶体的知识。板书:1、离子晶体PPT展示:氯化钠晶体,学生观察,并思考下列问题(1)氯化钠属于哪一类化合物,其晶体中有没有单个氯化钠分子?(2)组成微粒是什么,微粒间有什么作用力?(3)离子晶体物理性质有什么特点板书:(1)定义:阴、阳离子按一定方式有规则地排列形成的晶体叫作离子晶体。(2)微粒:阴、阳离子,(3)微粒间作用力:离子键(4)物理性质:熔沸点较高,硬度较大。水溶液或者熔融状态下均导电。提问:哪些类别的物质属于离子晶体呢?板书:(5)判断:强碱、部分金属氧化物、部分盐类思考:二氧化碳,在常温和压强为6079.8千帕压力下,冷凝成无色的液体,再在低压下迅速蒸发,便凝结成一块块冰雪状固体物质,其温度是零下78.5℃,即干冰.干冰也是一种晶体,那么组成微粒是什么,微粒间有什么样的作用力,有哪些性质呢?PPT展示:干冰及其模型板书:2、分子晶体(1)定义:由分子构成的物质所形成的晶体属于分子晶体(2)微粒:分子(3)作用力:分子间作用力(或范德华力)(4)物理性质:分子间的作用力很弱,分子晶体具有较低的熔点、沸点,硬度小、易挥发,许多物质在常温下呈气态或液态。讲解:同类型分子的晶体,其熔、沸点随分子量的增加而升高。例如卤素单质的熔、沸点按F2、Cl2、Br2、I2顺序递增;但HF、H2O、NH3、CH3CH2OH等分子间,除存在范德华力外,还有氢键的作用力,它们的熔沸点较高。在固态和熔融状态时都不导电。PPT展示:水晶、紫水晶、钻石(金刚石)的图片,思考下面问题水晶、紫水晶和钻石(金刚石)的主要成分都是二氧化硅,钻石(金刚石)的成分是碳,这些固体物质硬度都很大,熔、沸点很高,不同于离子晶体和分子晶体,那么,这些固体又属于哪一类晶体,组成微粒是什么,微粒间的作用力是怎么样的呢?板书:3、原子晶体(1)定义:相邻原子之间只通过强烈的共价键结合而成的空间网状结构的晶体叫做原子晶体。(2)微粒:原子(可以是同种原子,也可以是不同种原子)(3)作用力:共价键讲解:在SiO2晶体中,1个硅原子和4个氧原子形成4个共价键,每个硅原子周围结合4个氧原子;同时,每个氧原子跟2个硅原子相结合:实际上,SiO2晶体是由硅原子和氧原子按1:2的比例所组成的立体网状的晶体:金刚石晶体中每个碳原子与相邻的四个碳原子以共价健结合,形成空间网状结构。(4)物理性质:高熔点、沸点和硬度,在通常情况下不导电,热的不良导体。原子晶体不导电、不易溶于任何溶剂,化学性质十分稳定。讲解:常见的原子晶体有:晶体硅、二氧化硅、碳化硅、金刚石等过度:还有一类晶体,是由金属原子构成的,我们称之为金属晶体。板书:4、金属晶体(1)定义:金属原子通过金属键形成的晶体称为金属晶体(2)微粒:金属原子(3)作用力:金属键(4)物理性质:容易导电、导热、有延展性、有金属光泽;熔沸点差距很大。PPT展示:1、离子晶体、分子晶体、原子晶体的比较2、(1)晶体类型判断方法:①分析微粒种类:离子、分子、原子。②微粒间的相互作用力:离子键、分子间作用力、共价键、金属键。(2)物质类别与晶体类型①离子化合物(强碱和大多数盐)都是离子晶体;②共价分子(单质或化合物)是分子晶体;③常见的原子晶体,如二氧化硅、碳化硅、金刚石、晶体硅等。板书:二、非晶体1、定义:内部原子或分子的排列呈现杂乱无章的分布状态的固体物质。2、结构特点:没有一定规则的外形。3、物理性质:没有固定的熔点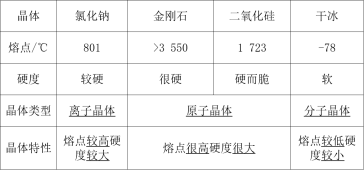 4、举例:石蜡、玻璃、橡胶、松香、沥青等。PPT展示:课堂练习
4、举例:石蜡、玻璃、橡胶、松香、沥青等。PPT展示:课堂练习![]() 本节课主要按“定义、构成微粒、微粒间作用力、物理性质”四个方面学习了晶体的相关知识,系统学习了离子晶体、分子晶体、原子晶体和金属晶体,使学生从微观结构层面上加深了对晶体的认识,有助于学生今后从微观结构上进一步学习有关物质。
本节课主要按“定义、构成微粒、微粒间作用力、物理性质”四个方面学习了晶体的相关知识,系统学习了离子晶体、分子晶体、原子晶体和金属晶体,使学生从微观结构层面上加深了对晶体的认识,有助于学生今后从微观结构上进一步学习有关物质。






