
初中化学人教版 (五四制)九年级全册课题2 溶解度教学设计
展开教材分析
第九单元《溶液》共划分为三个课题。本课属于课题2《溶解度》第二课时的教学内容。本课是在学生对溶液的组成、基本特征有了初步认识,知道结晶现象,能区分饱和溶液和不饱和溶液,并初步了解两者之间相互转化的方法基础上的再学习。溶解度的概念的学习将使学生对溶液的认识从定性认识转向定量分析,并为判断溶液是否饱和、饱和溶液和不饱和溶液的相互转化、结晶方法的选择等提供了较好的数据分析支撑,可以帮助学生初步形成运用定量数据分析指导定性化学实验的观念。
学情分析
九年级学生思维活跃,获取信息的途径多样,喜欢将所学知识和已有经验、生活实际相联系,愿意表达自己的观点。同时,通过课题1和课题2第一课时的学习,学生已经知道在一定温度下,固体物质在一定量的水中是不能无限溶解的,都有一个最大值,最终会达到饱和状态。但学生还没有意识到当温度一定时,某物质的饱和溶液的组成是固定不变的,物质在水中的溶解限度是一定的;更不知道如何准确地比较不同物质溶解性的差异,从定量的角度去认识物质的溶解性以及溶液的种种状态也很少思考。教学中通过创设情境、提出问题,引发学生思考,使学生认识到自己经验的不足,从而激发他们的学习热情。
教学目标
知识与技能
1、正确认识固体物质溶解度的概念。
2、知道溶解度曲线的变化规律和含义。
过程与方法
1、初步学会列表法、作图法等常用数据处理方法。
2、通过简单的探究活动,增进对概念的理解和方法的运用。
情感态度价值观
1、引发学生思考,增强对化学的好奇心和学习兴趣。
2、体会化学学习与生活实际的紧密联系。
重点难点
重点:认识固体的溶解度概念
难点:认识固体的溶解度概念、溶解度曲线的变化规律及运用
教法学法
教法:情景设疑、体验探究、问题启导、知识建构。
学法:小组合作、共享交流、自主探究、反思悟法。
教学过程
板书设计
教学环节
教师活动
学生活动
设计意图
创设情景
【动图】运动员的田径比赛。
【问题】田径比赛如何比出冠军?
记录学生回答的方法
观看动图
分析得出:
条件一:同一开始时间
条件二:同一跑道
条件三:同一距离
测 量:完成时间
借助学生熟悉的运动,迅速吸引学生注意力,从而激发他们的学习热情,体会控制变量方法的应用。
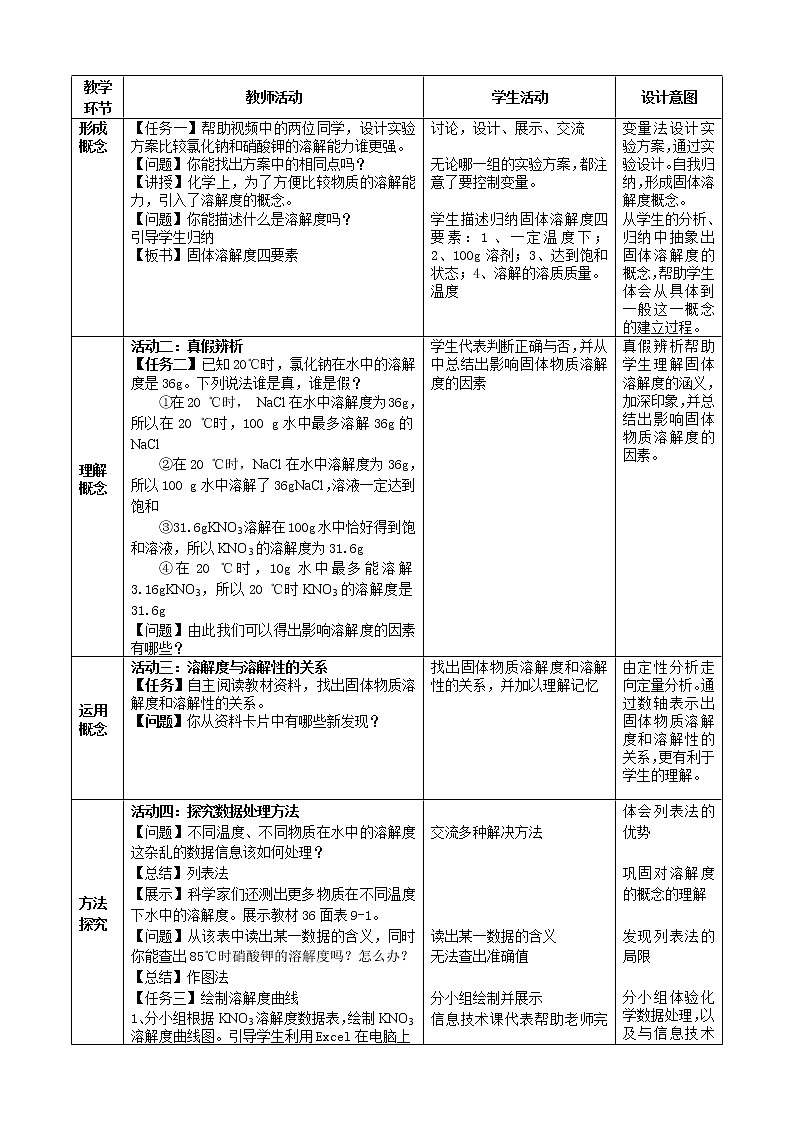
形成概念
活动一:比较溶解能力
【任务一】帮助视频中的两位同学,设计实验方案比较氯化钠和硝酸钾的溶解能力谁更强。
【问题】你能找出方案中的相同点吗?
【讲授】化学上,为了方便比较物质的溶解能力,引入了溶解度的概念。
【问题】你能描述什么是溶解度吗?
引导学生归纳
【板书】固体溶解度四要素
讨论,设计、展示、交流
无论哪一组的实验方案,都注意了要控制变量。
学生描述归纳固体溶解度四要素:1、一定温度下; 2、100g溶剂;3、达到饱和状态;4、溶解的溶质质量。
温度
自主利用控制变量法设计实验方案,通过实验设计。自我归纳,形成固体溶解度概念。
从学生的分析、归纳中抽象出固体溶解度的概念,帮助学生体会从具体到一般这一概念的建立过程。
理解
概念
活动二:真假辨析
【任务二】已知20℃时,氯化钠在水中的溶解度是36g。下列说法谁是真,谁是假?
①在20 ℃时, NaCl在水中溶解度为36g,所以在20 ℃时,100 g水中最多溶解36g的NaCl
②在20 ℃时,NaCl在水中溶解度为36g,所以100 g水中溶解了36gNaCl,溶液一定达到饱和
③31.6gKNO3溶解在100g水中恰好得到饱和溶液,所以KNO3的溶解度为31.6g
④在20 ℃时,10g水中最多能溶解3.16gKNO3,所以20 ℃时KNO3的溶解度是31.6g
【问题】由此我们可以得出影响溶解度的因素有哪些?
学生代表判断正确与否,并从中总结出影响固体物质溶解度的因素
真假辨析帮助学生理解固体溶解度的涵义,加深印象,并总结出影响固体物质溶解度的因素。
运用概念
活动三:溶解度与溶解性的关系
【任务】自主阅读教材资料,找出固体物质溶解度和溶解性的关系。
【问题】你从资料卡片中有哪些新发现?
找出固体物质溶解度和溶解性的关系,并加以理解记忆
由定性分析走向定量分析。通过数轴表示出固体物质溶解度和溶解性的关系,更有利于学生的理解。
方法
探究
活动四:探究数据处理方法
【问题】不同温度、不同物质在水中的溶解度这杂乱的数据信息该如何处理?
【总结】列表法
【展示】科学家们还测出更多物质在不同温度下水中的溶解度。展示教材36面表9-1。
【问题】从该表中读出某一数据的含义,同时你能查出85℃时硝酸钾的溶解度吗?怎么办?
【总结】作图法
【任务三】绘制溶解度曲线
1、分小组根据KNO3溶解度数据表,绘制KNO3溶解度曲线图。引导学生利用Excel在电脑上
交流多种解决方法
读出某一数据的含义
无法查出准确值
分小组绘制并展示
信息技术课代表帮助老师完成利用Excel在电脑上绘制KNO3的溶解度曲线。
体会列表法的优势
巩固对溶解度的概念的理解
发现列表法的局限
分小组体验化学数据处理,以及与信息技术的紧密联系。
方法
探究
绘制KNO3的溶解度曲线。
2、根据所绘制的KNO3溶解度曲线,找出85℃时,KNO3的溶解度。
【任务四】获取溶解度曲线相关信息
【问题1】根据你绘制的溶解度曲线图,判断溶液在曲线上的点A、曲线下方的点B、曲线上方的点C的状态。
【问题2】溶解度曲线中两条线交点有何含义?
【问题3】观察两组溶解度曲线图片,溶解度随温度变化有何规律?
【任务五】讨论:两种溶解度的表示方法有什么不同?
根据所绘制的KNO3溶解度曲查出85℃时硝酸钾的溶解度
交流得出溶液在曲线上的点A、曲线下方的点B、曲线上方的点C的状态
60℃时,a,b两物质的溶解度相等,均为52g
总结出:大多数固体物质在水中的溶解度随温度升高增大,且有一部变化显著,有一部分不明显,极少数固体物质,如氢氧化钙随温度升高而减小。
小组交流谈论两种溶解度的表示方法的特点
挖掘图、表等信息的不同表达方式背后的新知,真正找到图表背后的新知,提升获取、分析、转换信息的能力
方法
运用
活动五:溶解度曲线的应用
氯化钠
【问题1】要使硝酸钾从其饱和溶液中析出晶体,最好用什么方法?为什么?
【问题2】海水晒盐用的什么方法?为什么?
【问题3】如图硝酸钾固体中含有少量氯化钠,提纯硝酸钾流程图,你能说出该方法的原理吗?
聆听、溶解度曲线判断
硝酸钾的溶解度随温度变化较大,采用降温结晶容易获得硝酸钾
氯化钠的溶解度随温度变化较缓慢,降温析出晶体少,故采用蒸发溶剂的方法获得晶体。
联系实际,类比解释
检验方法是否掌握的最佳方式就是运用方法,让学生在有意义的方法运用中实现能力的提升。
总结反馈
进行交流总结,分享本节课的收获
建立本节课知识间的知识网络,条理性的感受本节课的重难点,学会归纳总结、
§9、2 溶解度(2)
固体的溶解度
一、定义要素
1、一定温度
2、100g溶剂
3、达到饱和状态
4、溶解的溶质质量
二、影响因素
1、内因:溶质和溶剂种类
2、外因:温度
三、数据处理
1、溶解度曲线
2、溶解度数据表
溶解度方案设计关键词:
xx℃
等量的水
饱和状态
溶质的质量等
通过描绘的溶解度曲线读出85℃硝酸钾溶解度
第一组
第二组
第三组
第四组
第五组
初中化学人教版 (五四制)九年级全册课题2 溶解度教学设计: 这是一份初中化学人教版 (五四制)九年级全册课题2 溶解度教学设计,共2页。教案主要包含了实验探究,点拨总结,溶解度定义,投影展示,跟踪训练,交流讨论,巩固练习,梳理所学,盘点收获等内容,欢迎下载使用。
人教版 (五四制)九年级全册课题2 溶解度教案: 这是一份人教版 (五四制)九年级全册课题2 溶解度教案,共2页。教案主要包含了导入新课,授课等内容,欢迎下载使用。
初中化学人教版 (五四制)九年级全册课题2 溶解度教案: 这是一份初中化学人教版 (五四制)九年级全册课题2 溶解度教案,共1页。













