






初中化学人教版九年级下册第九单元 溶液课题3 溶液的浓度课文课件ppt
展开
这是一份初中化学人教版九年级下册第九单元 溶液课题3 溶液的浓度课文课件ppt,共18页。PPT课件主要包含了溶质的质量分数,固体溶质,稀释与浓缩问题,混合溶液问题等内容,欢迎下载使用。
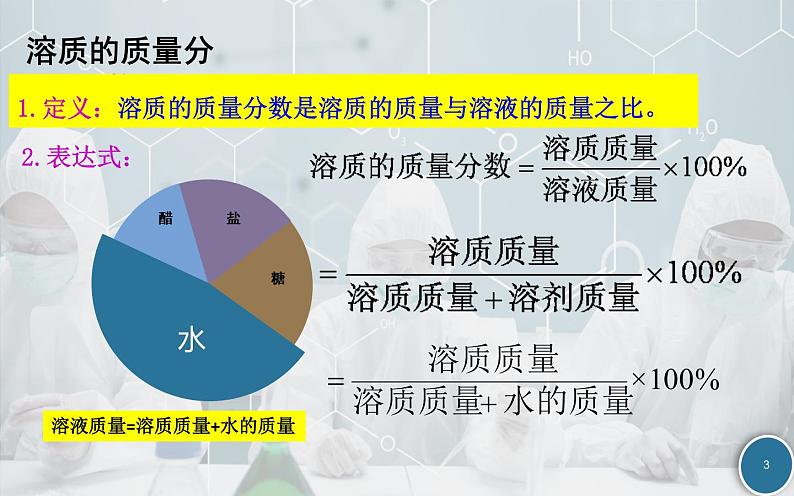
1.定义:溶质的质量分数是溶质的质量与溶液的质量之比。
溶液质量=溶质质量+水的质量
溶剂水=溶液质量-溶质质量=50g-4.5g=45.5g
例1.配制50g质量分数为9%的氯化钠溶液,所需氯化钠固体的质量为 g;水质量为 g。
设:溶质氯化钠的质量为X。
1)氯化钠的质量分数=
练1.已知50g氯化钠溶液中含5g氯化钠,计算:1)该溶液中质量分数?2)再加50g水后,质量分数?
2)加水后的质量分数=
变形:溶质质量=溶液质量×质量分数
原理:稀释溶液的过程中,溶质的质量不会发生变化。
水的质量=稀溶液质量-浓溶液质量
m浓×浓%=m稀×稀%
溶质质量=浓溶液质量×浓溶液的质量分数 =稀溶液质量×稀溶液的质量分数
例2.用9%的氯化钠溶液配制50g质量分数为0.9%的氯化钠溶液,所需浓溶液的质量为 g;水质量为 g。
m浓×9%=50g×0.9%
m浓×98%=100g×4.9%
m水=m稀-m浓=100g-5g=95g
例3现有100g溶质质量分数为10%的食盐溶液,若使溶液的浓缩变为20%,此溶液蒸发掉水 g.
m浓×20%=100g×10%
m水=m稀-m浓 =100g-50g =50g
原理:加热浓缩溶液的过程中,溶质的质量不会发生变化。
蒸发水的质量=稀溶液质量-浓溶液质量
练习3:把200g18%的氯化钠溶液浓缩到72%,需要蒸发掉 水?
m浓×72%=200g×18%
m水=m稀-m浓 =200g-50g=150g
例4.60克60%NaOH溶液与40克40%NaOH溶液混合,求溶质的质量分数。
3.溶质质量分数不同的两种溶液的混合
M浓×a浓% + M稀×b稀% =(M浓+M稀)×C混%
60g×60%+40g×40%=(60+40)×混%
36g +16g =100×混%52g =100×混%混%=52%
练习4:将100g15%该溶液与100g5%的过氧乙酸溶液混合,所得溶液的质量分数为_____。
公式M浓×a%浓 + M稀×b%稀 =(M浓+M稀)× c混%
100g×15%+100g×5%=(100+100)×混%
20g =200×混%
15g +5g =200×混%
总结:溶质的质量分数计算
水的质量=浓溶液质量-稀溶液质量
原理:溶解、稀释、浓缩、浓稀混合过程中,溶质质量都不会发生变化。
1.过氧乙酸是一种常用的消毒剂。现有一种过氧乙酸溶液,其溶质质量分数为15%。请填空:
⑴100g该溶液中含溶质________g。
⑵将100g20%该溶液与100g40%的消毒溶液混合,所得溶液的溶质质量分数为_____。
2.化学实验室现有98%的浓硫酸,把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸。需水的质量为________。
3.把200g18%的氯化钠溶液浓缩到36%,需要蒸发掉_______克水?
相关课件
这是一份初中人教版课题3 溶液的浓度教学演示课件ppt,共27页。PPT课件主要包含了各加入20ml水,比较颜色,浅蓝色--→深蓝色,稀----→浓,发现什么,葡萄糖注射液的浓度,溶质的质量分数,计算公式,注意公式推导,溶质质量分数的含义等内容,欢迎下载使用。
这是一份人教版九年级下册课题3 溶液的浓度一等奖ppt课件,共33页。PPT课件主要包含了新课导入,颜色的深浅,溶液的浓度,溶质的质量分数,一溶质的质量分数,X=150g,溶液稀释问题的计算,x50g,溶液浓缩的计算,x196g等内容,欢迎下载使用。
这是一份初中化学人教版九年级下册课题1 常见的酸和碱说课课件ppt,共19页。PPT课件主要包含了第十单元,酸和碱,常见的碱,碱的化学性质,⒈碱与指示剂反应,想看看吗,神奇吧,总结碱的化学性质,跟指示剂的反应,课堂练习等内容,欢迎下载使用。









