

四川省内江市第一中学2024-2025学年高一下学期3月月考 化学试题(原卷版+解析版)
展开 这是一份四川省内江市第一中学2024-2025学年高一下学期3月月考 化学试题(原卷版+解析版),共23页。试卷主要包含了 下列反应的离子方程式正确的是等内容,欢迎下载使用。
一、单选题(每题3分,共45分)
1. 下列关于化学在生活中应用的说法,正确的是
A. 纯碱和小苏打都可用于制发酵粉,它们分别属于碱和盐
B. 河水中有许多杂质和有害细菌,加入明矾后即可饮用
C. “84”消毒液和洁厕灵混合使用会发生氧化还原反应而使消毒能力增强
D. 饮用的葡萄酒中要含有一定量的SO2是为了除产生的杂菌及防止其被氧化
2. 下列有关物质分类或归类不正确的是
A. 混合物:漂白粉、氯水、空气B. 酸性氧化物:、、
C. 同素异形体:、金刚石、石墨D. 电解质:、、
3. 医学界通过标记的发现了一种的羧酸衍生物,这种羧酸衍生物在特定条件下可以通过断裂DNA抑制艾滋病毒的繁殖。下列有关的说法正确的是
A. 与互为同位素B. 原子核内中子数为6
C. 、、属于不同的核素D. 、互为同素异形体
4. 下列物质中既含有离子键又含有共价键的是
A. B. C. D.
5. 化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是
A. 用电子式表示水分子的形成过程:
B. 中子数为10的氧原子:
C. CO2的电子式:
D. 铵根离子结构式:
6. 在下列条件的溶液中,一定能大量共存的离子组是
A. 无色溶液:Ca2+、H+、Fe2+、
B. 常温下使石蕊试液变蓝的溶液:Na+、K+、、
C. 澄清透明溶液:K+、Cu2+、、OH-
D. 加入铁粉放出H2的溶液:K+、Ba2+、、Fe3+
7. 硫和氮都是化工生产中重要的非金属元素。已知NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4LSO3中含有SO3分子数为NA
B. 1mlNH3和1ml,含有的电子数均为10NA
C. 足量Cu与含2mlH2SO4的浓硫酸共热反应,生成SO2(标准状况)的体积为22.4L
D. 1mlN2与足量H2充分反应,转移电子数为6NA
8. 根据下列实验事实或现象,解释合理的是
A. 把SO2通入滴有酚酞的氢氧化钠溶液中,溶液的红色褪去,是因为SO2具有漂白性
B. 把酸雨样品在空气中露置一段时间后,测得溶液酸性增强,是因为溶解了更多CO2
C. 把氨气通入滴有几滴酚酞的水中,溶液变红,是因为氨气电离出氢氧根离子显碱性
D. 向SO2水溶液中加入NaHCO3粉末,有气泡产生,说明H2SO3酸性强于H2CO3
9. 下列反应的离子方程式正确的是
A. 将过量的铁粉加入稀硝酸中:Fe+4H++=Fe3++NO↑+2H2O
B. 钠与CuSO4溶液反应:2Na+Cu2+═Cu+2Na+
C. 向碳酸氢铵溶液中加入过量的NaOH溶液:+OH﹣=H2O+
D. 向AlCl3溶液中加入氨水至过量:Al3++3NH3·H2O═Al(OH)3↓+3NH
10. 氨广泛应用于化工、化肥、制药等领域,一种新型制备氨的方法如图。下列说法错误的是
A. 反应①属于氮的固定
B. 反应②属于氧化还原反应
C. 反应⑤在无水环境中进行时,有白烟产生
D. 该转化过程总反应的反应物是N2和H2O,产物是NH3和O2
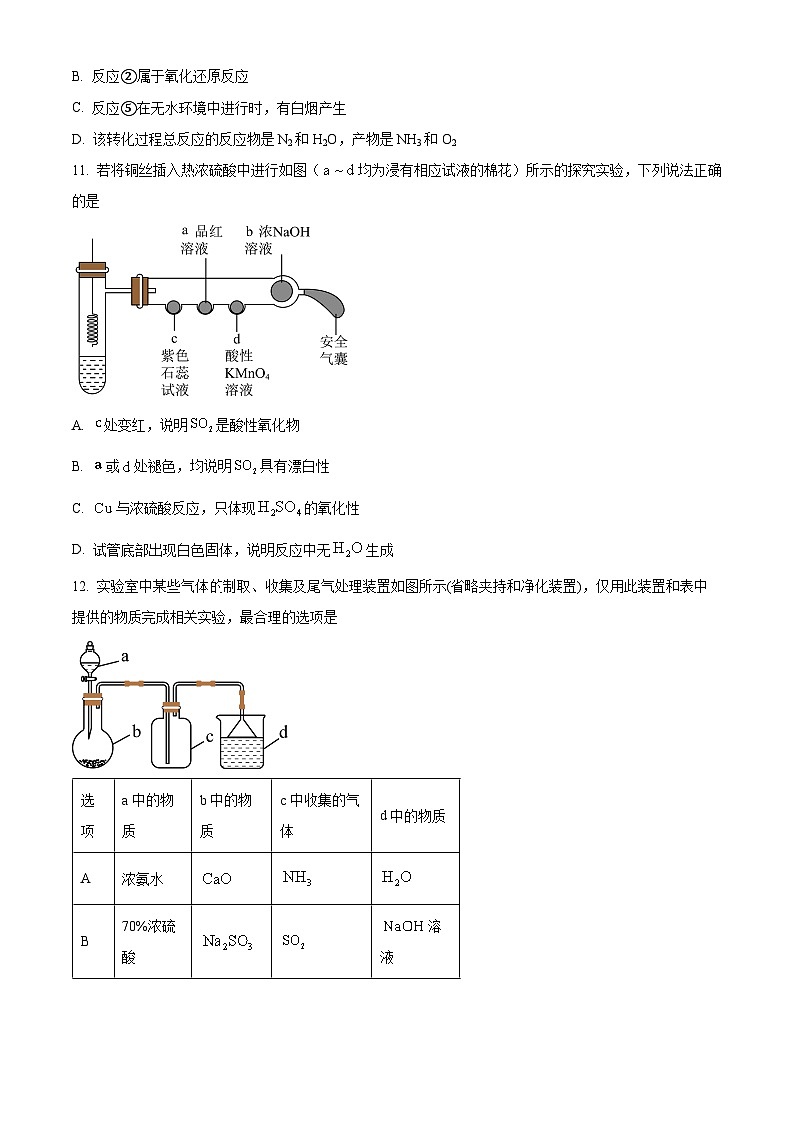
11. 若将铜丝插入热浓硫酸中进行如图(均为浸有相应试液的棉花)所示的探究实验,下列说法正确的是
A. 处变红,说明是酸性氧化物
B. 或处褪色,均说明具有漂白性
C. 与浓硫酸反应,只体现的氧化性
D. 试管底部出现白色固体,说明反应中无生成
12. 实验室中某些气体制取、收集及尾气处理装置如图所示(省略夹持和净化装置),仅用此装置和表中提供的物质完成相关实验,最合理的选项是
A. AB. BC. CD. D
13. 下列反应必须加入氧化剂且一步反应就能完成的是
① ② ③ ④ ⑤
A. ①②③④B. ②③④C. ④D. ③④
14. “价—类”二维图是研究物质性质的一种方法,图中a~f表示的均是含硫物质。下列说法正确的是
A. a可用硫化亚铁与稀硝酸反应制取
B. 可发生反应:(未配平)
C. c能使溴水褪色,证明c有漂白性
D. f既有氧化性又有还原性
15. 下表是元素周期表的一部分,W、X、Y、Z为短周期主族元素,X的最外层电子数等于电子层数,下列说法不正确的是
A. 原子半径:WH2TeO4
C.向硫化氢溶液中通入氧气可能会发生:O2 + 2H2S = 2S↓ + 2H2O
D.沸点:H2O>H2S
E.氢化物的稳定性:H2O>H2S>H2Se>H2Te
17. 高铁酸钾(化学式:)是一种暗紫色固体,具有强氧化性。在强碱性溶液中稳定,易溶于水,微溶于浓KOH溶液,难溶于异丙醇(一种有机溶剂),在生活中常被用作水处理剂。某兴趣小组利用废铁屑(含少量杂质)制备高铁酸钾的工艺流程如图所示:
回答下列问题:
(1)中铁元素的化合价为_____,“氧化Ⅰ”反应的还原产物为_____。
(2)已知“转化”为复分解反应,“氧化Ⅱ”中NaClO被还原为NaCl,则“氧化Ⅱ”反应的离子方程式为_____。
(3)晶体“洗涤”时,洗涤剂最好选用_____(填字母序号)。
A. B. NaOH溶液C. 异丙醇D. 稀盐酸
(4)若晶体未洗涤干净,含有的杂质阴离子为_____。
(5)另一种制备的原理为:
①请用单线桥法表示出电子转移情况_____
②由该反应可知,氧化性:_____(填“>”或“H2Te
【答案】(1)第三周期第IVA族
(2) (3) (4)Cl- > O2 - > Na+ > Al3+
(5)黄 (6)Al2O3 +2OH- +3H2O=2[Al(OH)4]-
(7)2Rb2O2+2H2O=4RbOH+O2↑
(8)ABCE
【解析】
【分析】由各元素在周期表的位置可知,①为H、②为C、③为N、④为O、⑤为Na、⑥为Al、⑦为S、⑧为Cl、⑨为K、⑩为Se;
【小问1详解】
硅元素的原子序数为14,其在周期表中的位置为:第三周期第IVA族;
【小问2详解】
元素⑨为K,K的原子序数为19,其原子结构示意图为;
【小问3详解】
元素①、②分别为H、C,H、C形成的10电子分子为CH4,其电子式为;
【小问4详解】
元素④、⑤、⑥、⑧分别为O、Na、Al、Cl,一般电子层数越多离子半径越大,四种离子中Cl-的半径最大,O2-、Na+、Al3+均为10电子微粒,具有相同的电子层结构,核电荷数越大、离子半径越小,离子半径由大到小的顺序是Cl- > O2 - > Na+ > Al3+;
【小问5详解】
元素⑤和元素⑧分别为Na、Cl,形成的化合物NaCl,含钠元素的物质高温灼烧时,火焰呈黄色;
【小问6详解】
⑥的氧化物和⑤最高价氧化物的水化物分别为Al2O3、NaOH,Al2O3为两性氧化物,能和氢氧化钠溶液反应,反应的离子方程式为:Al2O3 +2OH- +3H2O=2[Al(OH)4]-;
【小问7详解】
已知2Na2O2+2H2O=4NaOH+O2↑,铷(Rb)位于IA族,Rb2O2与水能剧烈反应并释放出O2,则其化学方程式为:2Rb2O2+2H2O=4RbOH+O2↑;
【小问8详解】
A.元素的非金属性越强,单质的氧化性越强,与氢气化合物越容易,则氧、硫、硒(Se)、锑(Te)的单质和氢气化合越来越难,甚至Te和氢气不直接化合可以由非金属性强弱的变化规律来推测,故A符合题意;
B.元素的非金属性越强,最高价氧化物的水化物的酸性越强,酸性:H2SO4>H2SeO4>H2TeO4可以由非金属性强弱的变化规律来推测,故B符合题意;
C.元素的非金属性越强,单质的氧化性越强,氧气的氧化性强于硫,向硫化氢溶液中通入氧气可能会发生:O2 + 2H2S = 2S↓ + 2H2O,故C符合题意;
D.水的沸点高于硫化氢是因为水分子之间存在氢键,沸点:H2O>H2S不可以由非金属性强弱的变化规律来推测,故D不符合题意;
E.元素的非金属性越强,简单氢化物越稳定,氢化物的稳定性:H2O>H2S>H2Se>H2Te可以由非金属性强弱的变化规律来推测,故E符合题意;
故答案为:ABCE。
17. 高铁酸钾(化学式:)是一种暗紫色固体,具有强氧化性。在强碱性溶液中稳定,易溶于水,微溶于浓KOH溶液,难溶于异丙醇(一种有机溶剂),在生活中常被用作水处理剂。某兴趣小组利用废铁屑(含少量杂质)制备高铁酸钾的工艺流程如图所示:
回答下列问题:
(1)中铁元素的化合价为_____,“氧化Ⅰ”反应的还原产物为_____。
(2)已知“转化”为复分解反应,“氧化Ⅱ”中NaClO被还原为NaCl,则“氧化Ⅱ”反应的离子方程式为_____。
(3)晶体“洗涤”时,洗涤剂最好选用_____(填字母序号)。
A. B. NaOH溶液C. 异丙醇D. 稀盐酸
(4)若晶体未洗涤干净,含有杂质阴离子为_____。
(5)另一种制备的原理为:
①请用单线桥法表示出电子转移情况_____。
②由该反应可知,氧化性:_____(填“>”或“
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)





