
湖南省郴州市2024-2025学年高三上学期第一次教学质量监测(一模)化学试卷(Word版附答案)
展开这是一份湖南省郴州市2024-2025学年高三上学期第一次教学质量监测(一模)化学试卷(Word版附答案),文件包含湖南省湘东十校2024-2025学年高三上学期10月联考地理试题Word版含解析docx、湖南省湘东十校2024-2025学年高三上学期10月联考地理试题Word版无答案docx等2份试卷配套教学资源,其中试卷共22页, 欢迎下载使用。
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
4.考试时间为75分钟,满分为100分。
5.本试题卷共9页。如缺页,考生须声明,否则后果自负。
姓名________________ 准考证号________________
郴州市2025届高三第一次教学质量监测试卷
化 学
可能用到的相对原子质量:H:1 B:11 C:12 N:14 O:16 S:32 Fe:56
一、选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。)
1.中国“天宫”空间站运用的“黑科技”很多,下列对所涉及物质的性质描述错误的是( )
A.被誉为“百变金刚”的太空机械臂主要成分为铝合金,其强度大于纯铝
B.太阳电池翼采用碳纤维框架和玻璃纤维网,二者均为无机非金属材料
C.“问天”实验舱采用了砷化镓太阳电池片,砷化镓具有良好的导电性
D.核心舱配置的离子推进器以氙气和氩气作为推进剂,氙气和氩气属于稀有气体
2.冠醚能与阳离子作用,12—冠—4与作用而不与作用;18—冠—6与作用,但不与或作用。下列说法错误的是( )
A.超分子中O原子与间存在离子键
B.冠醚与阳离子作用跟环的大小有关
C.12—冠—4中C和O的杂化方式相同
D.18—冠—6可增大KCN在溴乙烷中的溶解度
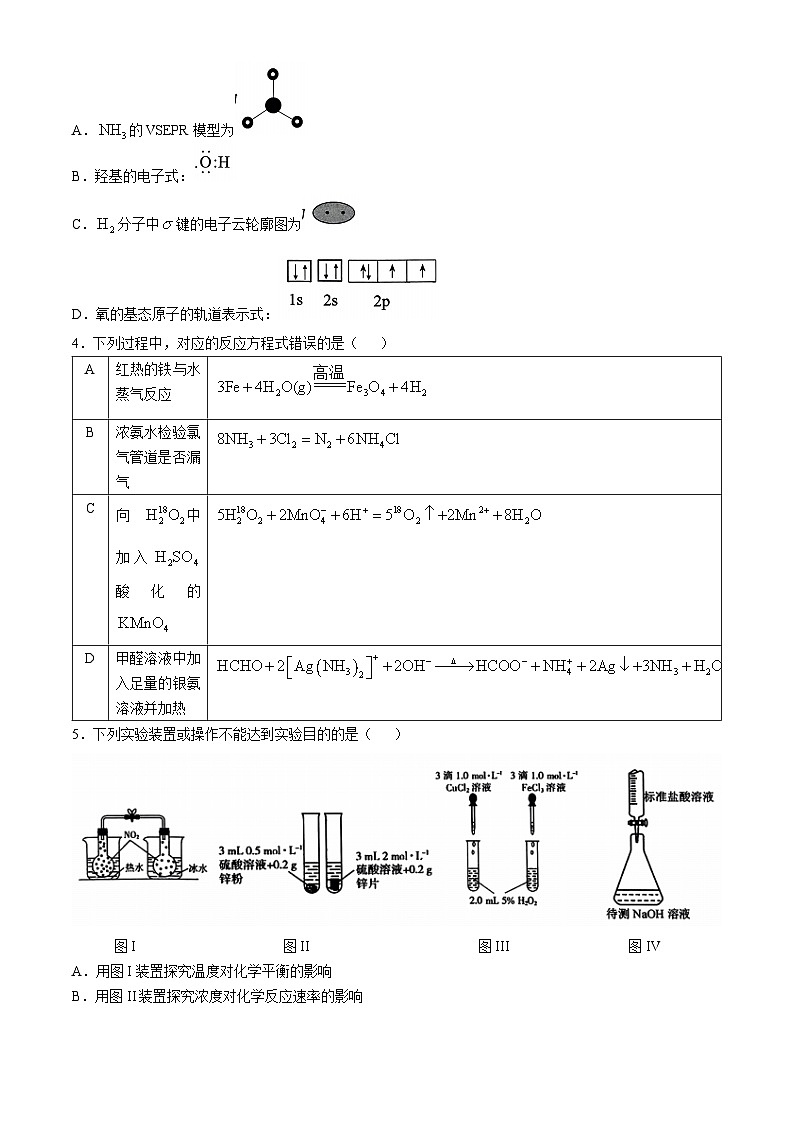
3.下列化学用语表述错误的是( )
A.的VSEPR模型为
B.羟基的电子式:
C.分子中键的电子云轮廓图为
D.氧的基态原子的轨道表示式:
4.下列过程中,对应的反应方程式错误的是( )
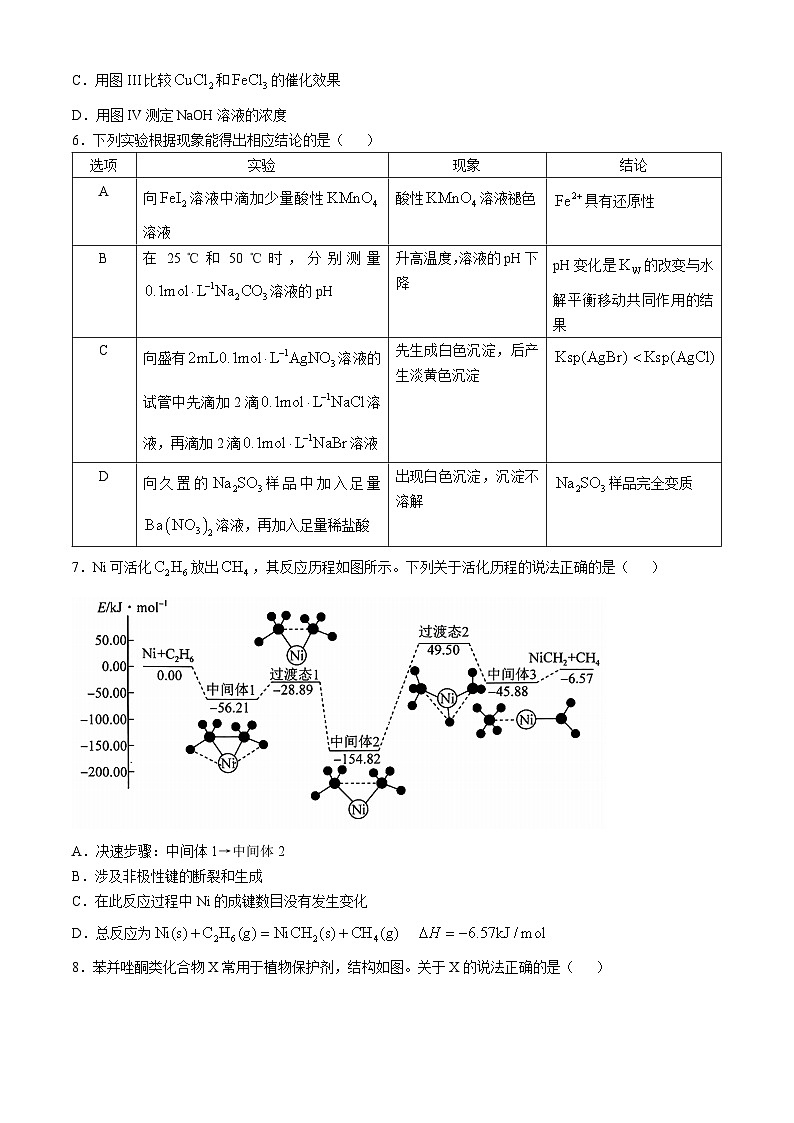
5.下列实验装置或操作不能达到实验目的的是( )
图I 图II 图III 图IV
A.用图I装置探究温度对化学平衡的影响
B.用图II装置探究浓度对化学反应速率的影响
C.用图III比较和的催化效果
D.用图IV测定NaOH溶液的浓度
6.下列实验根据现象能得出相应结论的是( )
7.Ni可活化放出,其反应历程如图所示。下列关于活化历程的说法正确的是( )
A.决速步骤:中间体1→中间体2
B.涉及非极性键的断裂和生成
C.在此反应过程中Ni的成键数目没有发生变化
D.总反应为
8.苯并唑酮类化合物X常用于植物保护剂,结构如图。关于X的说法正确的是( )
A.分子中所有原子可能共面
B.能使酸性高锰酸钾溶液褪色,但不能使溴水褪色
C.X与足量加成后所得产物分子中手性碳原子数目为4个
D.1mlX与足量NaOH溶液充分反应,最多可消耗2mlNaOH
9.我国科学家在寻找“点击反应”的砌块过程中发现的一种新化合物的结构如图所示,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,X与Z同主族。下列说法正确的是( )
A.电负性:
B.第一电离能:
C.W与X的简单氢化物的键角前者小
D.Z的最高价氧化物的空间结构为平面正三角形
10.利用电解法脱除生活废水中的氮磷,其装置和脱除原理如右图所示。开始时,n接电源正极,电解一段时间后将电源正负极交换,可转化为沉淀。
下列说法不正确的是( )
A.电解一段时间(正负极交换前),溶液pH不变
B.若开始时n接电源负极,则无法除去
C.若除去等物质的量的和,理论上电路中通过的电子数相同
D.除磷的电解反应为
11.二氧化氯()是一种黄绿色气体,是国际上公认的安全、无毒的绿色消毒剂。二氧化氯的制备以及由二氧化氯制备一种重要的含氯消毒剂——亚氯酸钠()的工艺流程如图,下列说法正确的是( )
已知:①的溶解度随温度升高而增大,适当条件下可结晶析出;
②纯易分解爆炸,一般用稀有气体或空气稀释到10%以下以保证安全。
A.“吸收塔”内发生反应的化学方程式为
B.“发生器”中鼓入空气的作用是将氧化成
C.对晶体进行重结晶可获得纯度更高的晶体
D.工业上的氯碱工业(制备烧碱和氯气)用的是阴离子交换膜
12.氮化硼(BN)晶体有多种结构。六方氮化硼是通常存在的稳定相,与石墨相似,具有层状结构。六方氮化硼在高温、高压下,可以转化为立方氮化硼,其结构、硬度与金刚石相似。
设为阿伏加德罗常数的值,它们的晶体结构及晶胞如图所示。下列说法错误的是( )
A.六方氮化硼转化为立方氮化硼是吸热反应
B.六方氮化硼和立方氮化硼中,B原子的杂化方式都是
C.立方氮化硼晶胞棱长为361.5pm,其密度是
D.立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是立方氮化硼晶体
13.某恒温密闭容器发生可逆反应:,在时刻反应达到平衡,在时刻缩小容器体积,时刻再次达到平衡状态后未再改变条件.下列有关说法中正确的是( )
A.Z和W在该条件下至少有一个为气态
B.若在该温度下此反应平衡常数表达式为,则时间段与时刻后的X浓度不相等
C.时间段与时刻后,两时间段反应体系中气体的平均摩尔质量可能相等
D.若该反应只在某温度T以上自发进行,则该反应的平衡常数K随温度升高而减小
14.25℃时,向HR溶液中滴加NaOH溶液,测得随pH的变化关系如图所示。下列叙述错误的是( )
A.M点水的电离程度大于N点的
B.pH为5.0时,
C.的NaR溶液的pH约为9
D.滴至溶液时,
二、非选择题(本题共4大题,共58分)
15.配合物乙二胺四乙酸铁钠(结构如图一所示,以下简写为NaFeY)可以添加到酱油中作为铁强化剂,制备乙二胺四乙酸铁钠晶体步骤如下:
①称取一定质量的于烧杯中溶解,加入适量浓氨水后搅拌、过滤、洗涤、干燥。
②将第一步得到的、乙二胺四乙酸、加入图二仪器a中,搅拌,80℃水浴1h,再加入适量碳酸钠溶液反应10min。
③将②反应后溶液经操作X后,过滤洗涤,晾干得到产品。
回答下列问题:
图一 图二
(1)乙二胺四乙酸铁钠中含有的化学键类型有共价键、________、________。
(2)步骤①中氨水应当________(填“分批”或“一次性”)加入。
(3)盛装溶液仪器名称为________,加入碳酸钠溶液后可观察到产生大量气泡,则步骤②由生成的总反应化学方程式为________________。
(4)步骤③操作X为________。
(5)市售铁强化剂中含有、、,其中。称取mg样品,加稀硫酸溶解后配成100mL溶液。取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用标准溶液滴定,重复操作2~3次,消耗标准溶液的平均值为VmL。
已知:、、、。
①滴定终点的现象为:当滴入最后半滴标准液时,溶液由________
②样品中铁元素的质量分数为________。
16.高性能磁带的磁粉主要成分是,某探究小组设计了下图所示流程制取,图中正极材料的主要成分是,还含有少量Al和Fe,{已知常温下,,空气难氧化}
请根据流程回答下列问题:
(1)基态C原子的价电子排布式为________。
(2)提高酸浸浸取率的措施是________________。(写一条即可)
(3)废渣的成分是________。
(4)配制硫酸亚铁溶液时加入稀硫酸的作用是________________。
(5)在工序“酸浸”过程中,加入的目的是(用化学方程式表示):________________________。
(6)实验室要完成“工序②”操作除用到仪器坩埚、酒精灯外还会用到________________________。
(7)写出“工序①”的离子方程式:________________________。
(8)常温时,“沉钴”过程中,当溶液的时,________。
17.有机物M是一种新型光电材料,合成路线如下。
已知:
回答下列问题:
(1)A的名称是________,M中含有________个手性碳原子。
(2)A→B反应分两步进行,第二步的反应类型为________________,C中官能团的名称是________。
(3)D→E的化学方程式为________________。
(4)N为B的同系物,其相对分子质量比B小14,写出其中核磁共振氢谱峰面积之比为的结构简式________。
(5)①苯胺②对甲基苯胺③对氯苯胺,相同条件下碱性由强到弱的顺序是________(填序号)。
(6)以丙烯为原料合成(无机试剂自选),写出合成路线图________。
18.及氮氧化物属于污染性气体,排放到空气中可形成光化学烟雾、酸雨等,科学家一直致力于研究这些气体的处理,变废为宝。回答下列问题:
(1)已知反应:① ,
② ,
则反应的________。该反应在________下自发进行。(填写“低温”“高温”“任意温度”)
(2)常温下,NO、溶于水可制得溶液,向溶液中滴入的NaOH溶液,使得溶液的,该溶液中________。
[,保留一位小数]。
(3)研究表明,CO与在作用下发生反应:的能量变化及反应历程如图所示:
a.该反应分两步进行,两步反应分别为:反应①;反应②________________;
b.在固定体积的密闭容器中,发生该反应,改变原料气配比进行多组实验(各次实验的温度可能相同,也可能不同),测定的平衡转化率。部分实验结果如图所示。B、C、D三点对应的实验温度分别为、和,则、、的大小关系________(填写序号)
①②③④
(4)燃煤烟气中可通过反应实现硫的回收。将和2mlCO通入1L恒容密闭容器中,在恒温T℃,起始压强为条件下反应,5min时,反应达到平衡,气体密度减少。平衡常数为________(L/ml);若升高温度,气体的密度增加(S仍为液体),则该反应的________0(填“>”或“<”)。
(5)深埋在潮湿土壤中的铁管道,在硫酸盐还原菌(该还原菌最佳生存环境pH为7~8之间)作用下,能被腐蚀,其电化学腐蚀原理如图所示,写出正极的电极反应式:_________________________。
参考答案
C 2、A 3、A 4.D 5.B 6.B 7、D 8.C 9.D 10.A
C 12.B 13.C 14.C
16.(1)3d74s2 (2) 适当升高温度
(3)Fe(OH)3
(4)防止亚铁离子水解
(5)8+ + 11 H2SO4 = 4Li2SO4 + 8 CSO4 + Na2SO4 + 11H2O
(6)泥三角、三脚架
(7)4Fe2+ + O2 + 8OH— =4 FeOOH↓ (8)1.6 ×10—10
(1)对甲基苯甲醛 2 (2)消去反应 醛基 碳溴键
(4)
(5)②﹥①﹥③
(6)
18.
A
红热的铁与水蒸气反应
B
浓氨水检验氯气管道是否漏气
C
向中加入酸化的
D
甲醛溶液中加入足量的银氨溶液并加热
选项
实验
现象
结论
A
向溶液中滴加少量酸性溶液
酸性溶液褪色
具有还原性
B
在25℃和50℃时,分别测量溶液的pH
升高温度,溶液的pH下降
pH变化是的改变与水解平衡移动共同作用的结果
C
向盛有溶液的试管中先滴加2滴溶液,再滴加2滴溶液
先生成白色沉淀,后产生淡黄色沉淀
D
向久置的样品中加入足量溶液,再加入足量稀盐酸
出现白色沉淀,沉淀不溶解
样品完全变质
相关试卷
这是一份湖南省郴州市2024-2025学年高三上学期第一次教学质量监测(一模)化学试题,共10页。
这是一份湖南省株洲市2023-2024学年高三上学期教学质量检测一(一模)化学试卷(Word版附答案),共13页。试卷主要包含了选择题的作答,非选择题的作答,考试结束后,将答题卡上交等内容,欢迎下载使用。
这是一份湖南省郴州市2024届高三上学期第一次教学质量监测试卷(10月)化学+PDF版含答案,文件包含第9课《我和我的家》课件pptx、第9课《我和我的家》教案docx等2份课件配套教学资源,其中PPT共32页, 欢迎下载使用。












