
所属成套资源:高中化学新教材同步必修第二册(同步讲义)
人教版 (2019)必修 第二册实验活动9 乙醇、乙酸的主要性质学案
展开
这是一份人教版 (2019)必修 第二册实验活动9 乙醇、乙酸的主要性质学案,共5页。
1.通过实验加深对乙醇、乙酸的主要性质的认识。
2.初步了解有机化合物的制备方法。
3.提高实验设计能力,体会实验设计在实验探究中的应用。
实验用品
试管、试管夹、量筒、胶头滴管、玻璃导管、乳胶管、橡胶塞、铁架台、试管架、酒精灯、碎瓷片、火柴、乙醇、乙酸、饱和Na2CO3溶液、浓H2SO4、铜丝,实验还需用品有澄清石灰水、石蕊溶液、酚酞溶液、锌粒、NaOH溶液、蒸发皿。
实验步骤
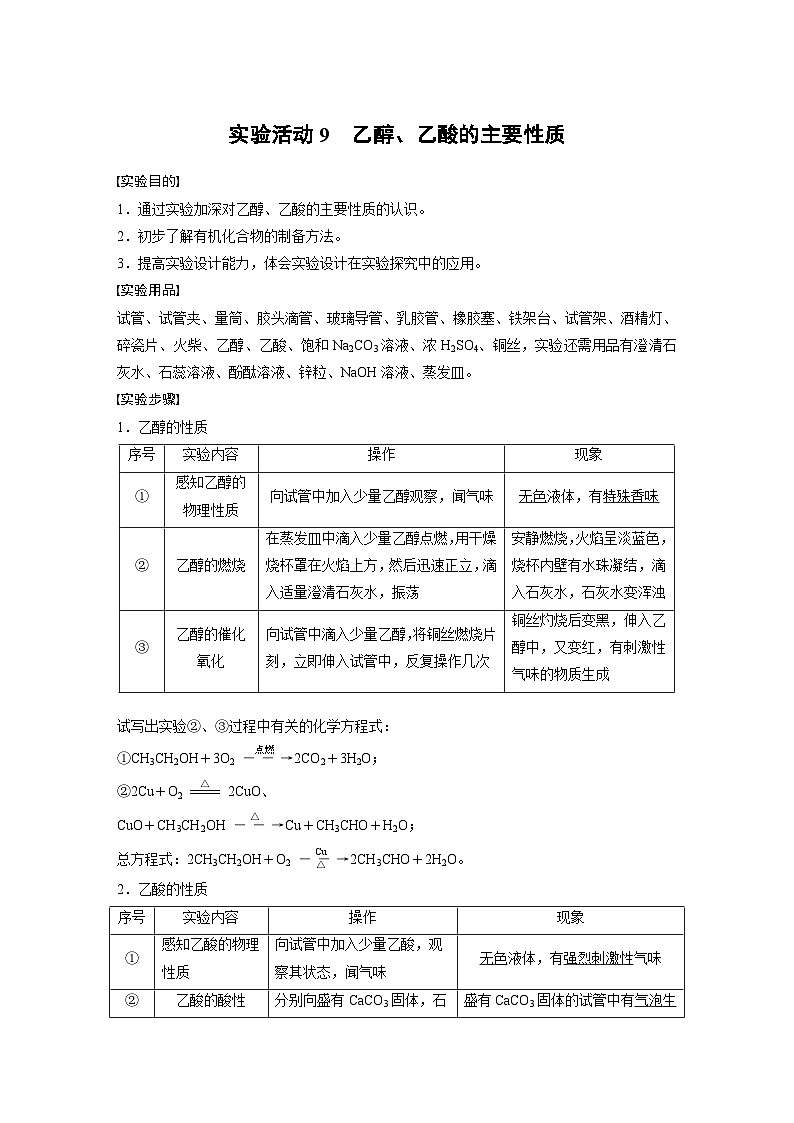
1.乙醇的性质
试写出实验②、③过程中有关的化学方程式:
①CH3CH2OH+3O2eq \(――→,\s\up7(点燃))2CO2+3H2O;
②2Cu+O2eq \(=====,\s\up7(△))2CuO、
CuO+CH3CH2OHeq \(――→,\s\up7(△))Cu+CH3CHO+H2O;
总方程式:2CH3CH2OH+O2eq \(――→,\s\up7(Cu),\s\d5(△))2CH3CHO+2H2O。
2.乙酸的性质
写出实验②、③反应过程中相关的反应方程式:
②2CH3COOH+CaCO3===(CH3COO)2Ca+CO2↑+H2O、
Zn+2CH3COOH===(CH3COO)2Zn+H2↑、
CH3COOH+NaOH===CH3COONa+H2O;
③CH3COOH+CH3CH2OHeq \(,\s\up7(浓H2SO4),\s\d5(△))CH3COOCH2CH3+H2O。
问题讨论
1.在乙醇氧化生成乙醛的实验中,加热铜丝及将它插入乙醇里的操作为什么反复几次?
提示 反复的目的是使生成的乙醛更多,更易感知实验现象。
2.在制乙酸乙酯的实验中,浓H2SO4和饱和Na2CO3溶液各是什么作用?盛有饱和Na2CO3溶液的试管内发生哪些变化?
提示 浓H2SO4在反应中作催化剂和吸水剂,饱和Na2CO3溶液的作用为吸收挥发出的乙酸,溶解挥发出来的乙醇,降低乙酸乙酯的溶解度,利于液体分层;饱和Na2CO3溶液分层,上层是无色油状液体,在溶液内,有无色气泡产生,因为挥发出的CH3COOH有酸性,能和饱和Na2CO3溶液反应生成二氧化碳,化学方程式为2CH3COOH+Na2CO3―→2CH3COONa+CO2↑+H2O。
3.已知含示踪原子18O的乙醇催化氧化的产物中只有乙醛分子中含18O(),和乙酸酯化反应的产物中只有乙酸乙酯中含有18O,试从化学键的角度分析乙醇的催化氧化和酯化反应的机理?
提示 ①根据乙醇的结构和信息,如18O只存在乙醛分子中(),则催化氧化反应中,乙醇分子中断裂的化学键只能是O—H键和羟基相邻的C—H键,即:,化学方程式为+2H2O。
②因为18O只存在乙酸乙酯中,根据乙醇和乙酸的结构,在酯化反应中,只能是乙醇分子中断裂O—H键,乙酸分子中断裂C—O键,归纳为羧酸脱羟基醇脱氢原子,即:CH3—CH2—18O—H+eq \(,\s\up7(浓H2SO4),\s\d5(△))+H2O。
1.(2018·郑州高一检测)下列说法正确的是( )
A.检测乙醇中是否含有水可加入钠,若有氢气生成则含水
B.除去乙醇中微量水,可加入金属钠,使其完全反应
C.乙醇和钠反应时,钠沉在乙醇的底部,缓慢地放气泡
D.乙醇和水的沸点不同,可直接蒸馏获得无水乙醇
答案 C
解析 乙醇和水都和钠反应生成氢气,故A、B项错误;直接蒸馏所获得的乙醇中仍含有水,不能得到纯净的无水乙醇,故D项错误;钠的密度大于乙醇,而且反应比较缓慢,故C项正确。
2.如图为实验室制取少量乙酸乙酯的装置图,下列关于该实验的叙述中,不正确的是( )
A.向a试管中先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,再加冰醋酸
B.试管b中导气管下端管口不能浸入液面下的原因是防止实验过程中发生倒吸现象
C.实验时为加快反应速率,可大火加热
D.实验中,饱和Na2CO3溶液作用为吸收乙酸、溶解乙醇,并降低乙酸乙酯的溶解度
答案 C
解析 浓硫酸的密度大于水,稀释过程放热,则加入试剂的顺序为向a试管中先加入乙醇,然后边摇动试管边慢慢加入浓硫酸,冷却后再加入冰醋酸,A项正确;乙醇和乙酸均与水互溶,则试管b中导气管下端管口不能浸入液面下的原因是防止实验过程中产生倒吸现象,B项正确;实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移动,且加热能加快反应速度,但大火加热,会使乙醇、乙酸大量挥发,从而降低了乙酸乙酯的产率,故应小火加热,故C项不正确;试管b中饱和Na2CO3溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇,同时降低乙酸乙酯的溶解度,D项正确。
3.下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与并协助他们完成相关实验任务。
[实验目的] 制取乙酸乙酯。
[实验原理] 甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯,该反应的化学方程式为________________________________________________________。
[装置设计] 甲、乙、丙三位同学分别设计了如下图所示三套实验装置:
若从甲、乙两位同学设计的装置中选择一套作为实验室制取乙酸乙酯的装置,选择的装置应是________(填“甲”或“乙”)。丙同学将甲装置中的玻璃管改成了球形的干燥管,除了起冷凝作用外,另一重要作用是____________________________________________________。
[实验步骤] A.按所选择的装置组装仪器,在试管①中先加入3 mL体积分数为95%的乙醇,并在摇动下缓缓加入2 mL浓硫酸充分摇匀,冷却后再加入2 mL冰醋酸。
B.将试管固定在铁架台上。
C.在试管②中加入5 mL饱和Na2CO3溶液。
D.用酒精灯对试管①加热。
E.当观察到试管②中有明显现象时停止实验。
[问题讨论]
(1)步骤A组装好实验装置,加入样品前还应检查____________________________________。
(2)试管②中观察到的现象是______________________________________________________。
(3)试管②中饱和Na2CO3溶液的作用是________________________,饱和Na2CO3溶液________(填“能”或“不能”)用NaOH溶液代替,其原因是_________________。
答案 [实验原理]CH3CH2OH+CH3COOHeq \(,\s\up7(浓硫酸),\s\d5(△))CH3COOCH2CH3+H2O
[装置设计]乙 防止倒吸
[问题讨论]
(1)装置气密性
(2)液体分为两层
(3)溶解乙醇、中和乙酸、降低乙酸乙酯的溶解度 不能 NaOH和乙酸乙酯反应,促进乙酸乙酯的水解
解析 反应过程产生的蒸气中含有乙酸、乙醇、乙酸乙酯和水,其中乙酸、乙醇都易溶于水,所以应该做到防止倒吸。蒸气进入到饱和碳酸钠溶液中,上层即是乙酸乙酯,下层是水层,溶解了乙酸钠、乙醇、碳酸钠等物质。
序号
实验内容
操作
现象
①
感知乙醇的物理性质
向试管中加入少量乙醇观察,闻气味
无色液体,有特殊香味
②
乙醇的燃烧
在蒸发皿中滴入少量乙醇点燃,用干燥烧杯罩在火焰上方,然后迅速正立,滴入适量澄清石灰水,振荡
安静燃烧,火焰呈淡蓝色,烧杯内壁有水珠凝结,滴入石灰水,石灰水变浑浊
③
乙醇的催化氧化
向试管中滴入少量乙醇,将铜丝燃烧片刻,立即伸入试管中,反复操作几次
铜丝灼烧后变黑,伸入乙醇中,又变红,有刺激性气味的物质生成
序号
实验内容
操作
现象
①
感知乙酸的物理性质
向试管中加入少量乙酸,观察其状态,闻气味
无色液体,有强烈刺激性气味
②
乙酸的酸性
分别向盛有CaCO3固体,石蕊溶液,锌粒和含酚酞的NaOH溶液中加入适量乙酸
盛有CaCO3固体的试管中有气泡生成,石蕊溶液变红,锌粒溶解,有气泡生成,含酚酞的NaOH溶液红色褪去
③
酯化反应
盛有饱和Na2CO3的试管中有一层有香味的油状液体生成,溶液中有气泡产生
相关学案
这是一份人教版 (2019)必修 第二册实验活动9 乙醇、乙酸的主要性质学案,共7页。
这是一份高中化学人教版 (2019)必修 第二册第七章 有机化合物实验活动9 乙醇、乙酸的主要性质导学案,共3页。
这是一份高中化学人教版 (2019)必修 第二册实验活动9 乙醇、乙酸的主要性质优质导学案,共5页。学案主要包含了实验目的,实验用品,实验步骤,问题和讨论,拓展训练等内容,欢迎下载使用。