

新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二下学期开学摸底考试化学试卷(含答案)
展开
这是一份新疆巴音郭楞蒙古自治州第一中学2022-2023学年高二下学期开学摸底考试化学试卷(含答案),共20页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
一、单选题
1.对于不同的化学反应,决定其反应速率的最主要因素是( )
A.反应体系的温度B.反应物的性质C.反应体系的压强D.反应物的浓度
2.在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度
②使用催化剂
③增大反应物浓度
④将块状固体反应物磨成粉末
⑤增大压强
A.①②③⑤B.①②④⑤C.①②④D.①②③④
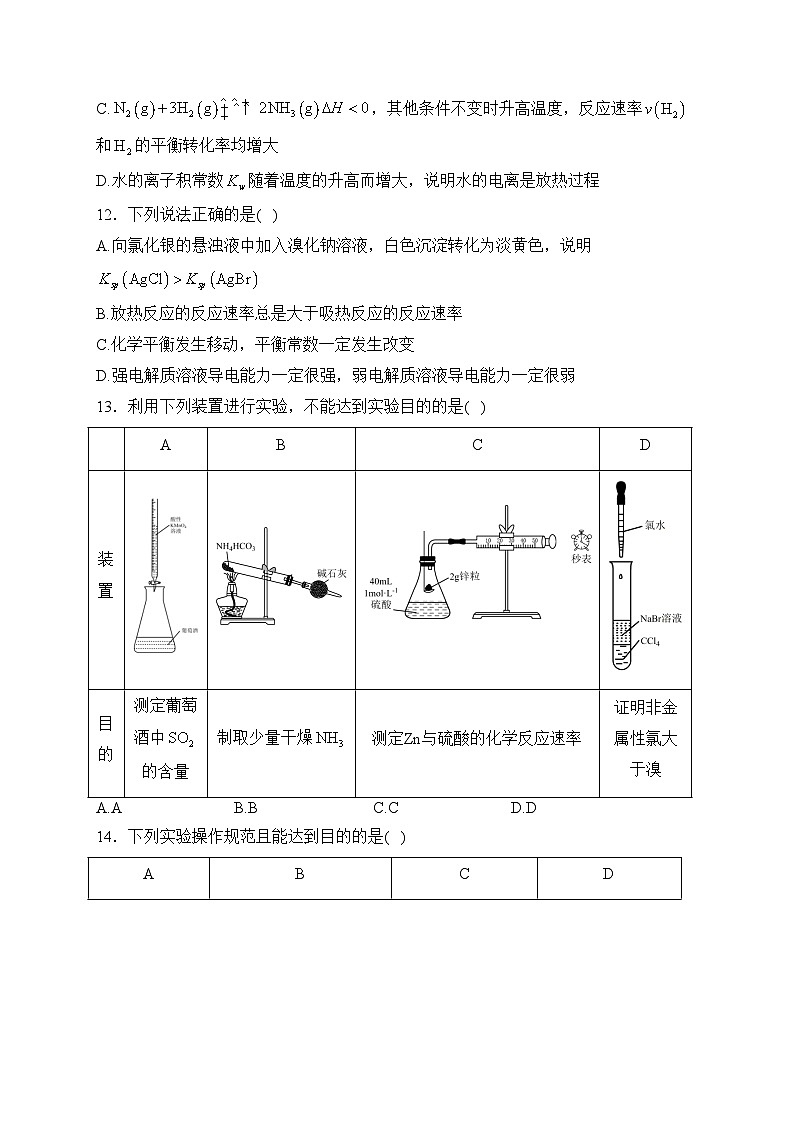
3.生活离不开化学,下列事实与电化学腐蚀有关的是( )
A.暴晒在太阳光下的地膜塑料易变成碎片
B.在铁中添加一定量的镍制成的金属硬币不易被腐蚀
C.铜、铝电线连接起来使用易出现断电现象
D.在雨水冲击下的汉白玉建筑物纹理变得模糊
4.下列措施抑制水的电离的是( )
A.加热B.加入NaOH溶液C.加入固体D.加入固体
5.下列有关化学反应的认识错误的是( )
A.一定有化学键的断裂与形成B.一定有电子转移
C.一定有新物质生成D.一定伴随着能量变化
6.室温下,下列有关的NaClO溶液的分析正确的是( )
A.
B.水电离出的为
C.含有个
D.加入少量NaOH固体,变小
7.已知气体的燃烧热为,1ml不完全燃烧生成CO和时放出的热量为519kJ。如果1ml与一定量燃烧生成CO、、,并放出731.25kJ的热量,则一定量的质量为( )
A.40gB.56gC.60gD.无法计算
8.已知在25℃、101kPa下,1g燃烧生成和时放出48.40kJ的热量,表示上述反应的热化学方程式正确的是( )
A.
B.
C.
D.
9.用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作不正确的是( )
A.酸式滴定管用蒸馏水洗净后,用已知浓度的盐酸润洗酸式滴定管
B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液
C.若用甲基橙作指示剂,则锥形瓶中溶液由橙色变为黄色即达到滴定终点
D.读数时,视线与滴定管内液体的凹液面最低处保持水平
10.下列不能用平衡移动原理解释的是( )
A.合成氨时将氨液化分离,可提高原料的利用率
B.、、HI混合气体加压后颜色变深
C.实验室用排饱和NaCl溶液的方法收集
D.由和组成的平衡体系加压后颜色先变深后变浅
11.下列有关说法正确的是( )
A.室温下不能自发进行,说明该反应的
B.将纯水加热至较高温度,水的离子积变大、pH变小、呈中性
C.,其他条件不变时升高温度,反应速率和的平衡转化率均增大
D.水的离子积常数随着温度的升高而增大,说明水的电离是放热过程
12.下列说法正确的是( )
A.向氯化银的悬浊液中加入溴化钠溶液,白色沉淀转化为淡黄色,说明
B.放热反应的反应速率总是大于吸热反应的反应速率
C.化学平衡发生移动,平衡常数一定发生改变
D.强电解质溶液导电能力一定很强,弱电解质溶液导电能力一定很弱
13.利用下列装置进行实验,不能达到实验目的的是( )
A.AB.BC.CD.D
14.下列实验操作规范且能达到目的的是( )
A.AB.BC.CD.D
15.在比较化学反应速率时,不可以利用的相关性质为( )
A.气体的体积和体系的压强B.颜色的深浅
C.固体物质量的多少D.反应的剧烈程度
16.下列说法中正确的是( )
A.物质燃烧放出的热量是燃烧热
B.1mlC燃烧生成CO时放出的热量就是C的燃烧热
C.1ml燃烧生成水时放出的热量是的燃烧热
D.相同条件下,1ml完全分解吸收的热量与、化合生成1ml放出的热量值相等
17.水的电离平衡曲线如图所示,曲线中的点都符合常数,下列说法错误的是( )
A.图中温度
B.图中五点间的关系:
C.若从A点到D点,可采用在水中加入少量酸的方法
D.时,将的硫酸溶液与的KOH溶液等体积混合后,溶液显中性
18.下列实验能达到预期目的的是( )
A.AB.BC.CD.D
19.下列关于化学反应的说法正确的是( )
A.将苯滴入溴水中,振荡后水层接近无色,发生取代反应
B.化学反应除了生成新的物质外,不一定伴随着能量的变化
C.放热的化学反应不需要加热就能发生
D.氧化铁与铝反应既是氧化还原反应又是放热反应
20.可逆反应中,当其它条件不变时,C的质量分数与温度(T)的关系如图,则下列说法正确的是( )
A.放热反应B.吸热反应C.吸热反应D.放热反应
21.常温下,下列各组离子在指定溶液中能大量共存的是( )
A.澄清透明的溶液中:、、、
B.中性溶液中:、、、
C.的溶液中:、、、
D.的溶液中:、、、
22.用下图所示装置及试剂进行铁的电化学腐蚀实验探究,测得几支锥形瓶中压强、溶解氧随时间变化关系的曲线如下。下列分析错误是( )
A.压强增大主要是因为产生了B.时正极只发生:
C.负极的反应都为:D.都发生了吸氧腐蚀
23.在一定条件下,反应,达到平衡状态的标志是:( )
A.单位时间内生成2nmlA,同时生成nmlD
B.容器内压强不随时间而变化
C.单位时间内生成nmlB,同时消耗1.5nmlC
D.容器内混合气体密度不随时间而变化
24.下列离子方程式书写正确的是( )
A.用FeS除去废水中的:
B.用醋酸溶液处理水垢中的氢氧化镁:
C.在溶液中滴加NaClO溶液:
D.谷氨酸与足量氢氧化钠溶液反应:
25.图象能正确反映对应变化关系的是( )
A.AB.BC.CD.D
二、填空题
26.已知下列热化学方程式:
①
②
③
请回答:
(1)上述反应中属于放热反应的是_______(填序号,下同),属于吸热反应的是_______。
(2)2g的完全燃烧生成液态水,放出的热量为_______。
(3)依据事实,写出下列反应的热化学方程式。
①1ml与适量反应生成,需吸收68kJ的热量,该反应的热化学方程式为_______。
②1ml与适量反应生成,放出92.4kJ的热量,该反应的热化学方程式为_______。
27.化学反应与生产研究息息相关,我们不仅关注能量变化,还需要关注化学反应的快慢和程度。请根据要求,回答下列问题:
(1)下面是四个化学反应理论上不可以用于设计原电池的化学反应是_______(填字母,下同)。
A.B.
C.D.
(2)将氢气与氧气的反应设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中_______(填A或B)处电极入口通氧气,其电极反应式为_______。
(3)某温度时,在2L容器中发生X、Y两种物质间的转化反应,X、Y物质的量随时间变化的曲线如图所示:
①该反应的化学方程式为_______。
②反应开始至2min时,Y的平均反应速率为_______。
③2min时,_______(填“>”“
解析:(1)反应A、C是非氧化还原反应,理论上不可以用于设计原电池。
(2)电子由负极经外电路流向正极,b极为正极,正极电极反应式为;
(3)X的物质的量增加、Y的物质的量减少,所以Y是反应物、X是生成物,物质的量的变化量之比等于化学计量数之比,即Y与X的化学计量数之比为2:1,且由题图可知该反应是可逆反应,故该反应的化学方程式为。反应开始至2 min时,Y的平均反应速率为。2 min时,还未达平衡状态,反应正向进行中,故。
28.答案:(1)增大
(2)HCN;;B;
(3);;由于一级电离产生氢离子,增大了溶液中氢离子浓度,使电离平衡向左移动
(4)能
解析:(1)弱酸的电离吸热,所以温度升高时,酸的电离程度增大,电离平衡常数K增大,故答案为:增大。
29.答案:(1)化学;电;32.1
(2)阴极;
(3)Mg经导线流向Al;;B
(4)吸氧腐蚀;牺牲阳极的阴极保护法(或外加电流的阴极保护法)
解析:(2)由图2所示的装置可知:A电极通入的是二氧化硫,具有还原性,易失电子,所以电极A为阳极,电极B为阴极;
电极A上发生的电极反应为:;
(3)由图3可知,电解质溶液为KOH溶液,Al与碱反应,而Mg不反应,则外电路中电子流向为Al流向Mg,故其电流方向为由Mg经导线流向Al,Mg电极的电极反应为:,若要改变外电路中的电流方向,可将图3中的KOH溶液换为盐酸,则Mg比Al活泼;
(4)图4是铁在中性盐溶液中的吸氧腐蚀,为了防止这类反应的发生,若利用原电池原理,则采用牺牲阳极的阴极保护法,即铁为正极,不易腐蚀,若利用电解池原理,则采用外加电流的阴极保护法,即铁作阴极,不被腐蚀。
30.答案:(1)54.8
(2)ab
(3)相等;偏小
解析:(1)取溶液与溶液在小烧杯中进行中和反应,根据数据可知,硫酸过量,氢氧化钠完全反应,根据反应,生成水的物质的量=n(NaOH)=0.05Lx0.5ml/L=0.025ml,三次实验温度平均升高,已知中和后生成的溶液的比热容为,该反应放出的热量Q=cmΔt=xx80mLx= 1371J=1.371kJ,则生成时放出的热量 =54.8kJ/ml;
(2)该实验测得数值结果小于57.3kJ⋅ml−1,即偏小,
a.装置保温、隔热效果差,测得的热量偏小,中和热的数值偏小,故a符合题意;
b.测量氢氧化钠的温度后,温度计没有用水冲洗干净,直接测定溶液的温度,会发生酸和碱的中和,温度偏高,则温度差减小,实验测得中和热的数值偏小,故b符合题意;
c.尽量一次快速将NaOH溶液倒入盛有硫酸的小烧杯中,不允许分多次把NaOH溶液倒入盛有硫酸的小烧杯中,故c不符合题意;
答案选ab;
(3)反应放出的热量和所用酸以及碱的量的多少有关,若用和溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,中和热即强酸和强碱的稀溶液反应生成1ml水放出的热量不随反应物量的多少变化,故相等;醋酸是弱电解质,醋酸的电离是吸热过程,所以导致反应前后温度的变化值偏小。
A
B
C
D
装置
目的
测定葡萄酒中的含量
制取少量干燥
测定Zn与硫酸的化学反应速率
证明非金属性氯大于溴
A
B
C
D
除去碳酸钠中的碳酸氢钠
氯气的净化
粗铜精炼
收集NO气体
选项
实验内容
实验目的
A
向溶液X中滴加浓盐酸,将产生气体通入品红溶液,溶液褪色
证明溶液X中含有或
B
室温下,向溶液中加入几滴溶液出现白色沉淀,再滴加几滴溶液,出现黄色沉淀
证明相同温度下:
C
常温下,测得相同浓度溶液的pH:
证明常温下的水解程度:
D
将溶液滴入酸性溶液中,紫红色褪去
证明有还原性
A
B
C
D
电解水
往、混合溶液加入Zn粉至过量
加热一定质量的固体
向等质量、等浓度的稀硫酸中分别加入足量Mg和Zn
酸
HCN
HClO
电离平衡常数()
相关试卷
这是一份博爱县第一中学2023-2024学年高二下学期开学摸底考试化学试卷(含答案),共20页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
这是一份新疆巴音郭楞蒙古自治州且末县第一中学2023-2024学年高三上学期开学化学试题,共10页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。
这是一份新疆巴音郭楞蒙古自治州博湖县奇石中学2022-2023学年高二下学期期中考试化学试题(PDF版含答案),文件包含2022-2023学年第二学期高二年级期中考试试卷答案docx、2022-2023学年第二学期高二年级期中考试化学试卷pdf等2份试卷配套教学资源,其中试卷共10页, 欢迎下载使用。









