



所属成套资源:新人教版化学选择性必修2课件PPT整册
- 2.2《分子的空间结构》(第1课时)课件 课件 4 次下载
- 2.2《分子的空间结构》(第2课时)课件 课件 4 次下载
- 2.3《分子结构与物质的性质》(第2课时)课件 课件 5 次下载
- 3.1《物质的聚集状态与晶体的常识》课件 课件 7 次下载
- 3.2《分子晶体与共价晶体》(第1课时)课件 课件 10 次下载
高中人教版 (2019)第三节 分子结构与物质的性质完美版ppt课件
展开
这是一份高中人教版 (2019)第三节 分子结构与物质的性质完美版ppt课件PPT课件主要包含了核心素养,温故知新,电子式,结构式,共用电子对不偏移,共用电子对偏移,认识共价键的极性,不偏移,电中性,共价键的极性等内容,欢迎下载使用。
能从微观角度理解共价键的极性和分子极性的关系。
通过键的极性对物质性质的影响的探析,形成“结构决定性质”的认知模型。
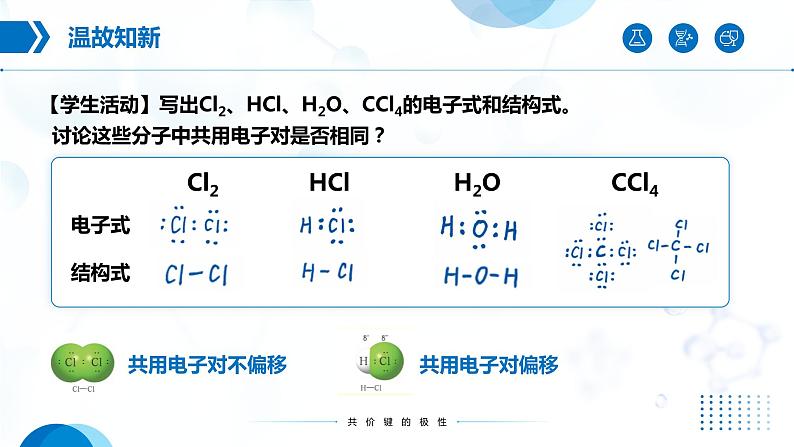
【学生活动】写出Cl2、HCl、H2O、CCl4的电子式和结构式。 讨论这些分子中共用电子对是否相同?
Cl2 HCl H2O CCl4
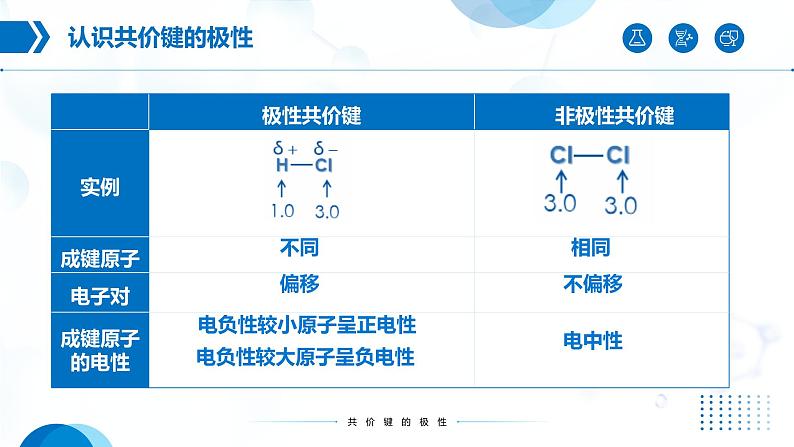
电负性较小原子呈正电性
电负性较大原子呈负电性
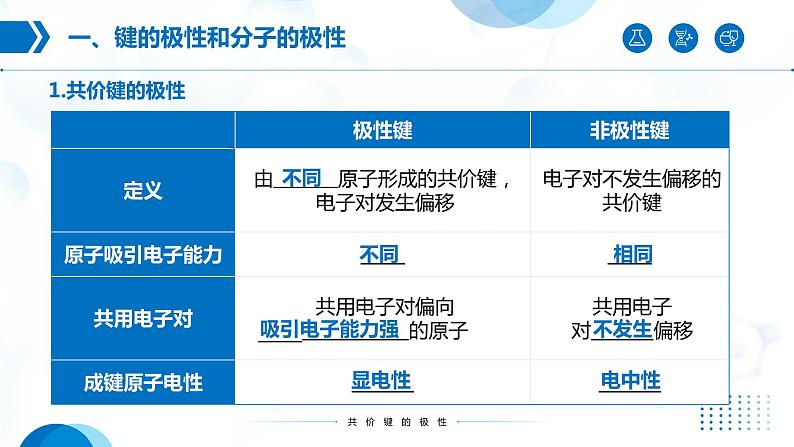
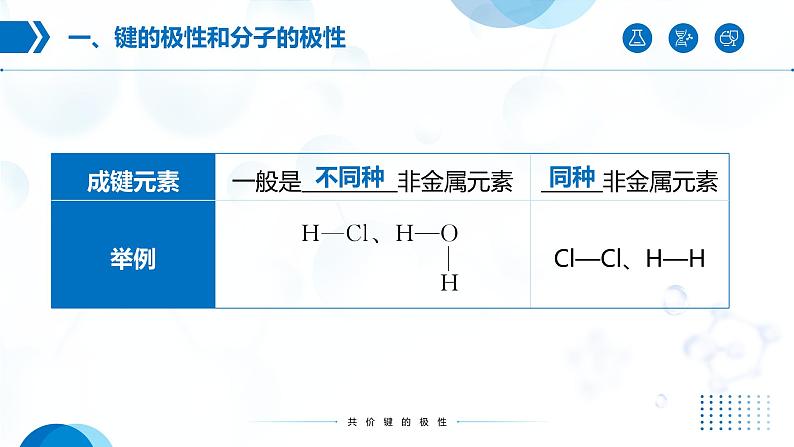
一、键的极性和分子的极性
回答下列问题:①H2 ②O2 ③HCl ④P4 ⑤C60 ⑥CO2 ⑦CH2==CH2 ⑧HCN ⑨H2O ⑩NH3 ⑪BF3 ⑫CH4 ⑬SO3 ⑭CH3Cl ⑮Ar ⑯H2O2只含非极性键的是_________;只含极性键的是 ___________________既含极性键又含非极性键的是_____。
【实验·探究】 在酸式滴定管中分别加入四氯化碳和蒸馏水,打开开关,用在头发上摩擦 过的气球靠近液体,观察现象。
水流发生偏转,四氯化碳液流无变化
水分子中存在正极与负极,四氯化碳分子中无正极与负极之分
2.极性分子和非极性分子
像水分子这样,分子中正电中心和负电中心不重合的分子叫做极性分子。
像四氯化碳分子这样,分子中正电中心和负电中心重合的分子叫做非极性分子。
3.共价键的极性和分子极性的关系
【问题·思考】 含有极性键的分子一定是极性分子吗?
正四面体形,空间构型对称
分子的正电中心与负电中心是否重合
H2 O2 Cl2
同种原子构成的双原子分子是非极性分子
不同原子构成的双原子分子是极性分子
相同原子构成的多原子分子大多是非极性分子
极性的表示方法极性向量
极性向量:描述极性键的电荷分布情况方向:大小:
由正电中心指向负电中心
电负性差值越大,键的极性越大,极性向量越大
非极性键无极性向量,说明在非极性键里,正负电荷的中心是重合的
5.从向量角度判断分子极性
正电中心与负电中心重合
正电中心与负电中心不重合
【归纳整理】常见ABn型分子的极性
大气高空的臭氧层,保护了地球生物的生存空气质量的重要指标有机合成的氧化剂替代氯气的净水剂……
臭氧是极性分子(极性微弱)
1.下列各组物质中,都是由极性键构成的极性分子的一组是A.CH4和Br2 B.NH3和H2OC.H2S和CCl4 D.CO2和HCl
解析 CH4、CCl4、CO2都是由极性键形成的非极性分子,NH3、 H2O、H2S、HCl都是由极性键形成的极性分子。
2.以极性键结合的多原子分子,分子是否有极性取决于分子的空间结构。下列分子都属于含极性键的非极性分子的是
A.CO2 H2O B.NH3 BCl3C.PCl3 CH4 D.CS2 BF3
二、键的极性对化学性质的影响
键的极性对化学性质的影响
表2-6 不同羧酸的pKa
烃基越长推电子效应越大
使羧基中的羟基的极性越小
随着烃基加长,酸性的差异越来越小
酸性:甲酸>乙酸>丙酸
Cl原子数目越多,吸引电子能力越大
使羧基中的羟基的极性越大
酸性:CF3COOH>CCl3COOH
1.三氟乙酸的酸性大于三氯乙酸酸性的原因
提示:由于氟的电负性大于氯的电负性,F—C的极性大于Cl—C的极性,使F3C—的极性大于Cl3C—的极性,导致三氟乙酸的羧基中的羟基的极性更大更易电离出氢离子。
2.三氯乙酸的酸性大于二氯乙酸酸性的原因
提示:由于Cl3C—比Cl2CH—多一个氯原子,使Cl3C—的极性大于Cl2CH—的极性,导致三氯乙酸的羧基中的羟基的极性更大,更易电离出氢离子。
3. 甲酸的酸性大于乙酸酸性的原因
提示:烃基(R—)是推电子基团,烃基越长推电子效应越大,使羧基中的羟基的极性越小,羧酸的酸性越弱。
4. 试比较下列有机酸的酸性强弱。
答案:①>②>③>④>⑤>⑥
①CF3COOH ②CCl3COOH ③CHCl2COOH ④CH2ClCOOH ⑤CH3COOH ⑥CH3CH2COOH
1.下列叙述中正确的是A.卤化氢分子中,卤素的非金属性越强,共价键的极性越大,热稳定性也越强B.以极性键结合的分子,一定是极性分子C.判断A2B或AB2型分子是否是极性分子的依据是看分子中是否含有极性键D.非极性分子中,各原子间都应以非极性键结合
2.下列叙述正确的是A.NO、N2O、NO2、NH3都是非极性分子B.CO2、SO3、BCl3、NF5都是非极性分子C.H2O、NH3是极性分子,分子中的H—O比N—H的极性弱D.PCl5、NCl3、SO3、BF3、CCl4都是非极性分子
相关课件
这是一份高中化学人教版 (2019)选择性必修2第三节 分子结构与物质的性质完美版课件ppt,共31页。PPT课件主要包含了C6H6,H2O,共价键,正四面体,sp3杂化,非极性分子,范德华力,GeCl4等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修2第三节 分子结构与物质的性质公开课课件ppt,共60页。PPT课件主要包含了键的极性,发生偏移,不发生偏移,分子的极性,不重合,非极性,向量和,电负性,氢原子,XHY等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修2第三节 分子结构与物质的性质优秀课件ppt,共33页。PPT课件主要包含了核心素养,范德华力,干冰汽化吸热,氢键的形成原理,水分子间氢键实物模型,邻羟基苯甲醛,对羟基苯甲醛,冰中的四面体结构,冰晶体构型,实验探究等内容,欢迎下载使用。










