初中化学沪教版 (上海)九年级第一学期3.2 溶液同步达标检测题
展开
这是一份初中化学沪教版 (上海)九年级第一学期3.2 溶液同步达标检测题,共17页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
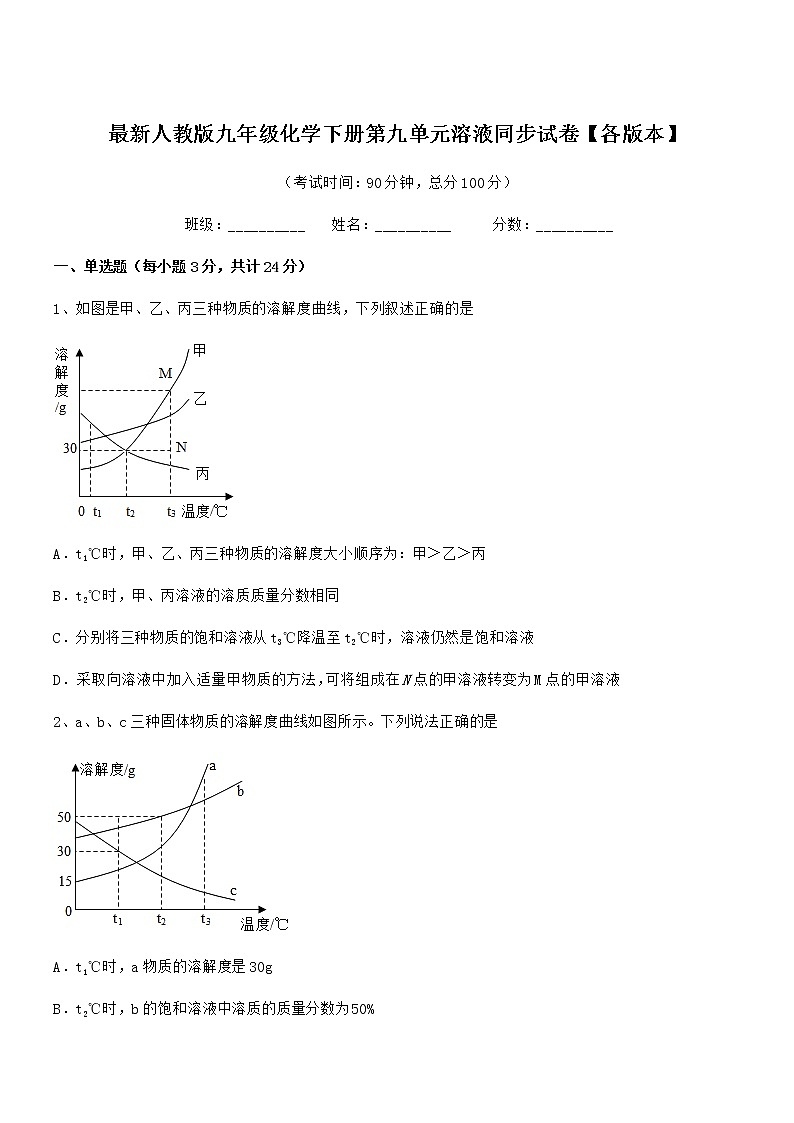
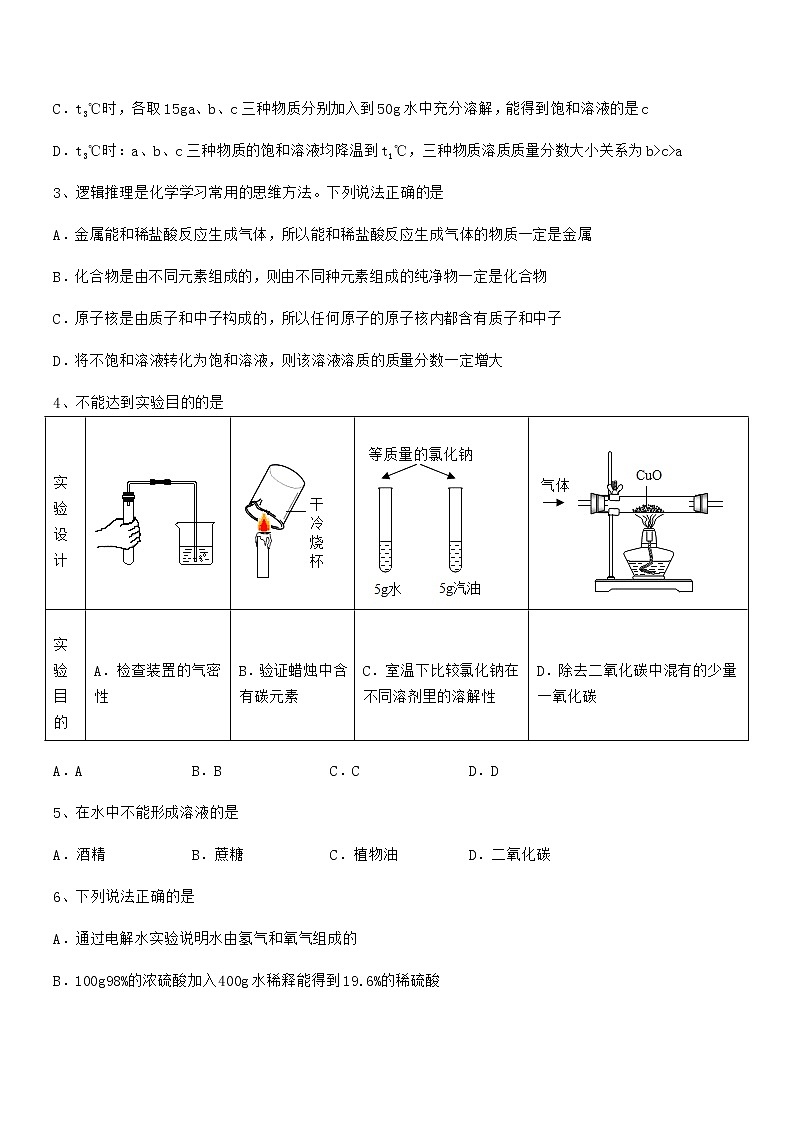
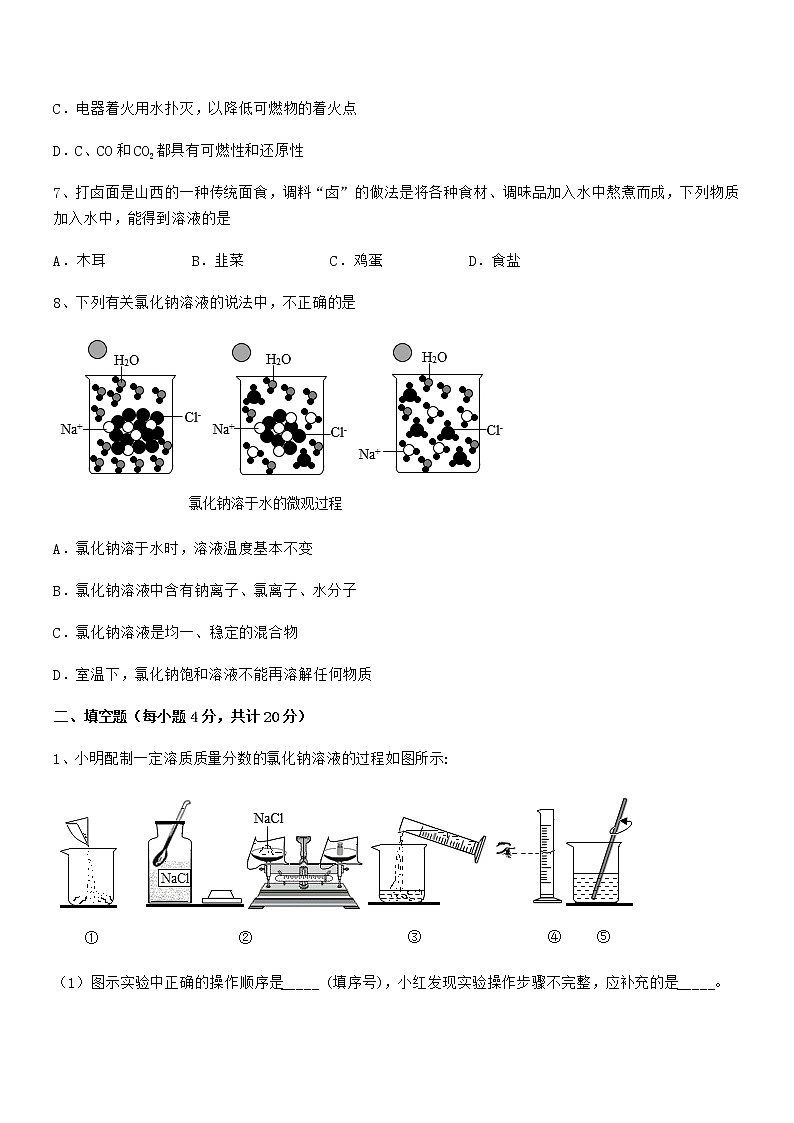
最新人教版九年级化学下册第九单元溶液同步试卷【各版本】(考试时间:90分钟,总分100分)班级:__________ 姓名:__________ 分数:__________一、单选题(每小题3分,共计24分)1、如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是A.t1℃时,甲、乙、丙三种物质的溶解度大小顺序为:甲>乙>丙B.t2℃时,甲、丙溶液的溶质质量分数相同C.分别将三种物质的饱和溶液从t3℃降温至t2℃时,溶液仍然是饱和溶液D.采取向溶液中加入适量甲物质的方法,可将组成在N点的甲溶液转变为M点的甲溶液2、a、b、c三种固体物质的溶解度曲线如图所示。下列说法正确的是A.t1℃时,a物质的溶解度是30gB.t2℃时,b的饱和溶液中溶质的质量分数为50%C.t3℃时,各取15ga、b、c三种物质分别加入到50g水中充分溶解,能得到饱和溶液的是cD.t3℃时:a、b、c三种物质的饱和溶液均降温到t1℃,三种物质溶质质量分数大小关系为b>c>a3、逻辑推理是化学学习常用的思维方法。下列说法正确的是A.金属能和稀盐酸反应生成气体,所以能和稀盐酸反应生成气体的物质一定是金属B.化合物是由不同元素组成的,则由不同种元素组成的纯净物一定是化合物C.原子核是由质子和中子构成的,所以任何原子的原子核内都含有质子和中子D.将不饱和溶液转化为饱和溶液,则该溶液溶质的质量分数一定增大4、不能达到实验目的的是实验设计实验目的A.检查装置的气密性B.验证蜡烛中含有碳元素C.室温下比较氯化钠在不同溶剂里的溶解性D.除去二氧化碳中混有的少量一氧化碳A.A B.B C.C D.D5、在水中不能形成溶液的是A.酒精 B.蔗糖 C.植物油 D.二氧化碳6、下列说法正确的是A.通过电解水实验说明水由氢气和氧气组成的B.100g98%的浓硫酸加入400g水稀释能得到19.6%的稀硫酸C.电器着火用水扑灭,以降低可燃物的着火点D.C、CO和CO2都具有可燃性和还原性7、打卤面是山西的一种传统面食,调料“卤”的做法是将各种食材、调味品加入水中熬煮而成,下列物质加入水中,能得到溶液的是A.木耳 B.韭菜 C.鸡蛋 D.食盐8、下列有关氯化钠溶液的说法中,不正确的是A.氯化钠溶于水时,溶液温度基本不变B.氯化钠溶液中含有钠离子、氯离子、水分子C.氯化钠溶液是均一、稳定的混合物D.室温下,氯化钠饱和溶液不能再溶解任何物质二、填空题(每小题4分,共计20分)1、小明配制一定溶质质量分数的氯化钠溶液的过程如图所示:(1)图示实验中正确的操作顺序是_____ (填序号),小红发现实验操作步骤不完整,应补充的是_____。(2)配制500g质量分数为20%的氯化钠溶液,所需氯化钠的质量为_______g.(3)溶解过程中玻璃棒的作用是_______。(4)对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有_______(填序号)。A.氯化钠中混有不溶性杂质 B.量取水的体积时,仰视读数C.装瓶时,有少量溶液洒出 D.氯化钠没有完全溶解(5)把500g质量分数为。的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是______g。2、研究溶液对于生产、生活有着重要意义。(1)水是常用溶剂,某同学进行图甲实验。①倾斜a试管,沿内壁缓缓加入乙醇,不振荡,现象是_______。②由实验可知,溶质状态可以是_____________。③实验结束后,用洗涤剂洗净b试管,原理是____________。(2)图乙是A、B、C三种物质(不含结晶水)的溶解度曲线。①P点的含义是____________。②将t2℃时90gA的饱和溶液降温至t1℃,析出A的质量为__________。③t2℃时,若从A和B两种物质的饱和溶液中析出等质量的固体,需蒸发掉较多水的是________(填“A”或“B”)物质的饱和溶液。(3)按图丙所示装置,将液体x注入装有固体y的试管中,会导致U形管中a端液面低于b端液面,则试剂x、y的组合可能是 。A.水、硝酸铵 B.水、氢氧化钠C.水、氧化钙 D.稀盐酸、镁3、甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为___________g。(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是___________。(3)现有操作步骤:a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是___________。(填字母序号)(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数___________(填“变大”“变小”或“不变”)4、如图是几种固体物质的溶解度曲线,回答(1)10℃时硝酸铵的溶解度是___________。(2)10℃时把10g氯化钠加入到100g水中充分搅拌,观察到的现象是_____,溶液中存在的溶质的粒子是_______。(3)约______℃时硝酸钠和硝酸钾的溶解度相等。(4)70℃ 50g水中最多溶解氯化铵的质量是______。(5)80℃时150g硝酸钾放入100g水中,充分搅拌,所得溶液中溶质的质量是______,溶质的质量分数是________。小红用此溶液通过降温结晶得到硝酸钾晶体,得到60g硝酸钾晶体需要把溶液温度降至__________℃。5、化学与生产、生活联系紧密。(1)北京冬奥会火炬“飞扬”使用液氢作为燃料,实现零碳排放,践行“绿色冬奥”理念。氢气燃烧的化学方程式为____。(2)泰州为举办省运会新建了许多场馆,使用了大量铝制品材料。铝制品耐腐蚀的原因是____。(3)家庭厨房中用洗洁精清洗油污,利用了洗洁精的____作用。(4)农业上配制100kg,15%的食盐溶液用来选种,需要食盐____kg。(5)生铁和钢性能不同主要是由于____不同。(6)自来水生产过程中一般用氯气(Cl2)杀菌消毒,标出氯气中氯元素的化合价____。(7)氧气的工业制法为分离液态空气法,则氮气的工业制法为____。三、计算题(每小题4分,共计36分)1、将13克的锌粒放入87.4克的稀盐酸中,当锌粒完全反应后:(1)最多可以放出多少克的氢气?(2)盐酸溶液中溶质的质量分数是多少?2、现在 70g20%的硫酸铵溶液,试计算下列问题。(1)若向上述溶液中加入 30g 水,求所得溶液中溶质的质量分数?(2)若向上述溶液中加入10g 硫酸铵,完全溶解,求所得溶液中硫酸铵的质量分数?3、将含杂质的铁样品7g放入盛有121.6g稀盐酸溶液的烧杯中,刚好完全反应(杂质既不溶于水,也不与酸反应),称得反应后烧杯内物质的总质量为128.4g。(已知:铁与稀盐酸反应生成氯化亚铁和氢气)求(1)生成氢气的质量_____。(2)铁样品中铁的质量分数_____。4、我国第一艘国产航母的许多电子元件使用了黄铜(假设合金中仅含铜,锌),兴趣小组同学向盛有30g黄铜样品的烧杯中逐渐加入稀硫酸,生成氢的质量与加入稀硫酸的质量关系如图所示,计算:(1)充分反应后生成氢气的质量为___________g。(2)硫酸溶液中溶质的质量分数。5、实验室有一瓶含有杂质并且部分变质的氢氧化钠样品(其中杂质不含钠元素也不溶于水)。实验小组同学进行了如下实验:请回答下列问题:(1)上述实验过程中发生反应的化学方程式_____。(2)根据已知条件列出样品中参加反应的物质质量(X)的比例式_____。(3)此样品中未变质的氢氧化钠的质量分数为_____。(4)将反应后溶液蒸发21.8g水,所得溶液中溶质的质量分数为_____。(5)将最终所得溶液加水进行稀释,需要的仪器有:烧杯、玻璃棒、_____。6、小樱同学在实验室进行有关浓硫酸溶液的实验,试剂瓶上的标签如下表所示。她从瓶中倒出20mL用于配制稀硫酸溶液。请计算:浓硫酸溶液(H2SO4)500mL溶质的质量分数98%密度1. 84 g/cm3强腐蚀性,阴冷,密封储藏 (1)这20mL浓硫酸溶液的质量为___________g。(2)她将这20mL浓硫酸溶液与100mL水均匀混合,水的密度为1g/cm3所得稀硫酸溶液中溶质的质量分数是多少?(结果保留到小数点后一位)7、某化工厂排放的废水中含有碳酸钾和氯化钾,十五中化学兴趣小组为探究废水中碳酸钾的含量,提取50g废水样品于容器中,逐滴加入9.8%的稀硫酸,反应过程中产生二氧化碳的质量与加入稀硫酸的质量如图。请计算:(提示:碳酸钾与硫酸反应的化学方程式为,氯化钾不与酸反应)(1)生成二氧化碳的质量为_________g。(2)该废水中碳酸钾的质量分数为多少?(写出计算过程)(3)反应后生成硫酸钾的质量为多少?8、为测定某氯化钠溶液中溶质的质量分数,做如下实验:向烧杯中加入10 g该氯化钠溶液,然后向其中滴加硝酸银溶液,发生反应生成氯化银沉淀。滴加硝酸银溶液质量与产生沉淀质量关系如图所示。根据实验计算:(1)该反应生成沉淀的质量为______克。(2)该氯化钠溶液中溶质的质量分数为多少?(提示:化学反应方程式为 NaCl+AgNO3=NaNO3+AgCl↓)9、某化学兴趣小组取部分变质的 Ca(OH)2(含杂质 CaCO3)样品8.0g投入200.0g水中,充分搅拌,通入足量CO2,溶质质量与反应的 CO2质量的关系如图所示。[提示:CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2能溶于水](1)Ca(OH)2全部转化为CaCO3时消耗的CO2 质量为______g。(2)8.0g样品中杂质CaCO3 的质量为多少?(3)通入 m3g CO2时,溶液中溶质的质量为多少?四、实验探究(每小题5分,共计20分)1、学习小组在学习“二氧化碳制取的研究”课题时,探究了二氧化碳气体的收集方法。(查阅资料)通常状况下,1体积水约能溶解1体积二氧化碳,所得溶液pH 约为5.6。(提出问题)二氧化碳能不能用排水法收集?(实验设计与操作)在通常状况下,测定二氧化碳溶于水所得溶液的pH,判断二氧化碳在水中的溶解度(体积)。(1)甲装置中反应的化学方程式是______。(2)实验时,需先将如图甲装置中的空气排尽。其操作是:开启弹簧夹K1、关闭弹簧夹K2,打开活塞,滴加稀盐酸至空气排尽。检验空气已排尽的方法是______。(3)关闭K1,打开K2、K3。待丙装置中收集半瓶气体时,关闭活塞K2和K3,充分振荡丙装置。然后用pH 计测得如下数据:物质丙装置中溶液丁装置中溶液pH5.606.50分析可知,在丙和丁装置中所溶解二氧化碳的体积______(填“大于”、“小于”或“等于”)丙和丁装置中溶液的总体积。(4)实验中,若没有乙装置,则测出的溶液pH 会______。(填“偏大”、“偏小”、或“不变”)(结论与反思)(5)由实验结果分析,你认为二氧化碳______(填“能”或“不能”)用排水法收集,收集时能减少二氧化碳在水中溶解度的措施是______(写一点即可)。(6)学习小组另取2.5g大理石粉末,逐滴加入7.3%的稀盐酸至不再产生气泡时,共消耗了20g 7.3%的稀盐酸,则该大理石粉末的纯度为______(杂质不与盐酸反应)。2、高锰酸钾在生产、生活中有广泛应用。实验小组的同学对高锰酸钾的某些性质和用途进行探究。实验一、高锰酸钾制取氧气:如图,用下列给定的药品、用品:高锰酸钾、棉花、火柴及下列仪器,制取氧气.(1)仪器⑤的名称是_______________;(2)制取并收集氧气时,应选用图中的仪器有_________。(填序号);利用此原理还需要补充的一种仪器是_________,在此实验中该仪器的用途是___________,该反应的方程式为:________________,根据所给仪器收集该气体应采用的收集方法是____。(3)实验时需要使用酒精灯,下列使用酒精灯的操作正确的是__________(从图中选出正确的操作编号).(4)小明用高锰酸钾制备氧气实验结束时,先熄灭酒精灯,导致水槽中的水倒流进人了导气管,可采用的补救措施是__________________(答一种即可)。实验二、探究高锰酸钾的溶解性:小组同学设计了如图所示实验,请根据实验操作图示回答相关问题:(1)步骤一:如图操作,振荡后静置,观察到:A试管中晶体全部溶解,溶液呈____色;B试管中晶体不溶解,汽油不变色;根据此实验可知影响物质溶解性的因素是__________。(2)步骤二:如图操作,将步骤一中A试管内溶液倒人B试管中,振荡后静置,观察现象。请你对B试管中出现的现象提出猜想并说明理由:________________________。实验三、高锰酸钾溶液检验二氧化硫:如图所示,在小烧杯A中加入少量的稀高锰酸钾溶液。取一根小木条,在一头蘸一些硫粉,并点燃,迅速伸人烧杯B中,片刻后取出小木条,振荡烧杯A,可观察到烧杯A中出现的现象是 _____,该反应的化学方程式可表示为,其中X的化学式是_____,反应前后锰元素和硫元素化合价发生的变化分别是__________________。I拓展实验实验过程中某同学的手上不小心沾上了高锰酸钾溶液,结果手上的皮肤变成了棕黄色,经过查阅资料结合已学过的化学知识分析原因,并在老师的指导下进行了如下拓展实验探究:查阅资料:KMnO4溶液呈中性、有腐蚀性讨论分析:构成皮肤细胞的基础物质是蛋白质,其属于_________(填“有机高分子化合物”或“碳水化合物”),遇到高锰酸钾溶液后被腐蚀,因此皮肤呈现棕黄色。进行如下两个实验探究KMnO4溶液对不同类物质的腐蚀性:实验四、将新鲜鸡皮在不同浓度的KMnO4溶液中浸泡相同时间,现象如表:KMnO4溶液浓度0.002%0.01%0.1%1%鸡皮的变化无明显变化边缘部分变为棕黄色全部变为棕色全部变为黑色 实验五、将铜片分别浸泡在4种溶液中进行实验,浸泡相同时间,现象如下表:编号①②③④实验25mL0.1% KMnO4溶液25mL0.1%KMnO4溶液+10滴浓硫酸25mL蒸馏水+10滴浓硫酸25mL1%KMnO4溶液+10滴浓硫酸铜片质量/g实验前0.540.540.540.5418小时后0.540.520.540.43解释与结论:(1)实验四的目的是_______________________________;(2)实验五中通过对比②和④,得出的结论是______________________________;(3)实验2中,欲得出“KMnO4和硫酸共同作用对铜才有腐蚀性”的结论,需要对比______(填编号)。3、实验小组同学在一定温度下进行硝酸钾的固体的溶解实验。(定性研究)同学们进行如下实验,发现1号试管中硝酸钾全部溶解,2号试管中固体没有完全溶解。要使2号试管中的固体全部溶解,可采取的方法有______。(列举一条即可)。(定量研究)实验小组同学在一定温度下进行硝酸钾的固体溶液实验。实验数据如下:实验序号实验1实验2实验3实验4水的质量(g)100100100100加入硝酸钾的质量(g)80100120140溶液质量(g)180200210M请根据数据进行分析:(1)请计算实验2所得溶液中硝酸钾的质量分数是____________。(2)现将实验2中的溶液稀释成10%的硝酸钾溶液,需要加水的质量为____________g。(3)请判断实验2中硝酸钾溶液是____________溶液。(选填“饱和”或“不饱和”)(4)实验4中M的数值是____________。4、据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。(提出问题)从废旧手机中可以回收到哪些有价值的金属?如何回收?(查阅资料)Ⅰ.手机电路板中的金属及其价格如下表所示:种类FeCuAlNiAuAgPd(钯)市场价格/($/t)3657175.51710.5142354.7×1077.6×1052.7×107矿石中含量72.40.8729.11.0241200.4手机电路板中含量51310.13501380210说明:Fe、Cu、Al、Ni的含量用质量分数(%)表示,Au、Ag、Pd的含量的单位为“g/t”。Ⅱ.Ni的金属活动性位于氢前;Pd的金属活动性位于氢后;NiCl2溶液为绿色。(实验方案)第一步:选择值得回收的金属。依据资料Ⅰ中的数据,废旧手机中有回收价值的金属有Au、Ag、Cu、Pd,(1)原因是:①它们的市场价格较高;② _____ 。第二步:设计实验分离、回收部分金属。序号实验步骤实验现象Ⅰ取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出焊锡熔化Ⅱ将金属电路放入烧杯中,加入过量10%的稀盐酸浸泡……Ⅲ取Ⅱ中未溶解的金属电路,用蒸馏水洗净后,放入如上图所示装置中,进行实验。溶液逐渐变成蓝色,仍有微量金属固体未溶解Ⅳ过滤Ⅲ中烧杯中的物质,洗涤滤纸上的物质滤纸上仍有微量金属固体(问题讨论)(2)由步骤I中的现象,可推知的焊锡的物理性质是 _____ (填字母)。a.熔点低 b.硬度大 c.抗腐蚀性强(3)步骤Ⅱ中实验室用溶质质量分数为37%、密度是1.18g•mL-1的浓盐酸配制10%的盐酸185g,需要浓盐酸 _____ mL;配制该稀盐酸应选择的量筒量程(水的密度为1g/cm3)为 _____ (填字母)。a.10mL b.50mL c.100mL d.200mL(4)步骤Ⅱ所得溶液中,至少含有 _____ (填数字)种溶质,该步骤中对应的实验现象是 _____ 。(5)请写出步骤Ⅲ中,溶液变成蓝色的化学方程式 _____ 。(6)步骤Ⅳ中过滤操作用到的玻璃仪器有玻璃棒、 _____ 和 _____ ,其中玻璃棒的作用是 _____ 。
相关试卷
这是一份2022年最新人教版九年级化学下册第九单元溶液期中复习试卷各版本,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2022年最新人教版九年级化学下册第九单元溶液期中复习试卷【各版本】,共14页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。
这是一份2021学年最新人教版九年级化学下册第九单元溶液期中复习试卷【各版本】,共15页。试卷主要包含了单选题,填空题,计算题,实验探究等内容,欢迎下载使用。









