所属成套资源:人教版化学初三下学期教学设计+PPT课件+训练题+学案+视频全册
人教版课题3 溶液的浓度一等奖教学设计
展开
这是一份人教版课题3 溶液的浓度一等奖教学设计,共5页。教案主要包含了提出问题,引导回答,讨论与交流,指引观察,指导自学等内容,欢迎下载使用。
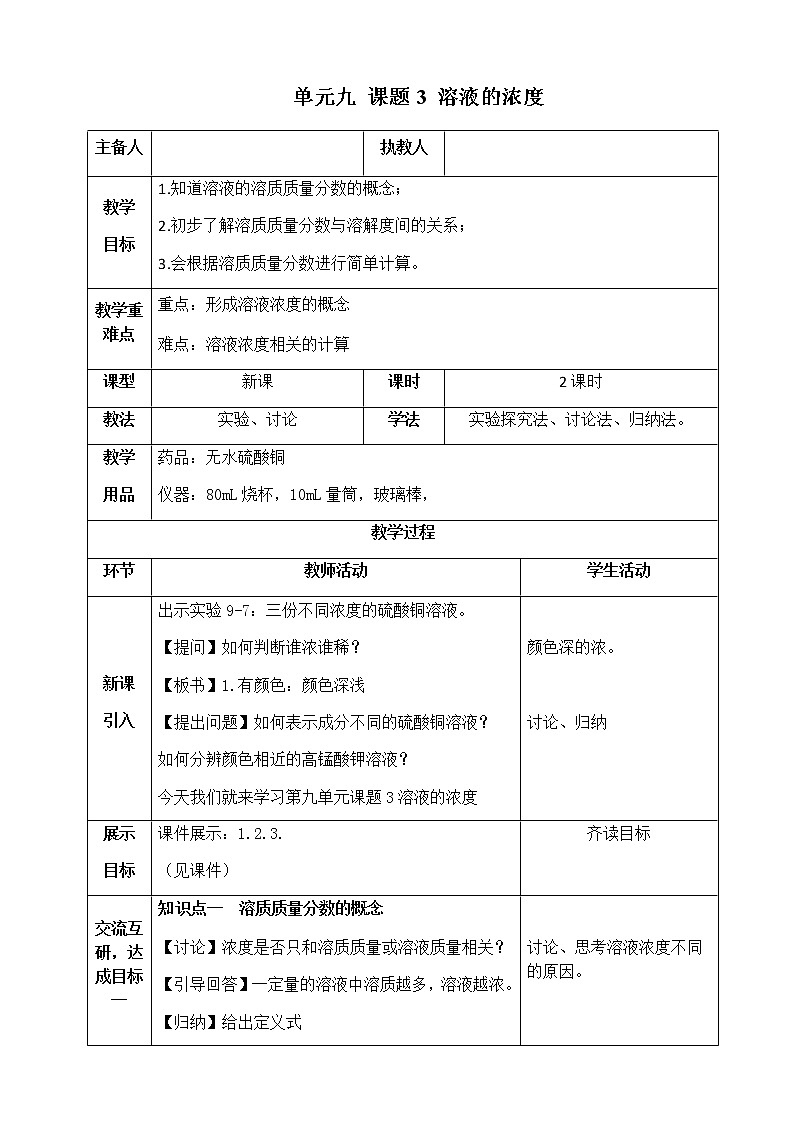
主备人
执教人
教学
目标
1.知道溶液的溶质质量分数的概念;
2.初步了解溶质质量分数与溶解度间的关系;
3.会根据溶质质量分数进行简单计算。
教学重难点
重点:形成溶液浓度的概念
难点:溶液浓度相关的计算
课型
新课
课时
2课时
教法
实验、讨论
学法
实验探究法、讨论法、归纳法。
教学
用品
药品:无水硫酸铜
仪器:80mL烧杯,10mL量筒,玻璃棒,
教学过程
环节
教师活动
学生活动
新课
引入
出示实验9-7:三份不同浓度的硫酸铜溶液。
【提问】如何判断谁浓谁稀?
【板书】1.有颜色:颜色深浅
【提出问题】如何表示成分不同的硫酸铜溶液?
如何分辨颜色相近的高锰酸钾溶液?
今天我们就来学习第九单元课题3溶液的浓度
颜色深的浓。
讨论、归纳
展示
目标
课件展示:
(见课件)
齐读目标
交流互研,达成目标一
知识点一 溶质质量分数的概念
【讨论】浓度是否只和溶质质量或溶液质量相关?
【引导回答】一定量的溶液中溶质越多,溶液越浓。
【归纳】给出定义式
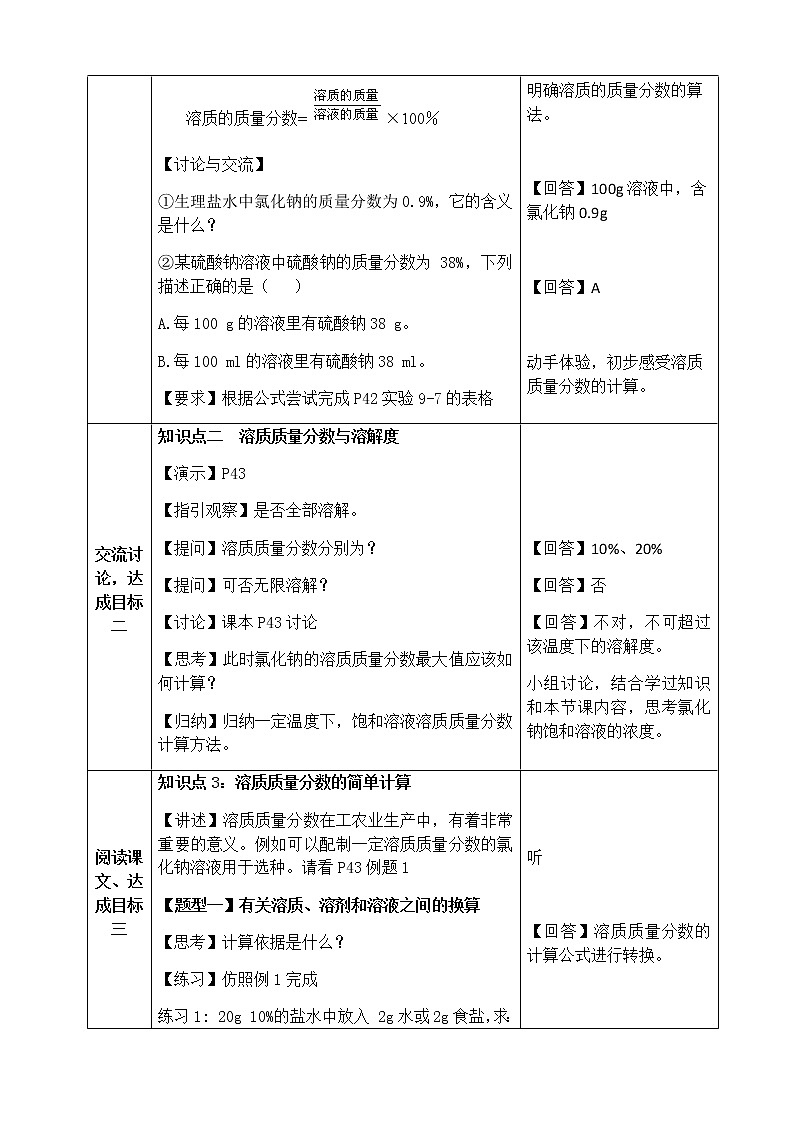
溶质的质量分数= ×100%
【讨论与交流】
①生理盐水中氯化钠的质量分数为0.9%,它的含义是什么?
②某硫酸钠溶液中硫酸钠的质量分数为 38%,下列描述正确的是( )
A.每100 g的溶液里有硫酸钠38 g。
B.每100 ml的溶液里有硫酸钠38 ml。
【要求】根据公式尝试完成P42实验9-7的表格
讨论、思考溶液浓度不同的原因。
明确溶质的质量分数的算法。
【回答】100g溶液中,含氯化钠0.9g
【回答】A
动手体验,初步感受溶质质量分数的计算。
交流讨论,达成目标二
知识点二 溶质质量分数与溶解度
【演示】P43
【指引观察】是否全部溶解。
【提问】溶质质量分数分别为?
【提问】可否无限溶解?
【讨论】课本P43讨论
【思考】此时氯化钠的溶质质量分数最大值应该如何计算?
【归纳】归纳一定温度下,饱和溶液溶质质量分数计算方法。
【回答】10%、20%
【回答】否
【回答】不对,不可超过该温度下的溶解度。
小组讨论,结合学过知识和本节课内容,思考氯化钠饱和溶液的浓度。
阅读课文、达成目标三
知识点3:溶质质量分数的简单计算
【讲述】溶质质量分数在工农业生产中,有着非常重要的意义。例如可以配制一定溶质质量分数的氯化钠溶液用于选种。请看P43例题1
【题型一】有关溶质、溶剂和溶液之间的换算
【思考】计算依据是什么?
【练习】仿照例1完成
练习1: 20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。
练习2: 20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。
【题型二】饱和溶液中溶质的质量分数计算
【提问】由P43的讨论可知,饱和溶液中溶质的质量分数的计算依据是?
【练习】计算说明,能否配制出20℃溶质质量分数为30%的食盐水?
【题型三】溶液的浓稀问题
【思考】向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算?
【指导自学】请看课本P44例题2.找出计算的关键。
【归纳】计算的依据:
稀释前溶质质量 = 稀释后溶质质量
浓缩前溶质质量 = 浓缩后溶质质量
【练习】配制10%硫酸98g,要98%硫酸(密度为1.84g/m L)多少mL?
【题型四】有关化学方程式的简单计算
中考链接:分析下面哪种解法正确?(见课件)
【强调】不是纯物质的质量不能直接带入化学方程式进行计算。
【练习】100g 9.8%硫酸跟多少克锌完全反应?同时生成多少克氢气?
【练习】实验室用100g稀硫酸和一定量的锌完全反应,制得0.8g氢气。求该稀硫酸溶质的质量分数。
听
【回答】溶质质量分数的计算公式进行转换。
计算、交流、回答
思考、回答:不变,溶液是均一稳定的混合物
否,最多26.5%
阅读,并找到溶液稀释前后,溶质的质量不变。
听、看、记
动笔计算
回答。说明理由,100g稀硫酸不是纯物质。要使用纯物质进行计算。
动笔计算,并分享过程和答案。
归纳
总结
回顾学习目标,思考所学,提出疑问。
回顾所学,归纳小结
当堂
检测
实践出真知,请大家完成下列检测:
第一课时
1.配制100mL密度为1.1g/mL的20%的NaCl溶液需要多少gNaCl和多少g水?
2.配制500m L20%的硫酸溶液(密度为1.14g/mL)需要98%硫酸溶液(密度为1.84g / mL )多少mL ?
第二课时
3.40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少?
布置
作业
第一课时:手写作业: P45 2.3.7
第二课时:手写作业: P45
记录并完成
主板书设计
9.3溶液的浓度
一、溶液浓度的判断
1.有色:颜色深浅
2.精确:溶质质量分数、
二、溶质质量分数
1.概念:溶质质量与溶液质量之比。
2.计算公式:
三、有关溶质质量分数的简单计算
1. 有关溶质、溶剂和溶液之间的换算
2. 饱和溶液中溶质的质量分数计算
3. 溶液的浓稀问题
4. 有关化学方程式的简单计算
教学
后记
相关教案
这是一份初中化学人教版九年级下册课题3 溶液的浓度第2课时教案,共5页。教案主要包含了教学目标,教学重难点,教学准备,教学过程,板书设计等内容,欢迎下载使用。
这是一份化学九年级下册课题3 溶液的浓度教案,文件包含第9单元课题3第1课时DOC、第9单元课题3第2课时DOC等2份教案配套教学资源,其中教案共0页, 欢迎下载使用。
这是一份化学九年级下册课题3 溶液的浓度教案设计,共12页。教案主要包含了学习目标,课前准备,新课学习,跟踪练习1,重点题型,解题秘籍,易错解答,基础过关等内容,欢迎下载使用。










